Generiskt Namn: terbutalin sulfate
doseringsform: injektion, lösning
medicinskt granskad av Drugs.com. Senast uppdaterad den Sep 1, 2020.
- översikt
- biverkningar
- dosering
- Professional
- interaktioner
- mer
en steril vattenlösning för subkutan injektion
endast Rx
varning: förlängd tokolys
Terbutalinsulfat har inte godkänts och bör inte användas för långvarig tokolys (längre än 48-72 timmar). I synnerhet bör Terbutalinsulfat inte användas för underhållstokolys i öppenvården eller hemmet. Allvarliga biverkningar, inklusive dödsfall, har rapporterats efter administrering av Terbutalinsulfat till gravida kvinnor. Hos modern inkluderar dessa biverkningar ökad hjärtfrekvens, övergående hyperglykemi, hypokalemi, hjärtarytmier, lungödem och myokardiell ischemi. Ökad fetal hjärtfrekvens och neonatal hypoglykemi kan uppstå som ett resultat av moderns administrering (se kontraindikationer: långvarig tokolys).
- terbutalin beskrivning
- terbutalin – klinisk farmakologi
- prekliniska
- farmakokinetik
- indikationer och användning för terbutalin
- kontraindikationer
- varningar
- försämring av astma
- användning av antiinflammatoriska medel
- kardiovaskulära effekter
- kramper
- försiktighetsåtgärder
- allmänt
- läkemedelsinteraktioner
- karcinogenes, mutagenes, nedsatt fertilitet
- graviditet-teratogena effekter
- användning vid arbete och leverans
- ammande mödrar
- pediatrisk användning
- geriatrisk användning
- biverkningar
- överdosering
- terbutalin dosering och administrering
- hur levereras terbutalin
- HUVUDDISPLAYPANEL
- huvuddisplaypanel
- SERIALIZATION IMAGE
- mer om terbutalin
- konsumentresurser
- professionella resurser
- relaterade behandlingsguider
terbutalin beskrivning
Terbutalinsulfat, USP, den aktiva beståndsdelen i Terbutalinsulfatinjektion, USP, är en beta-adrenerg agonist bronkodilator tillgänglig som en steril, icke-pyrogen vattenlösning i injektionsflaskor, för subkutan administrering. Varje milliliter lösning innehåller 1 mg Terbutalinsulfat, USP (0,82 mg av den fria basen), natriumklorid för isotonicitet, 0,055% edetatdinatriumdihydrat som stabiliseringsmedel och saltsyra för justering till ett mål pH på 4. Terbutalin sulfate är (kub) – a–3,5 – dihydroxibenzyi alkoholsulfat (2:1) (salt). Molekylformeln är (C12H19N03) 2 * H2SO4 och strukturformeln är:
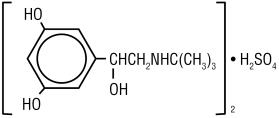
Terbutalinsulfat, USP är ett vitt till gråvitt kristallint pulver. Det är luktfritt eller har en svag lukt av ättiksyra. Det är lösligt i vatten och i 0,1 n saltsyra, något lösligt i metanol och olösligt i kloroform. Dess molekylvikt är 548,65.
terbutalin – klinisk farmakologi
terbutalinsulfatinjektion är en beta-adrenerg receptoragonist. In vitro och in vivo farmakologiska studier har visat att terbutalin utövar en förmånlig effekt på beta2‑adrenerga receptorer. Även om det är erkänt att beta2-adrenerga receptorer är de dominerande receptorerna i bronkial glatt muskulatur, indikerar data att det finns en population av beta2-receptorer i det mänskliga hjärtat, som finns i en koncentration mellan 10% och 50%. Den exakta funktionen hos dessa receptorer har inte fastställts (se varningar). Kontrollerade kliniska studier på patienter som fått terbutalin subkutant har inte visat någon förmånlig beta2-adrenerg effekt.
de farmakologiska effekterna av beta – adrenerga agonister, inklusive terbutalin, är åtminstone delvis hänförliga till stimulering genom beta-adrenerga receptorer av intracellulärt adenylcyklas, enzymet som katalyserar omvandlingen av adenosintrifosfat (ATP) till cykliskt 3′,5′-adenosinmonofosfat (cAMP). Ökade cAMP-nivåer är förknippade med avslappning av bronkial glatt muskulatur och hämning av frisättning av mediatorer av omedelbar överkänslighet från celler, särskilt från mastceller.kontrollerade kliniska studier har visat att Terbutalinsulfatinjektion lindrar bronkospasm vid akut och kronisk obstruktiv lungsjukdom genom att signifikant öka lungflödeshastigheten (t.ex. en ökning med 15% eller mer i FEV1). Efter subkutan administrering av 0,25 mg terbutalinsulfatinjektion sker en mätbar förändring av expiratorisk flödeshastighet vanligtvis inom 5 minuter och en kliniskt signifikant ökning av FEV1 sker inom 15 minuter. Den maximala effekten uppträder vanligtvis inom 30 till 60 minuter, och kliniskt signifikant bronkodilatoraktivitet kan fortsätta i 1,5 till 4 timmar. Varaktigheten av kliniskt signifikant förbättring är jämförbar med den som observerats med equimilligramdoser av epinefrin.
prekliniska
studier på försöksdjur (minipigs, gnagare och hundar) har visat förekomsten av hjärtarytmier och plötslig död (med histologiska bevis på myokardiell nekros) när beta-agonister och metylxantiner administreras samtidigt. Den kliniska betydelsen av dessa fynd är okänd.
farmakokinetik
subkutan administrering av 0, 5 mg Terbutalinsulfat till 17 friska, vuxna, manliga försökspersoner resulterade i genomsnittlig (SD) topp plasmakoncentration av terbutalin på 9, 6 (3, 6) ng/mL, vilket observerades vid en median (intervall) tid på 0, 5 (0, 08 till 1, 0) timmar efter dosering. Medelvärdet (SD) AUC (0 till 48) och det totala kroppsclearance var 29,4 (14,2) h•ng/mL respektive 311 (112) mL/min. Den terminala halveringstiden bestämdes hos 9 av de 17 patienterna och hade ett medelvärde (SD) på 5, 7 (2, 0) timmar.
efter subkutan administrering av 0, 25 mg Terbutalinsulfat till två manliga försökspersoner observerades maximala serumkoncentrationer av terbutalin på 5, 2 och 5, 3 ng/mL cirka 20 minuter efter dosering.
halveringstiden för läkemedlet hos 10 av 14 patienter var cirka 2,9 timmar efter subkutan administrering, men längre halveringstider för eliminering (mellan 6 och 14 timmar) hittades hos de andra 4 patienterna. Cirka 90% av läkemedlet utsöndrades i urinen 96 timmar efter subkutan administrering, varav cirka 60% av detta var oförändrat läkemedel. Det verkar som om sulfatkonjugatet är en huvudmetabolit av terbutalin och urinutsöndring är den primära elimineringsvägen.
indikationer och användning för terbutalin
Terbutalinsulfatinjektion, USP är indicerat för förebyggande och återföring av bronkospasm hos patienter 12 år och äldre med astma och reversibel bronkospasm associerad med bronkit och emfysem.
kontraindikationer
1. Förlängd tokolys
Terbutalinsulfat har inte godkänts och bör inte användas för långvarig tokolys (längre än 48-72 timmar). I synnerhet bör Terbutalinsulfat inte användas för underhållstokolys i öppenvården eller hemma (se boxad varning: långvarig tokolys).
2. Överkänslighet
Terbutalinsulfatinjektion är kontraindicerad hos patienter som är kända för att vara överkänsliga mot sympatomimetiska aminer eller någon komponent i denna läkemedelsprodukt.
varningar
försämring av astma
astma kan försämras akut under en period av timmar eller kroniskt under flera dagar eller längre. Om patienten behöver fler doser Terbutalinsulfat än vanligt kan detta vara en markör för destabilisering av astma och kräver omvärdering av patienten och behandlingsregimen, med särskild hänsyn till det möjliga behovet av antiinflammatorisk behandling, t.ex. kortikosteroider.
användning av antiinflammatoriska medel
användningen av enbart beta-adrenerga agonistbronkodilatorer är kanske inte tillräcklig för att kontrollera astma hos många patienter. Tidigt övervägande bör ges till tillsats av antiinflammatoriska medel, t.ex. kortikosteroider.
kardiovaskulära effekter
Terbutalinsulfat, liksom alla andra beta-adrenerga agonister, kan ge en kliniskt signifikant kardiovaskulär effekt hos vissa patienter mätt med puls, blodtryck och / eller symtom. Även om sådana effekter är ovanliga efter administrering av Terbutalinsulfat vid rekommenderade doser, kan läkemedlet behöva avbrytas om de uppstår. Dessutom har beta‑agonister rapporterats producera elektrokardiogramförändringar (EKG), såsom utplattning av T-vågen, förlängning av QTc-intervallet och St-segmentdepression. Den kliniska betydelsen av dessa fynd är okänd. Därför bör Terbutalinsulfat, liksom alla sympatomimetiska aminer, användas med försiktighet hos patienter med hjärt-kärlsjukdomar, särskilt koronarinsufficiens, hjärtarytmier och högt blodtryck.
kramper
det har förekommit sällsynta rapporter om anfall hos patienter som fick terbutalin; anfall återkom inte hos dessa patienter efter att läkemedlet avbröts.
försiktighetsåtgärder
allmänt
terbutalin, som med alla sympatomimetiska aminer, ska användas med försiktighet hos patienter med hjärt-kärlsjukdomar, inklusive ischemisk hjärtsjukdom, hypertoni och hjärtarytmier; hos patienter med hypertyreoidism eller diabetes mellitus; och hos patienter som är ovanligt mottagliga för sympatomimetiska aminer eller som har konvulsiva störningar. Signifikanta förändringar i systoliskt och diastoliskt blodtryck har setts och kan förväntas inträffa hos vissa patienter efter användning av någon beta-adrenerg bronkodilator.omedelbara överkänslighetsreaktioner och exacerbationer av bronkospasm har rapporterats efter administrering av terbutalin.
beta – adrenerga agonistläkemedel kan ge signifikant hypokalemi hos vissa patienter, eventuellt genom intracellulär skakning, vilket har potential att ge negativa kardiovaskulära effekter. Minskningen är vanligtvis övergående och kräver inte tillskott.
stora doser intravenös terbutalin har rapporterats förvärra befintlig diabetes mellitus och ketoacidos.
läkemedelsinteraktioner
samtidig användning av terbutalinsulfatinjektion med andra sympatomimetiska medel rekommenderas inte, eftersom den kombinerade effekten på kardiovaskulärsystemet kan vara skadlig för patienten.
monoaminoxidashämmare eller tricykliska antidepressiva medel:terbutalin ska administreras med extrem försiktighet till patienter som behandlas med monoaminoxidashämmare eller tricykliska antidepressiva medel, eller inom 2 veckor efter avbrytande av sådana medel, eftersom Terbutalins verkan på kärlsystemet kan förstärkas.
betablockerare: Beta – adrenerga receptorblockerande medel blockerar inte bara den pulmonella effekten av beta-agonister, såsom Terbutalinsulfatinjektion, men kan ge allvarlig bronkospasm hos astmatiska patienter. Därför bör patienter med astma normalt inte behandlas med betablockerare. Under vissa omständigheter, t.ex. som profylax efter hjärtinfarkt, kan det emellertid inte finnas några acceptabla alternativ till användningen av beta-adrenerga blockerande medel hos patienter med astma. I denna inställning kan kardioselektiva betablockerare övervägas, även om de bör administreras med försiktighet.
diuretika: EKG-förändringar och / eller hypokalemi som kan bero på administrering av icke-kaliumsparande diuretika (såsom loop-eller tiaziddiuretika) kan akut förvärras av beta-agonister, särskilt när den rekommenderade dosen av beta-agonisten överskrids. Även om den kliniska betydelsen av dessa effekter inte är känd, rekommenderas försiktighet vid samtidig administrering av beta-agonister med icke-kaliumsparande diuretika.
karcinogenes, mutagenes, nedsatt fertilitet
i en 2-årig studie på Sprague‑Dawley-råttor orsakade Terbutalinsulfat en signifikant och dosrelaterad ökning av förekomsten av godartade leiomyom i mesovariet vid kostdoser på 50 mg/kg och högre (cirka 810 gånger den maximala rekommenderade dagliga subkutana dosen (sc) för vuxna på mg/m2-basis). I en 21-månadersstudie på CD-1-möss visade Terbutalinsulfat inga tecken på tumorigenicitet vid kostdoser upp till 200 mg/kg (cirka 1600 gånger den maximala rekommenderade dagliga sc-dosen för vuxna på mg/m2-basis). Mutagenicitetspotentialen för Terbutalinsulfat har inte fastställts.reproduktionsstudier på råttor som använde Terbutalinsulfat visade ingen nedsatt fertilitet vid orala doser upp till 50 mg/kg (cirka 810 gånger den maximala rekommenderade dagliga sc-dosen för vuxna på mg/m2-basis).
graviditet-teratogena effekter
graviditetskategori C
det finns inga adekvata och välkontrollerade studier av Terbutalinsulfat hos gravida kvinnor. Publicerade djurstudier visar att råttavkommor uppvisar förändringar i beteende och hjärnutveckling, inklusive minskad cellulär proliferation och differentiering när dammar behandlades subkutant med terbutalin under det sena stadiet av graviditet och laktationsperiod. Terbutalinexponeringen hos råttdammar var cirka 24 till 48 gånger den vanliga humana dosen hos vuxna på 2-4 mg/dag, baserat på mg/m2.
Terbutalinsulfat har inte godkänts och bör inte användas för långvarig tokolys (längre än 48-72 timmar). I synnerhet bör Terbutalinsulfat inte användas för underhållstokolys i öppenvården eller hemmet. Allvarliga biverkningar, inklusive dödsfall, har rapporterats efter administrering av Terbutalinsulfat till gravida kvinnor. Hos modern inkluderar dessa biverkningar ökad hjärtfrekvens, övergående hyperglykemi, hypokalemi, hjärtarytmier, lungödem och myokardiell ischemi. Ökad fetal hjärtfrekvens och neonatal hypoglykemi kan uppstå som ett resultat av moderns administrering (se Boxed varning: långvarig tokolys och kontraindikationer: långvarig tokolys).
i embryofetala utvecklingsstudier på djur observerades inga teratogena effekter hos avkomman när dräktiga råttor och kaniner fick Terbutalinsulfat vid orala doser upp till 50 mg/kg/dag, cirka 810 respektive 1600 gånger, den maximala rekommenderade dagliga subkutana dosen för vuxna, på mg/m2-basis.
Terbutalinsulfat ska endast användas under graviditet om de potentiella fördelarna motiverar den potentiella risken för fostret.
användning vid arbete och leverans
på grund av risken för beta-agonistinterferens med livmoderkontraktilitet bör användning av terbutalinsulfatinjektion för lindring av bronkospasm under arbetet begränsas till de patienter i vilka fördelarna klart överväger risken.
terbutalin korsar placentan. Efter administrering av engångsdos IV av terbutalin till 22 kvinnor i sen graviditet som levererades av valfri kejsarsnitt på grund av kliniska skäl befanns navelblodnivåerna av terbutalin sträcka sig från 11% till 48% av moderns blodnivåer.
ammande mödrar
det är inte känt om detta läkemedel utsöndras i bröstmjölk. Därför bör terbutalinsulfatinjektion endast användas under omvårdnad om den potentiella nyttan motiverar den möjliga risken för den nyfödda.
pediatrisk användning
Terbutalinsulfatinjektion rekommenderas inte för patienter under 12 år på grund av otillräckliga kliniska data för att fastställa säkerhet och effektivitet.
geriatrisk användning
kliniska studier av Terbutalinsulfatinjektion inkluderade inte tillräckligt många försökspersoner över 65 år för att avgöra om de svarar annorlunda än yngre försökspersoner. Annan rapporterad klinisk erfarenhet har inte identifierat skillnader i svar mellan äldre och yngre patienter. I allmänhet bör dosval för en äldre patient vara försiktig, vanligtvis med början vid den låga änden av doseringsområdet, vilket återspeglar den större frekvensen av nedsatt lever -, njur-eller hjärtfunktion och samtidig sjukdom eller annan läkemedelsbehandling.
biverkningar
biverkningar som observerats med Terbutalinsulfatinjektion liknar de som vanligen ses med andra sympatomimetiska medel. Alla dessa reaktioner är övergående och kräver vanligtvis inte behandling.
Följande tabell jämför biverkningar som ses hos patienter som behandlats med Terbutalinsulfatinjektion (0,25 mg och 0,5 mg), med de som ses hos patienter som behandlats med epinefrininjektion (0,25 mg och 0,5 mg), under åtta dubbelblinda crossover-studier med totalt 214 patienter.
| Incidence (%) of Adverse Reactions | |||||
| Terbutaline (%) | Epinephrine (%) | ||||
|
0.25 mg |
0.5 mg N = 205 |
0.25 mg N = 153 |
0.5 mg N = 61 |
||
| Reaction Central Nervous System |
|||||
| Tremor | 7.8 | 38.0 | 16.3 | 18.0 | |
| Nervousness | 16.9 | 30.7 | 8.5 | 31.1 | |
| Dizziness | 1.3 | 10.2 | 7.8 | 3.3 | |
| Headache | 7.8 | 8.8 | 3.3 | 9.8 | |
| Drowsiness | 11.7 | 9.8 | 14.4 | 8.2 | |
| Cardiovascular | |||||
| Palpitations | 7.8 | 22.9 | 7.8 | 29.5 | |
| Tachycardia | 1.3 | 1.5 | 2.6 | 0.0 | |
| Respiratory | |||||
| Dyspnea | 0.0 | 2.0 | 2.0 | 0.0 | |
| Chest discomfort | 1.3 | 1.5 | 2.6 | 0.0 | |
| Gastrointestinal | |||||
| Nausea/vomiting | 1.3 | 3.9 | 1.3 | 11.5 | |
| Systemic | |||||
| Weakness | 1.3 | 0.5 | 2.6 | 1.6 | |
| Flushed feeling | 0.0 | 2.4 | 1.3 | 0.0 | |
| Sweating | 0.0 | 2.4 | 0.0 | 0.0 | |
| Pain at injection site | 2.6 | 0.5 | 2.6 | 1.6 | |
OBS: Vissa patienter fick mer än en dosstyrka av terbutalinsulfat och epinefrin. Dessutom fanns rapporter om ångest, muskelkramper och torr mun (< 0,5%). Det har förekommit sällsynta rapporter om förhöjda leverenzymer och överkänslighetsvaskulit vid administrering av terbutalin.
för att rapportera misstänkta biverkningar, kontakta Hikma Pharmaceuticals USA Inc.. vid 1-877-233-2001, eller FDA vid 1-800-FDA – 1088 eller www.fda.gov/medwatch.
överdosering
median sc dödlig dos av Terbutalinsulfat hos mogna råttor var cirka 165 mg/kg (cirka 2700 gånger den maximala rekommenderade dagliga sc-dosen för vuxna på mg/m2-basis). Median sc dödlig dos av Terbutalinsulfat hos unga råttor var cirka 2 000 mg/kg (cirka 32 000 gånger den maximala rekommenderade dagliga sc-dosen för vuxna på mg/m2-basis).
de förväntade symtomen vid överdosering är överdriven beta-adrenerg stimulering och / eller förekomst eller överdrift av något av de symtom som anges under biverkningar, t.ex. kramper, angina, hypertoni eller hypotoni, takykardi med hastigheter upp till 200 slag per minut, arytmier, nervositet, huvudvärk, tremor, muntorrhet, hjärtklappning, illamående, yrsel, trötthet, sjukdomskänsla och sömnlöshet. Hypokalemi kan också uppstå. Det finns ingen specifik motgift. Behandlingen består av avbrytande av Terbutalinsulfatinjektion tillsammans med lämplig symptomatisk behandling. Den förnuftiga användningen av en kardioselektiv beta-receptorblockerare kan övervägas, med tanke på att sådan medicinering kan ge bronkospasm. Det finns inte tillräckligt med bevis för att avgöra om dialys är fördelaktigt vid överdosering av Terbutalinsulfatinjektion.
terbutalin dosering och administrering
injektionsflaskor ska endast användas för subkutan administrering och inte intravenös infusion.sterilitet och noggrann dosering kan inte garanteras om injektionsflaskorna inte används i enlighet med dosering och administrering.
kassera oanvänd portion efter engångsbruk.
den vanliga subkutana dosen av terbutalinsulfatinjektion är 0,25 mg injicerad i det laterala deltoidområdet. Om signifikant klinisk förbättring inte sker inom 15 till 30 minuter kan en andra dos på 0, 25 mg administreras. Om patienten då inte svarar inom ytterligare 15 till 30 minuter, bör andra terapeutiska åtgärder övervägas. Den totala dosen inom 4 timmar bör inte överstiga 0,5 mg.
Obs: parenterala läkemedel ska inspekteras visuellt för partiklar och missfärgning före administrering, när lösning och behållare tillåter.
hur levereras terbutalin
Terbutalinsulfatinjektion, USP, 1 mg/mL, levereras i en volym av 1 mL i en 2 mL bärnstensfärgad glasflaska. Varje injektionsflaska innehåller 1 mg Terbutalinsulfat per 1 mL lösning; 0,25 mL lösning ger den vanliga kliniska dosen på 0,25 mg.
NDC 0143-9375-10 kartong med 10 injektionsflaskor.
Förvara på 20 till 25 till C (68 till 77 till f) .
skydda mot ljus genom att förvara injektionsflaskorna i originalkartongen tills de dispenseras.
använd inte om lösningen är missfärgad.
kassera oanvänd portion efter engångsbruk.
Tillverkad av:
HIKMA FARMAC (PORTUGAL), S. A..
Estrada do Rio da m, n 8, 8A e 8B-Ferven,
2705-906 Terrugem SNT,
PORTUGAL
distribueras av:
Hikma Pharmaceuticals USA Inc.
Eatontown, NJ 07724 USA
Novaplus är ett registrerat varumärke som tillhör Vizient, Inc.
Reviderad: Oktober 2020
PIN552-NOV/2
HUVUDDISPLAYPANEL
NDC 0143-9375-01 Rx
terbutalin
sulfat
injektion, USP
1 mg/mL
för subkutan
Använd endast

huvuddisplaypanel
NDC 0143-9375-10 RX
terbutalin
sulfat
injektion, USP
1 mg/ml
för subkutan
Använd endast
10 x 1 ml injektionsflaskor med engångsdos
steril, icke-pyrogen, vattenhaltig
lösning för subkutan injektion.
Använd inte om lösningen är missfärgad.
OBS: vanlig engångsdos är en fjärdedel
av injektionsflaskans innehåll. SEE PRESCRIBING
INFORMATION.
SERIALIZATION IMAGE
| Terbutaline SULFATE Terbutaline sulfate injection |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
Labeler – Hikma Pharmaceuticals USA Inc. (001230762)
Registrant – HIKMA Pharmaceutica (PORTUGAL), S. A. (452742943)
mer om terbutalin
- biverkningar
- under graviditet eller amning
- doseringsinformation
- Drogbilder
- läkemedelsinteraktioner
- jämför alternativ
- prissättning& kuponger
- på engelska
- 11 recensioner
- läkemedelsklass: adrenerga bronkodilatorer
- FDA-varningar (1)
konsumentresurser
- patientinformation
- terbutalin (avancerad läsning)
- terbutalin subkutan (avancerad läsning)
professionella resurser
- förskrivningsinformation
- terbutalin (professionell patientrådgivning)
- terbutalin tabletter (FDA)
relaterade behandlingsguider
- för tidigt arbete
- allergisk astma
- astma, underhåll
- astma, akut
medicinsk ansvarsfriskrivning