het Concept van Open valentie (“valentie”)
de valentie (of valentie) van een element is een maat voor het combineren van kracht met andere atomen wanneer het chemische verbindingen of moleculen vormt. Het concept van valentie werd ontwikkeld in de laatste helft van de 19e eeuw en was succesvol in het verklaren van de moleculaire structuur van veel organische verbindingen. De zoektocht naar de onderliggende oorzaken van valentie leidde tot de moderne theorieën van chemische binding, waaronder Lewis structures (1916), valence bond theory (1927), moleculaire orbitalen (1928), valence shell electron pair repulsion theory (1958) en alle geavanceerde methoden van kwantumchemie.
het gecombineerde vermogen of de affiniteit van een atoom van een element werd bepaald door het aantal waterstofatomen waarmee het werd gecombineerd. In methaan heeft koolstof een valentie van 4; in ammoniak heeft stikstof een valentie van 3; in water heeft zuurstof een valentie van twee; en in waterstofchloride heeft chloor een valentie van 1. Chloor, omdat het een valentie van één heeft, kan waterstof vervangen worden, dus fosfor heeft een valentie van 5 in fosforpentachloride, PCl5. Valentiediagrammen van een verbinding vertegenwoordigen de connectiviteit van de elementen, lijnen tussen twee elementen, soms bindingen genoemd, representeerden een verzadigde valentie voor elk element. Voorbeelden zijn:-
| Compound | H2 | CH4 | C3H8 | C2H2 | NH3 | NaCN | H2S | H2SO4 | Cl2O7 |
| Diagram |  |
 |
 |
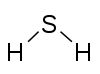 |
 |
 |
|||
| Valencies | Hydrogen 1 | Carbon 4 Hydrogen 1 |
Carbon 4 Hydrogen 1 |
Carbon 4 Hydrogen 1 |
Nitrogen 3 Hydrogen 1 |
Sodium 1 Carbon 4 Nitrogen 3 |
Sulfur 2 Hydrogen 1 |
Sulfur 6 Oxygen 2 Hydrogen 1 |
Chlorine 7 Oxygen 2 |
valentie beschrijft alleen connectiviteit, Het beschrijft niet de geometrie van moleculaire verbindingen, of wat nu bekend staat als ionverbindingen of gigantische covalente structuren. De lijn tussen atomen vertegenwoordigt geen paar elektronen zoals in Lewis diagrammen.
Further Reading
Khan Academy
Valence Electrons
Cliffs Notes
Valence Electrons
Contributors
- Wikipedia