Vivo patofysiologi
insulinsyntes och utsöndring
Insulin är ett litet protein med en molekylvikt på cirka 6000 Dalton. Den består av två kedjor som hålls samman av disulfidbindningar. Figuren till höger visar en molekylär modell av bovint insulin, med A-kedjan färgad blå och den större B-kedjan grön. Du kan få en bättre uppskattning för insulinets struktur genom att själv manipulera en sådan modell.
aminosyrasekvensen är mycket bevarad bland ryggradsdjur, och insulin från ett däggdjur är nästan säkert biologiskt aktivt i ett annat. Till och med idag behandlas många diabetespatienter med insulin extraherat från grispancreas.
biosyntes av Insulin
Insulin syntetiseras i signifikanta mängder endast i betaceller i bukspottkörteln. Insulin mRNA översätts som en enda kedjeprekursor som kallas preproinsulin, och avlägsnande av dess signalpeptid under insättning i endoplasmatisk retikulum genererar proinsulin.
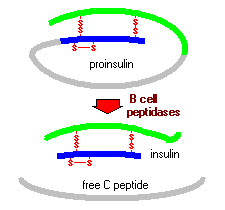 Proinsulin består av tre domäner: en amino-terminal B-kedja, en karboxi-terminal A-kedja och en anslutande peptid i mitten känd som C-peptiden. Inom endoplasmatisk retikulum exponeras proinsulin för flera specifika endopeptidaser som exciserar C-peptiden och därigenom genererar den mogna formen av insulin. Insulin och fri C-peptid förpackas i Golgi i sekretoriska granuler som ackumuleras i cytoplasman.
Proinsulin består av tre domäner: en amino-terminal B-kedja, en karboxi-terminal A-kedja och en anslutande peptid i mitten känd som C-peptiden. Inom endoplasmatisk retikulum exponeras proinsulin för flera specifika endopeptidaser som exciserar C-peptiden och därigenom genererar den mogna formen av insulin. Insulin och fri C-peptid förpackas i Golgi i sekretoriska granuler som ackumuleras i cytoplasman.
När betacellen stimuleras på lämpligt sätt utsöndras insulin från cellen genom exocytos och diffunderar i kapillärblod. C-peptid utsöndras också i blod, men har ingen känd biologisk aktivitet.
kontroll av insulinsekretion
Insulin utsöndras främst som svar på förhöjda blodkoncentrationer av glukos. Detta är vettigt eftersom insulin är ”ansvarig” för att underlätta glukosinträde i celler. Vissa neurala stimuli (t. ex. och ökade blodkoncentrationer av andra bränslemolekyler, inklusive aminosyror och fettsyror, främjar också insulinsekretion.
vår förståelse av mekanismerna bakom insulinsekretion förblir något fragmentarisk. Ändå har vissa funktioner i denna process tydligt och upprepade gånger visats, vilket ger följande modell:
- glukos transporteras in i betacellen genom underlättad diffusion genom en glukostransportör; förhöjda koncentrationer av glukos i extracellulär vätska leder till förhöjda koncentrationer av glukos i betacellen.
- förhöjda koncentrationer av glukos i betacellen leder slutligen till membrandepolarisering och en tillströmning av extracellulärt kalcium. Den resulterande ökningen av intracellulärt kalcium anses vara en av de primära utlösarna för exocytos av insulininnehållande sekretoriska granuler. Mekanismerna genom vilka förhöjda glukosnivåer i betacellen orsakar depolarisering är inte tydligt fastställda, men verkar bero på metabolism av glukos och andra bränslemolekyler i cellen, kanske avkänd som en förändring av ATP:ADP-förhållande och omvandlas till förändringar i membranledningsförmåga.
- ökade nivåer av glukos i betaceller verkar också aktivera kalciumoberoende vägar som deltar i insulinsekretion.
 stimulering av insulinfrisättning observeras lätt hos hela djur eller människor. Den normala fastande blodglukoskoncentrationen hos människor och de flesta däggdjur är 80 till 90 mg per 100 ml, associerad med mycket låga nivåer av insulinsekretion.
stimulering av insulinfrisättning observeras lätt hos hela djur eller människor. Den normala fastande blodglukoskoncentrationen hos människor och de flesta däggdjur är 80 till 90 mg per 100 ml, associerad med mycket låga nivåer av insulinsekretion.
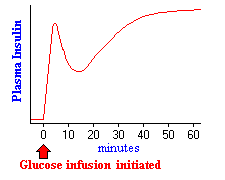
figuren till höger visar effekterna på insulinsekretion när tillräckligt med glukos infunderas för att upprätthålla blodnivåerna två till tre gånger fastningsnivån i en timme. Nästan omedelbart efter att infusionen börjar ökar plasmanivåerna av insulin dramatiskt. Denna initiala ökning beror på utsöndring av förformat insulin, vilket snart är avsevärt utarmat. Den sekundära ökningen av insulin återspeglar den betydande mängd nysyntetiserat insulin som frisätts omedelbart. Det är uppenbart att förhöjd glukos inte bara simulerar insulinsekretion utan också transkription av insulingenen och översättning av dess mRNA.
avancerade och kompletterande ämnen
- strukturen av Insulin