Nommer les Alcools
- Trouvez la chaîne la plus longue contenant le groupe hydroxy (OH). S’il y a une chaîne avec plus de carbones que celle contenant le groupe OH, elle sera nommée en tant que subsitutant.
- Placez le OH sur le nombre le plus bas possible pour la chaîne. À l’exception des groupes carbonyles tels que les cétones et les aldéhydes, les groupes alcool ou hydroxy ont la priorité pour la dénomination.
- Lors de la désignation d’une structure cyclique, le -OH est supposé être sur le premier carbone à moins que le groupe carbonyle ne soit présent, auquel cas le dernier aura priorité sur le premier carbone.
- Lorsque plusieurs groupes -OH sont sur la structure cyclique, numéroter les carbones sur lesquels résident les groupes -OH.
- Retirez le e final de la chaîne alcane mère et ajoutez -ol. Lorsque plusieurs alcools sont présents, utilisez di, tri, et.c avant la lo, après le nom du parent. ex. 2,3-hexandiol. Si un groupe carbonyle est présent, le groupe -OH est nommé avec le préfixe « hydroxy », le groupe carbonyle étant attaché au nom de la chaîne mère de sorte qu’il se termine par -al ou -one.
Exemples
Éthane:CH3CH3—–>Éthanol:  (l’alcool présent dans la bière, le vin et les autres sprits consommés)
(l’alcool présent dans la bière, le vin et les autres sprits consommés)
Alcool secondaire: 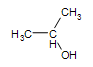 2-propanol
2-propanol
Autres groupes fonctionnels sur un alcool: 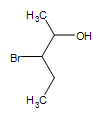 3-bromo-2-pentanol
3-bromo-2-pentanol
Alcool cyclique (deux groupes-OH): 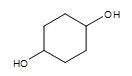 cyclohexan-1,4-diol
cyclohexan-1,4-diol
Autre groupe fonctionnel sur la structure cyclique:  3-hexèneol (l’alcène est en gras et indiqué en numérotant le carbone le plus proche de l’alcool)
3-hexèneol (l’alcène est en gras et indiqué en numérotant le carbone le plus proche de l’alcool)
Un alcool complexe:  4-éthyl-3hexanol (la chaîne mère est en rouge et le substituant est en bleu)
4-éthyl-3hexanol (la chaîne mère est en rouge et le substituant est en bleu)
Dans le système de nomenclature de l’UICPA, les groupes fonctionnels sont normalement désignés de deux manières. La présence de la fonction peut être indiquée par un suffixe caractéristique et un numéro de localisation. Ceci est courant pour les liaisons doubles et triples carbone-carbone qui ont les suffixes respectifs – ene et -yne. Les halogènes, en revanche, n’ont pas de suffixe et sont nommés comme substituants, par exemple: (CH3) 2C = CHCHClCH3 est le 4-chloro-2-méthyl-2-pentène.
Les alcools sont généralement nommés par la première procédure et sont désignés par un suffixe -ol, comme dans l’éthanol, CH3CH2OH (notez qu’un numéro de localisation n’est pas nécessaire sur une chaîne à deux carbones). Sur les chaînes plus longues, l’emplacement du groupe hydroxyle détermine la numérotation des chaînes. Par exemple : (CH3)2C = CHCH(OH) CH3 est le 4-méthyl-3-pentène-2-ol. D’autres exemples de nomenclature IUPAC sont présentés ci-dessous, ainsi que les noms communs souvent utilisés pour certains des composés les plus simples. Pour les alcools mono-fonctionnels, ce système commun consiste à nommer le groupe alkyle suivi du mot alcool. Les alcools peuvent également être classés comme primaires, 1º, secondaires, 2º et tertiaires, 3º, de la même manière que les halogénures d’alkyle. Cette terminologie fait référence à la substitution alkyle de l’atome de carbone portant le groupe hydroxyle (coloré en bleu sur l’illustration).
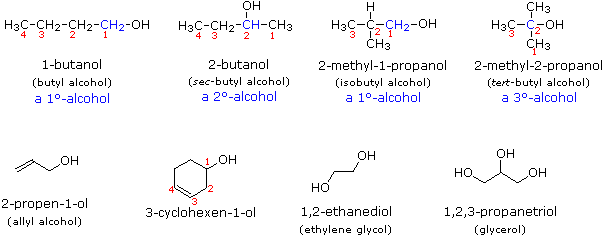
De nombreux groupes fonctionnels ont un désignateur de suffixe caractéristique, et un seul de ces suffixes (autre que « -e » et « -yne ») peut être utilisé dans un nom. Lorsque la fonction hydroxyle est présente avec une fonction de priorité nomenclaturale plus élevée, elle doit être citée et localisée par le préfixe hydroxy et un nombre approprié. Par exemple, l’acide lactique porte le nom d’acide 2-hydroxypropanoïque IUPAC.