- Bortrifluorid Chemische Eigenschaften, Verwendung, Herstellung
- Beschreibung
- Beschreibung
- Chemische Eigenschaften
- Physikalische Eigenschaften
- Verwendet
- Verwendungen
- Verwendungen
- Herstellung
- Allgemeine Beschreibung
- Luft & Wasserreaktionen
- Reaktivitätsprofil
- Gefahr
- Gesundheitsgefahr
- Brandgefahr
- Entflammbarkeit und Explosivität
- Materialverwendung
- Mögliche Exposition
- Physiologische Wirkungen
- lagerung
- Versand
- Reinigungsmethoden
- Unverträglichkeiten
- Abfallentsorgung
- Vorsichtsmaßnahmen
- VERFÜGBARE SORTEN
Bortrifluorid Chemische Eigenschaften, Verwendung, Herstellung
Beschreibung
Bortrifluorid ist die anorganische Verbindung mit der Formel BF3. Es ist ein hochgiftiges, farbloses und nicht brennbares Gas mit einem durchdringenden und stechenden Geruch. Es löst sich schnell in Wasser und organischen Verbindungen auf, die Stickstoff oder Sauerstoff enthalten. Es kann langsam durch kaltes Wasser hydrolysiert werden, um Flusssäure abzugeben, und kann auch hydrolysieren, um weiße dichte Dämpfe in feuchter Luft zu bilden. Seine Dämpfe sind schwerer als Luft. Das Einatmen des Gases reizt die Atemwege und Verbrennungen können auftreten, wenn das Gas die Haut in hohen Konzentrationen berührt.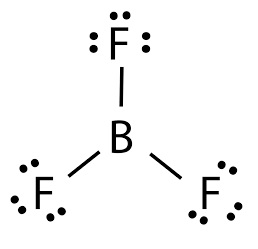
Bortrifluorid Lewis-Struktur
Bortrifluorid wird vor allem als Reagenz verwendet, typischerweise als Lewis-Säure, um so unterschiedliche Vorgänge wie Isomerisierung, Alkylierung, Polymerisation, Veresterung, Kondensation, Cyclisierung, Hydratation, Dehydratisierung, Sulfonierung, Entschwefelung, Nitrierung, Halogenierung, Oxidation und Acylierung zu katalysieren. Außerdem kann es auch als vielseitiger Baustein für andere Borverbindungen verwendet werden. 1. https://en.wikipedia.org/wiki/Boron_trifluoride
2. https://cameochemicals.noaa.gov/chemical/255
3. http://www.c-f-c.com/specgas_products/boron-trifluoride.htm
4.https://www.praxairdirect.com/Specialty-Gas-Information-Center/Pure-Gas-Specifications/Boron-Trifluoride.html
Beschreibung
Trockenes Bortrifluorid wird mit Flussstahl, Kupfer, Kupfer–Zink und Kupfer–Silizium-Legierungen sowie Nickel verwendet. Feuchtes Gas ist für die meisten metallischen Materialien ätzendund einige Kunststoffe. Daher Kel-F? und Teflon? sind die bevorzugten Dichtungsmaterialien.Quecksilberhaltige Manometer sollten nicht verwendet werden, da Bortrifluorid in Quecksilber löslich ist. Es zersetzt sich in heißem Wasser und liefert Fluorwasserstoff. Bortrifluorid istweit verbreitet als Katalysator für organische Synthesereaktionen.
Chemische Eigenschaften
Bortrifluorid ist ein nicht brennbares, farbloses Gas mit einem beißenden erstickenden Geruch. Es bildet dicke saure Dämpfe in feuchter Luft. Trockenes Bortrifluorid wird mit Flussstahl, Kupfer, Kupfer-Zink und Kupfer-Silizium-Legierungen sowie Nickel verwendet. Feuchtes Gas ist für die meisten metallischen Werkstoffe und einige Kunststoffe ätzend. Daher sind Kel-F und Teflon die bevorzugten Dichtungsmaterialien. Quecksilberhaltige Manometer sollten nicht verwendet werden, da Bortrifluorid in Quecksilber löslich ist. Es zersetzt sich in heißem Wasser und liefert Fluorwasserstoff, der als nicht verflüssigtes Druckgas versandt wird.
Physikalische Eigenschaften
Farbloses Gas; stechender erstickender Geruch; Dichte 2,975 g / L; Dämpfe in feuchter Luft; verflüssigt sich bei -101 ° C; erstarrt bei -126,8 °; Der Dampfdruck bei -128 ° C beträgt 57,8 torr; kritische Temperatur -12,2 ° C; kritischer Druck 49,15 atm; kritisches Volumen 115 cm3 / mol; löslich in Wasser mit partieller Hydrolyse; Löslichkeit in Wasser bei 0 ° C 332 g / 100g; auch löslich in Benzol, Toluol, Hexan, Chloroform und Methylenchlorid; löslich in wasserfreier konzentrierter Schwefelsäure.
Verwendet
, um geschmolzenes Magnesium und seine Legierungen vor Oxidation zu schützen; als Flussmittel zum Löten von Magnesium; als Begasungsmittel; in Ionisationskammern zum Nachweis schwacher Neutronen. Die mit Abstand größte Anwendung von Bortrifluorid findet sich in der Katalyse mit und ohne fördernde Wirkstoffe.
Verwendungen
In der Katalyse mit und ohne promotingagents; Begasungsmittel; Flussmittel für solderingmagnesium
Verwendungen
Bortrifluorid wird als Katalysator für Polymerisationen, Alkylierungen und kondensationreactions verwendet; als Gasflussmittel für internes Löten orbrazing; und als Quelle von B10-Isotop.
Herstellung
Bortrifluorid wird durch Behandeln von Borax mit Flusssäure hergestellt; oder Borsäure mit Ammoniumbifluorid. Das komplexe Zwischenprodukt wird dann mit kalter rauchender Schwefelsäure behandelt.
Allgemeine Beschreibung
Bortrifluorid ist ein farbloses Gas mit einem stechenden Geruch. Bortrifluorid ist beim Einatmen giftig. Bortrifluorid ist in Wasser löslich und wird langsam durch kaltes Wasser hydrolysiert, um Flusssäure, ein ätzendes Material, abzugeben. Seine Dämpfe sind schwerer als Luft. Längerer Kontakt der Behälter mit Feuer oder Hitze kann zu heftigen Brüchen und Explosionen führen.
Luft & Wasserreaktionen
Dämpfe in der Luft. Lösliches im Wasser und langsam hydrolysiert durch kaltes Wasser, um Flusssäure zu geben. Reagiert schneller mit heißem Wasser.
Reaktivitätsprofil
Bortrifluorid ist ein farbloses, stark reizendes, giftiges Gas. Bei Kontakt mit Wasser, Dampf oder wenn es zur Zersetzung erhitzt wird, erzeugt Bortrifluorid giftige Fluoriddämpfe. Unverträglich mit Alkylnitraten, Calciumoxid. Die Reaktion mit Alkali- oder Erdalkalimetallen (außer Magnesium) führt zu Weißglut .
Gefahr
Giftig beim Einatmen, ätzend auf Haut und Gewebe. Untere Atemwege reizend und Pneumonitis.
Gesundheitsgefahr
Bortrifluorid (und organische Komplexe wie BF3-Etherat) sind extrem ätzende Substanzen, die alle Gewebe des Körpers schädigen. Bei Kontakt mit Feuchtigkeit in der Haut und anderen Geweben reagieren diese Verbindungen unter Bildung von Flusssäure und Fluorborsäure, die schwere Verbrennungen verursachen. Bortrifluoridgas reizt Haut, Augen und Schleimhäute extrem. Das Einatmen von Bortrifluorid kann zu schweren Reizungen und Verbrennungen der Atemwege, Atembeschwerden und möglicherweise zu Atemversagen und Tod führen. Die Exposition der Augen gegenüber SONNENLICHT kann zu schweren Verbrennungen und Erblindung führen. Es wird nicht davon ausgegangen, dass diese Verbindung ausreichende Warneigenschaften aufweist. Es wurde nicht festgestellt, dass Bortrifluorid beim Menschen krebserregend ist oder Reproduktions- oder Entwicklungstoxizität zeigt. Chronische Exposition gegenüber Bortrifluoridgas kann zu Reizungen und Schäden der Atemwege führen.
Brandgefahr
Beim Erhitzen bis zur Zersetzung oder bei Kontakt mit Wasser oder Dampf erzeugt Bortrifluorid giftige und ätzende Dämpfe fluorhaltiger Verbindungen. Zersetzt sich beim Erhitzen oder bei Kontakt mit feuchter Luft und bildet giftige und ätzende Dämpfe von Borsäure und Flusssäure. Reagiert mit Alkalien und Dämpfen in feuchter Luft und erzeugt Partikel, die die Sicht beeinträchtigen. Reagiert mit Alkalimetallen, Erdalkalimetallen (außer Magnesium), Alkylnitraten und Calciumoxid. Bortrifluorid hydrolysiert in feuchter Luft unter Bildung von Borsäure, Flusssäure und Fluoroborsäure.
Entflammbarkeit und Explosivität
Bortrifluoridgas ist nicht brennbar. Wasser sollte nicht zum Löschen verwendet werdenFeuer, in dem Bortrifluorid vorhanden ist. Trockenes chemisches Pulver sollte für verwendet werdenbrände mit organischen Komplexen von Bortrifluorid.
Materialverwendung
Trockenes Bortrifluorid reagiert nicht mit den üblichen Baumetallen, aber wenn Feuchtigkeit vorhanden ist, können die gebildeten sauren Hydrate (BF3 · H2Ound BF3 · 2H2O) viele gängige Metalle schnell korrodieren. Folglich müssen Leitungen, Druckregler und Ventile im Bortrifluorid-Betrieb zwischen den Nutzungszeiten gut vor dem Eintritt feuchter Luft geschützt sein. Gusseisen darf nicht verwendet werden, da aktive Fluoride seine Struktur angreifen. Wenn Stahlrohre für Borontrifluorid verwendet werden, müssen geschmiedete Stahlfittings anstelle von Gussfittings verwendet werden. Edelstahl, Monel, Nickel und Hastelloy C sind gute Materialien der Konstruktion.
Unter den für Dichtungen geeigneten Materialien sindteflon, Kel F und andere geeignete Fluorkohlenstoffoder Fluorchlorkohlenstoffkunststoffe. Die meisten Kunststoffe werden im Bortrifluoridservice versprödet. Die Verwendung von Polyvinylchlorid sollte seinvermeidet.
Mögliche Exposition
Bortrifluorid ist eine hochreaktive Chemikalie, die hauptsächlich als Katalysator in chemischen synthesis.It wird als Gas gespeichert und transportiert, kann aber mit einer Vielzahl von Materialien reagiert werden, um sowohl flüssige als auch feste Verbindungen zu bilden. Die Magnesiumindustrie nutzt die feuerhemmenden und antioxidativen Eigenschaften von Bortrifluoridin Gehäuse und Wärmebehandlung. Nukleare Anwendungen von Borontrifluorid umfassen Neutronendetektorinstrumente; bor-10anreicherung und die Herstellung von neutroabsorbierenden Salzen Formolten-Salz-Brüterreaktoren.
Physiologische Wirkungen
Boron trifluoride irritates the nose, mucousmembranes, and other parts of the respiratorysystem. Konzentrationen so niedrig wie ich ppm in aircan durch den Geruchssinn erkannt werden und areradily sichtbar.
ACGIH empfiehlt eine Grenzwertgrenze (TLV-C) von 1 ppm (2,8 mg/m3) für Bortrifluorid. Der TLV-C ist die Konzentration, die während eines Teils der Arbeitsexposition nicht überschritten werden darf.
lagerung
Alle Arbeiten mit Bortrifluorid sollten in einer Dunstabzugshaube durchgeführt werden, um eine Exposition durch Einatmen zu vermeiden, und Spritzschutzbrillen und undurchlässige Handschuhe sollten getragen werden, um Augen- und Hautkontakt zu vermeiden. Zylinder mit Bortrifluorid sollten seinlagern Sie an Orten, die für die Druckgasspeicherung geeignet sind, und trennen Sie sie von Alkalimetallen, Erdalkalimetallen und anderen unverträglichen Substanzen. Lösungen von Bortrifluorid solltenin dicht verschlossenen Behältern unter inerter Atmosphäre in Sekundärbehältern gelagert werden.
Versand
UN1008 Bortrifluorid, Gefahrenklasse: 2.3;Etiketten: 2.3-Giftiges Gas, 8-Ätzendes Material, Einatmungsgefährdungszone B. Die Flaschen müssen in einer sicheren aufrechten Position in einem gut belüfteten LKW transportiert werden.Schützen Sie Zylinder und Aufkleber vor körperlichem Schaden. Der Besitzer der Druckgasflasche ist die einzige entityallowed durch Bundesgesetz (49CFR) zu transportieren und zu refillthem. Es handelt sich um einen Verstoß gegen die Transportvorschriften.Druckgasflaschen ohne ausdrückliche schriftliche Genehmigung des Eigentümers nachfüllen.
Reinigungsmethoden
Die üblichen Verunreinigungen – Brom, BF5, HF und nichtflüchtige Fluoride – lassen sich leicht destillativ abtrennen. Brown und Johannesen führten BF3 in Benzonitril bei 0o, bis das letztere gesättigt war. Evakuierung auf 10-5mm entfernt dann alle Spuren von SiF4 und anderen gasförmigen Verunreinigungen. . Der Druck wird durch Zugabe von trockener Luft auf 20 mm erhöht, und der Kolben, der die BF3-Additionsverbindung enthält, wird mit heißem Wasser erwärmt. Das sich entwickelnde BF3 wird durch eine -80o-Falle (um Benzonitril zu kondensieren) in ein in flüssiger Luft gekühltes Rohr geleitet. Die Additionsverbindung mit Anisol kann ebenfalls verwendet werden. BF3 kann getrocknet werden, indem es durch H2SO4 geleitet wird, das mit Boroxid gesättigt ist. Es dämpft in feuchter Luft. GIFTIG.
Unverträglichkeiten
Bortrifluorid reagiert mit polymerisiertenungesättigten Verbindungen. Zersetzt auf kontakt withwater, feuchte luft, und andere formen von feuchtigkeit, bilden toxicand korrosiven wasserstoff fluorid, fluorborsäure, und boricacid. Reagiert heftig mit Alkali- und Erdalkalimetallen (außer Magnesium); Metalle wie Natrium-, Kalium- und Calciumoxid und mit Alkylnitraten. Greift viele Metalle in Gegenwart von Wasser an.
Abfallentsorgung
Rückgabe von nachfüllbaren Druckgasflaschen an den Lieferanten. Der Eigentümer des komprimierten Gasflaschenzylinders ist die einzige Person, die nach Bundesgesetz (49CFR) zum Transport und Nachfüllen zugelassen ist. Chemische Reaktion mit Wasserborsäure und Fluorborsäure bilden. Die Fluorborsäure wird mit Kalkstein unter Bildung von Borsäure und Calciumfluorid umgesetzt. Die Borsäure kann in ein Abwassersystem eingeleitet werden, während das Calciumfluorid abgedeckt oder deponiert werden kann. Schützen Sie Zylinder und Aufkleber vorphysischer Schaden.
Vorsichtsmaßnahmen
Expositionen gegenüber Bortrifluorid in beruflichen Arbeitsbereichen verursachen Reizwirkungen, schmerzhafte Verbrennungen, Läsionen und Sehverlust. Arbeitnehmer mit einer möglichen Exposition gegenüber Bortrifluorid sollten keine Kontaktlinsen tragen. In allen Fällen einer übermäßigen Exposition gegenüber Bortrifluorid ist eine sofortige ärztliche Behandlung erforderlich, und das Rettungspersonal sollte mit geeigneten Schutzmitteln ausgestattet sein. Berufstätige sollten Bortrifluorid nur in gut belüfteten Bereichen handhaben/ verwenden. Die Ventilschutzkappen müssen an Ort und Stelle bleiben. Arbeiter sollten die Zylinder nicht ziehen, schieben oder rollen und einen geeigneten Handwagen für die Zylinderbewegung verwenden. Druckgasflaschen dürfen ohne ausdrückliche schriftliche Genehmigung des Eigentümers nicht nachgefüllt werden. Bortrifluorid ist als extrem gefährlicher Stoff (EHS) gelistet.Der Zylinder sollte auf keinen Fall erhitzt werden, um die Entladungsrate des Produkts aus dem Zylinder zu erhöhen. Der Zylinder von Bortrifluorid sollte in einem kühlen, trockenen, gut belüfteten Bereich nicht brennbarer Konstruktion gelagert werden, weg von stark befahrenen Bereichen und Notausgängen
VERFÜGBARE SORTEN
Bortrifluorid ist für den kommerziellen und industriellen Einsatz in technischen Qualitäten mit den gleichen Komponentenanteilen von einem Hersteller zum anderen erhältlich.
Bortrifluorid ist auch in erhältlichhochreine Sorten für den Einsatz in der Elektronikindustrie. Die Richtlinien zur Gasreinheit wurden von der SemiconductorEquipment and Materials International entwickelt und veröffentlicht und sind im Buch der SEMI-Standards, GasesVolume, zu finden.