begreppet öppen Valens (”Valens”)
Valens (eller Valens) för ett element är ett mått på dess kombinationskraft med andra atomer när det bildar kemiska föreningar eller molekyler. Begreppet Valens utvecklades under den sista hälften av 19-talet och lyckades förklara molekylstrukturen hos många organiska föreningar. Sökandet efter de bakomliggande orsakerna till Valens leder till moderna teorier om kemisk bindning, inklusive Lewis structures (1916), valence bond theory (1927), molecular orbitals (1928), valence shell electron pair repulsion theory (1958) och alla avancerade metoder för kvantkemi.
den kombinerade kraften eller affiniteten hos en atom av ett element bestämdes av antalet väteatomer som den kombinerade med. I metan har KOL en valens av 4; i ammoniak har kväve en valens av 3; i vatten har syre en valens av två; och i väteklorid har klor en valens av 1. Klor, eftersom det har en valens av en, kan ersättas med väte, så fosfor har en valens av 5 i fosforpentaklorid, PCl5. Valensdiagram för en förening representerar elementens anslutning, linjer mellan två element, ibland kallade bindningar, representerade en mättad Valens för varje element. Exempel är:-
| Compound | H2 | CH4 | C3H8 | C2H2 | NH3 | NaCN | H2S | H2SO4 | Cl2O7 |
| Diagram |  |
 |
 |
 |
 |
 |
|||
| Valencies | Hydrogen 1 | Carbon 4 Hydrogen 1 |
Carbon 4 Hydrogen 1 |
Carbon 4 Hydrogen 1 |
Nitrogen 3 Hydrogen 1 |
Sodium 1 Carbon 4 Nitrogen 3 |
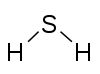
Sulfur 2 Hydrogen 1 |
Sulfur 6 Oxygen 2 Hydrogen 1 |
Chlorine 7 Oxygen 2 |
Valens beskriver endast anslutning, det beskriver inte geometrin hos molekylära föreningar, eller vad som nu är känt för att vara joniska föreningar eller jätte kovalenta strukturer. Linjen mellan atomer representerar inte ett par elektroner som det gör i Lewis-diagram.
Further Reading
Khan Academy
Valence Electrons
Cliffs Notes
Valence Electrons
Contributors
- Wikipedia