nume Generic: terbutalina sulfat
forma de dozare: injecție, soluție
Medical revizuite de Drugs.com. Ultima actualizare la 1 septembrie 2020.
- Prezentare generală
- efecte secundare
- dozare
- profesional
- interacțiuni
- mai mult
o soluție apoasă sterilă pentru injecție subcutanată
numai Rx
atenție: TOCOLIZA prelungită
sulfatul de terbutalină nu a fost aprobat și nu trebuie utilizat pentru tocoliza prelungită (peste 48-72 ore). În special, sulfatul de terbutalină nu trebuie utilizat pentru întreținerea tocolizei în ambulatoriu sau la domiciliu. Au fost raportate reacții adverse grave, inclusiv deces, după administrarea sulfatului de terbutalină la femeile gravide. La mamă, aceste reacții adverse includ creșterea frecvenței cardiace, hiperglicemie tranzitorie, hipokaliemie, aritmii cardiace, edem pulmonar și ischemie miocardică. Creșterea frecvenței cardiace fetale și hipoglicemia neonatală pot apărea ca urmare a administrării materne (vezi contraindicații: tocoliză prelungită).
- terbutalină descriere
- terbutalină – Farmacologie Clinică
- preclinice
- farmacocinetica
- indicații și utilizare pentru terbutalină
- contraindicații
- avertismente
- deteriorarea astmului
- utilizarea agenților antiinflamatori
- efecte cardiovasculare
- convulsii
- Precauții
- General
- interacțiuni medicamentoase
- carcinogeneză, mutageneză, afectarea fertilității
- sarcina-efecte teratogene
- utilizarea în travaliu și naștere
- mamele care alăptează
- utilizare pediatrică
- utilizare geriatrică
- reacții Adverse
- supradozaj
- dozare și administrare de terbutalină
- cum se administrează terbutalina
- panoul principal de afișare
- Panou principal de afișare
- SERIALIZATION IMAGE
- mai multe despre terbutalină
- resurse pentru consumatori
- resurse profesionale
- ghiduri de tratament conexe
terbutalină descriere
sulfat de terbutalină, USP, ingredientul activ al injecției cu sulfat de terbutalină, USP, este un bronhodilatator agonist beta‑adrenergic disponibil sub formă de soluție apoasă sterilă, nepirogenă, în flacoane, pentru administrare subcutanată. Fiecare mililitru de soluție conține 1 mg de sulfat de terbutalină, USP (0,82 mg de bază liberă), clorură de sodiu pentru izotonicitate, 0,055% edetat disodic dihidrat ca agent stabilizator și acid clorhidric pentru ajustarea la un pH țintă de 4. Sulfatul de terbutalină este sulfatul de alcool (inqu)-a–3,5-dihidroxibenzyi (2:1) (sare). Formula moleculară este (C12H19N03)2•H2SO4 și formula structurală este:
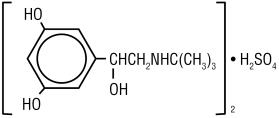
sulfat de terbutalină, USP este o pulbere cristalină albă până la gri-albă. Este inodor sau are un miros slab de acid acetic. Este solubil în apă și în acid clorhidric 0,1 N, ușor solubil în metanol și insolubil în cloroform. Greutatea sa moleculară este de 548,65.
terbutalină – Farmacologie Clinică
injecția cu sulfat de terbutalină este un agonist al receptorilor beta-adrenergici. Studiile farmacologice in vitro și in vivo au demonstrat că terbutalina exercită un efect preferențial asupra receptorilor beta2‑adrenergici. Deși se recunoaște că receptorii beta2-adrenergici sunt receptorii predominanți în mușchiul neted bronșic, datele indică faptul că există o populație de receptori beta2 în inima umană, existând într-o concentrație cuprinsă între 10% și 50%. Funcția exactă a acestor receptori nu a fost stabilită (vezi avertismente). Studiile clinice controlate la pacienții cărora li s-a administrat terbutalină subcutanat nu au evidențiat un efect beta2-adrenergic preferențial.
efectele farmacologice ale agoniștilor beta-adrenergici, inclusiv terbutalina, sunt cel puțin parțial atribuite stimulării adenil ciclazei intracelulare prin intermediul receptorilor beta-adrenergici, enzima care catalizează conversia adenozin trifosfatului (ATP) în 3′,5′-adenozin monofosfat ciclic (cAMP). Nivelurile crescute de cAMP sunt asociate cu relaxarea mușchiului neted bronșic și inhibarea eliberării mediatorilor de hipersensibilitate imediată din celule, în special din celulele mastocite.
studiile clinice controlate au arătat că injecția cu sulfat de terbutalină ameliorează bronhospasmul în boala pulmonară obstructivă acută și cronică prin creșterea semnificativă a debitelor pulmonare (de exemplu, o creștere de 15% sau mai mult în FEV1). După administrarea subcutanată de 0,25 mg de injecție cu sulfat de terbutalină, o modificare măsurabilă a debitului expirator apare de obicei în 5 minute, iar o creștere semnificativă clinic a FEV1 are loc în 15 minute. Efectul maxim apare de obicei în decurs de 30 până la 60 de minute, iar activitatea bronhodilatatoare semnificativă clinic poate continua timp de 1, 5 până la 4 ore. Durata îmbunătățirii semnificative clinic este comparabilă cu cea observată la dozele de equimiligram de epinefrină.
preclinice
studiile la animale de laborator (minipiguri, rozătoare și câini) au demonstrat apariția aritmiilor cardiace și a morții subite (cu dovezi histologice de necroză miocardică) atunci când beta-agoniștii și metilxantinele sunt administrate concomitent. Semnificația clinică a acestor constatări nu este cunoscută.
farmacocinetica
administrarea subcutanată a 0, 5 mg de sulfat de terbutalină la 17 subiecți sănătoși, adulți, de sex masculin a determinat o concentrație plasmatică maximă medie (DS) de terbutalină de 9, 6 (3, 6) ng / mL, observată la un interval median (interval) de 0, 5 (0, 08 până la 1, 0) ore după administrare. Valorile medii ale ASC (DS) (0 până la 48) și ale clearance-ului total au fost de 29, 4 (14, 2) ore•ng/mL și, respectiv, 311 (112) mL/min. Timpul de înjumătățire plasmatică prin eliminare a fost determinat la 9 din cei 17 subiecți și a avut o medie (DS) de 5, 7 (2, 0) ore.
după administrarea subcutanată a 0, 25 mg sulfat de terbutalină la doi subiecți de sex masculin, s-au observat concentrații serice maxime de terbutalină de 5, 2 și 5, 3 ng/mL la aproximativ 20 de minute după administrare.
timpul de înjumătățire prin eliminare al medicamentului la 10 din 14 pacienți a fost de aproximativ 2,9 ore după administrarea subcutanată, dar la ceilalți 4 pacienți s-au găsit timpi de înjumătățire prin eliminare mai mari (între 6 și 14 ore). Aproximativ 90% din medicament a fost excretat în urină la 96 de ore după administrarea subcutanată, aproximativ 60% din acesta fiind medicament nemodificat. Se pare că sulfatul conjugat este un metabolit major al terbutalinei, iar excreția urinară este calea principală de eliminare.
indicații și utilizare pentru terbutalină
injecție cu sulfat de terbutalină, USP este indicat pentru prevenirea și inversarea bronhospasmului la pacienții cu vârsta de 12 ani și peste cu astm bronșic și bronhospasm reversibil asociat cu bronșită și emfizem.
contraindicații
1. Tocoliza prelungită
sulfatul de terbutalină nu a fost aprobat și nu trebuie utilizat pentru tocoliza prelungită (peste 48-72 ore). În special, sulfatul de terbutalină nu trebuie utilizat pentru tocoliza de întreținere în ambulatoriu sau la domiciliu (vezi avertismentul din cutie: Tocoliza prelungită).
2. Hipersensibilitate
injectarea de sulfat de terbutalină este contraindicată la pacienții cunoscuți ca fiind hipersensibili la aminele simpatomimetice sau la orice componentă a acestui medicament.
avertismente
deteriorarea astmului
astmul se poate deteriora acut pe o perioadă de ore sau cronic pe parcursul mai multor zile sau mai mult. Dacă pacientul are nevoie de mai multe doze de sulfat de terbutalină decât de obicei, acesta poate fi un marker al destabilizării astmului și necesită reevaluarea pacientului și a regimului de tratament, acordând o atenție deosebită posibilei necesități de tratament antiinflamator, de exemplu, corticosteroizi.
utilizarea agenților antiinflamatori
utilizarea bronhodilatatoarelor agoniste beta-adrenergice în monoterapie poate să nu fie adecvată pentru controlul astmului la mulți pacienți. Trebuie luată în considerare din timp adăugarea de agenți antiinflamatori, de exemplu corticosteroizi.
efecte cardiovasculare
sulfatul de terbutalină, ca toți ceilalți agoniști beta-adrenergici, poate produce un efect cardiovascular semnificativ clinic la unii pacienți, măsurat prin frecvența pulsului, tensiunea arterială și / sau simptome. Deși astfel de efecte sunt mai puțin frecvente după administrarea de sulfat de terbutalină la dozele recomandate, dacă apar, este posibil ca medicamentul să fie întrerupt. În plus, s‑a raportat că beta-agoniștii produc modificări ale electrocardiogramei (ECG), cum ar fi aplatizarea undei T, prelungirea intervalului QTc și depresia segmentului ST. Semnificația clinică a acestor constatări nu este cunoscută. Prin urmare, sulfatul de terbutalină, la fel ca toate aminele simpatomimetice, trebuie utilizat cu precauție la pacienții cu tulburări cardiovasculare, în special insuficiență coronariană, aritmii cardiace și hipertensiune arterială.
convulsii
au existat raportări rare de convulsii la pacienții cărora li s-a administrat terbutalină; convulsiile nu au reapărut la acești pacienți după întreruperea tratamentului.
Precauții
General
terbutalina, ca și în cazul tuturor aminelor simpatomimetice, trebuie utilizată cu precauție la pacienții cu tulburări cardiovasculare, inclusiv boală cardiacă ischemică, hipertensiune arterială și aritmii cardiace; la pacienții cu hipertiroidism sau diabet zaharat; și la pacienții care răspund neobișnuit la aminele simpatomimetice sau care prezintă tulburări convulsive. S-au observat modificări semnificative ale tensiunii arteriale sistolice și diastolice și este de așteptat să apară la unii pacienți după utilizarea oricărui bronhodilatator beta-adrenergic.
au fost raportate reacții de hipersensibilitate imediată și exacerbări ale bronhospasmului după administrarea terbutalinei.medicamentele agoniste Beta-adrenergice pot produce hipokaliemie semnificativă la unii pacienți, posibil prin manevră intracelulară, care are potențialul de a produce efecte cardiovasculare adverse. Scăderea este de obicei tranzitorie, fără a necesita suplimente.
s-a raportat că dozele mari de terbutalină intravenoasă agravează diabetul zaharat preexistent și cetoacidoza.
interacțiuni medicamentoase
utilizarea concomitentă a injecției cu sulfat de terbutalină cu alți agenți simpatomimetici nu este recomandată, deoarece efectul combinat asupra sistemului cardiovascular poate fi dăunător pentru pacient.
inhibitori de monoaminooxidază sau antidepresive triciclice:terbutalina trebuie administrată cu precauție extremă pacienților tratați cu inhibitori de monoaminooxidază sau antidepresive triciclice sau în decurs de 2 săptămâni de la întreruperea acestor medicamente, deoarece acțiunea terbutalinei asupra sistemului vascular poate fi potențată.
Beta-blocante: Agenții de blocare a receptorilor Beta-adrenergici nu numai că blochează efectul pulmonar al beta-agoniștilor, cum ar fi injecția cu sulfat de terbutalină, dar pot produce bronhospasm sever la pacienții astmatici. Prin urmare, pacienții cu astm bronșic nu trebuie tratați în mod normal cu beta‑blocante. Cu toate acestea, în anumite circumstanțe, de exemplu, ca profilaxie după infarctul miocardic, nu pot exista alternative acceptabile la utilizarea blocantelor beta-adrenergice la pacienții cu astm. În acest cadru, beta-blocantele cardioselective ar putea fi luate în considerare, deși trebuie administrate cu precauție.
diuretice: modificările ECG și / sau hipokaliemia care pot rezulta din administrarea diureticelor care nu economisesc potasiu (cum ar fi diureticele cu buclă sau tiazidice) pot fi agravate acut de beta-agoniști, în special atunci când doza recomandată de beta-agonist este depășită. Deși semnificația clinică a acestor efecte nu este cunoscută, se recomandă prudență în administrarea concomitentă a beta-agoniștilor cu diuretice care nu economisesc potasiul.
carcinogeneză, mutageneză, afectarea fertilității
într-un studiu cu durata de 2 ani la șobolani Sprague-Dawley, sulfatul de terbutalină a determinat o creștere semnificativă și dependentă de doză a incidenței leiomioamelor benigne ale mezovariumului la doze dietetice de 50 mg/kg și peste (de aproximativ 810 ori doza zilnică maximă recomandată subcutanată (S.C.) pentru adulți, în mg / m2). Într-un studiu cu durata de 21 de luni la șoareci CD-1, sulfatul de terbutalină nu a evidențiat tumorigenitate la doze dietetice de până la 200 mg/kg (de aproximativ 1600 ori doza zilnică maximă recomandată pentru adulți în mg/m2). Potențialul de mutagenitate al sulfatului de terbutalină nu a fost determinat.
studiile asupra funcției de reproducere la șobolani care utilizează sulfat de terbutalină nu au demonstrat afectarea fertilității la doze orale de până la 50 mg/kg (de aproximativ 810 ori doza zilnică maximă recomandată pentru adulți în mg / m2).
sarcina-efecte teratogene
sarcina categoria C
nu există studii adecvate și bine controlate ale sulfatului de terbutalină la femeile gravide. Studiile publicate pe animale arată că puii de șobolan prezintă modificări ale comportamentului și dezvoltării creierului, inclusiv scăderea proliferării și diferențierii celulare atunci când barajele au fost tratate subcutanat cu terbutalină în stadiul final al sarcinii și perioadei de lactație. Expunerile la terbutalină la femelele de șobolan au fost de aproximativ 24 până la 48 de ori mai mari decât doza obișnuită la om, la adulți, de 2-4 mg/zi, în mg/m2.sulfatul de terbutalină nu a fost aprobat și nu trebuie utilizat pentru tocoliză prelungită (peste 48-72 ore). În special, sulfatul de terbutalină nu trebuie utilizat pentru întreținerea tocolizei în ambulatoriu sau la domiciliu. Au fost raportate reacții adverse grave, inclusiv deces, după administrarea sulfatului de terbutalină la femeile gravide. La mamă, aceste reacții adverse includ creșterea frecvenței cardiace, hiperglicemie tranzitorie, hipokaliemie, aritmii cardiace, edem pulmonar și ischemie miocardică. Creșterea frecvenței cardiace fetale și hipoglicemia neonatală pot apărea ca urmare a administrării materne (vezi avertismentul din cutie: tocoliză prelungită și contraindicații: tocoliză prelungită).
în studiile de dezvoltare embriofetală la animale, nu s-au observat efecte teratogene la descendenți atunci când șobolanii și iepurii gestanți au primit sulfat de terbutalină la doze orale de până la 50 mg/kg și zi, de aproximativ 810 și, respectiv, de 1600 de ori doza zilnică maximă recomandată subcutanată pentru adulți, pe bază de mg/m2.sulfatul de terbutalină trebuie utilizat în timpul sarcinii numai dacă beneficiile potențiale justifică riscul potențial pentru făt.
utilizarea în travaliu și naștere
datorită potențialului de interferență beta-agonistă cu contractilitatea uterină, utilizarea injecției cu sulfat de terbutalină pentru ameliorarea bronhospasmului în timpul travaliului trebuie limitată la acei pacienți la care beneficiile depășesc în mod clar riscul.
terbutalina traversează placenta. După administrarea unei doze unice IV de terbutalină la 22 de femei la sfârșitul sarcinii care au fost livrate prin cezariană electivă din motive clinice, s-a constatat că nivelurile de terbutalină din sângele ombilical variază între 11% și 48% din nivelurile sanguine materne.
mamele care alăptează
nu se știe dacă acest medicament este excretat în laptele uman. Prin urmare, injecția cu sulfat de terbutalină trebuie utilizată în timpul alăptării numai dacă beneficiul potențial justifică riscul posibil pentru nou-născut.
utilizare pediatrică
injecția cu sulfat de terbutalină nu este recomandată pacienților cu vârsta sub 12 ani din cauza datelor clinice insuficiente pentru a stabili siguranța și eficacitatea.
utilizare geriatrică
studiile clinice privind injecția cu sulfat de terbutalină nu au inclus un număr suficient de subiecți cu vârsta de 65 de ani și peste pentru a determina dacă răspund diferit față de subiecții mai tineri. Alte experiențe clinice raportate nu au identificat diferențe în răspunsurile dintre pacienții vârstnici și cei mai tineri. În general, selectarea dozei pentru un pacient în vârstă trebuie să fie prudentă, de obicei începând de la capătul scăzut al intervalului de dozare, reflectând frecvența mai mare a scăderii funcției hepatice, renale sau cardiace și a bolii concomitente sau a altor terapii medicamentoase.
reacții Adverse
reacțiile Adverse observate la injectarea sulfatului de terbutalină sunt similare cu cele observate frecvent la alte simpatomimetice. Toate aceste reacții sunt tranzitorii și, de obicei, nu necesită tratament.
tabelul următor compară reacțiile adverse observate la pacienții tratați cu injecție cu sulfat de terbutalină (0,25 mg și 0,5 mg), cu cele observate la pacienții tratați cu injecție cu epinefrină (0,25 mg și 0,5 mg), pe parcursul a opt studii dublu-orb încrucișate care au implicat un total de 214 pacienți.
| Incidence (%) of Adverse Reactions | |||||
| Terbutaline (%) | Epinephrine (%) | ||||
|
0.25 mg |
0.5 mg N = 205 |
0.25 mg N = 153 |
0.5 mg N = 61 |
||
| Reaction Central Nervous System |
|||||
| Tremor | 7.8 | 38.0 | 16.3 | 18.0 | |
| Nervousness | 16.9 | 30.7 | 8.5 | 31.1 | |
| Dizziness | 1.3 | 10.2 | 7.8 | 3.3 | |
| Headache | 7.8 | 8.8 | 3.3 | 9.8 | |
| Drowsiness | 11.7 | 9.8 | 14.4 | 8.2 | |
| Cardiovascular | |||||
| Palpitations | 7.8 | 22.9 | 7.8 | 29.5 | |
| Tachycardia | 1.3 | 1.5 | 2.6 | 0.0 | |
| Respiratory | |||||
| Dyspnea | 0.0 | 2.0 | 2.0 | 0.0 | |
| Chest discomfort | 1.3 | 1.5 | 2.6 | 0.0 | |
| Gastrointestinal | |||||
| Nausea/vomiting | 1.3 | 3.9 | 1.3 | 11.5 | |
| Systemic | |||||
| Weakness | 1.3 | 0.5 | 2.6 | 1.6 | |
| Flushed feeling | 0.0 | 2.4 | 1.3 | 0.0 | |
| Sweating | 0.0 | 2.4 | 0.0 | 0.0 | |
| Pain at injection site | 2.6 | 0.5 | 2.6 | 1.6 | |
notă: unii pacienți au primit mai mult de o doză de sulfat de terbutalină și epinefrină. În plus, au existat rapoarte de anxietate, crampe musculare și gură uscată (< 0,5%). Au existat raportări rare de creșteri ale enzimelor hepatice și de vasculită de hipersensibilitate în cazul administrării de terbutalină.pentru a raporta reacțiile adverse suspectate, contactați Hikma Pharmaceuticals USA Inc.. la 1-877-233-2001, sau FDA la 1-800-FDA – 1088 sau www.fda.gov/medwatch.
supradozaj
doza letală mediană sc de sulfat de terbutalină la șobolanii maturi a fost de aproximativ 165 mg/kg (de aproximativ 2700 ori doza zilnică maximă recomandată pentru adulți, în mg / m2). Doza letală mediană sc de sulfat de terbutalină la șobolanii tineri a fost de aproximativ 2000 mg/kg (de aproximativ 32000 de ori doza zilnică maximă recomandată pentru adulți, în mg/m2).
simptomele așteptate ale supradozajului sunt cele de stimulare beta-adrenergică excesivă și / sau apariția sau exagerarea oricăruia dintre simptomele enumerate la reacțiile ADVERSE, de exemplu convulsii, angină pectorală, hipertensiune arterială sau hipotensiune arterială, tahicardie cu rate de până la 200 bătăi pe minut, aritmii, nervozitate, cefalee, tremor, gură uscată, palpitații, greață, amețeli, oboseală, stare generală de rău și insomnie. De asemenea, poate apărea hipokaliemie. Nu există un antidot specific. Tratamentul constă în întreruperea injecției cu sulfat de terbutalină împreună cu terapia simptomatică adecvată. Poate fi luată în considerare utilizarea judicioasă a unui blocant beta-receptor cardioselectiv, având în vedere că un astfel de medicament poate produce bronhospasm. Nu există dovezi suficiente pentru a determina dacă dializa este benefică pentru supradozarea injecției cu sulfat de terbutalină.
dozare și administrare de terbutalină
flacoanele trebuie utilizate numai pentru administrare subcutanată și nu pentru perfuzie intravenoasă.
sterilitatea și dozarea exactă nu pot fi asigurate dacă flacoanele nu sunt utilizate în conformitate cu doza și administrarea.
A se arunca porțiunea neutilizată după administrarea la un singur pacient.
doza uzuală subcutanată de injecție cu sulfat de terbutalină este de 0,25 mg injectată în zona deltoidă laterală. Dacă nu apare o îmbunătățire clinică semnificativă în decurs de 15 până la 30 de minute, se poate administra o a doua doză de 0, 25 mg. Dacă pacientul nu răspunde în decurs de încă 15 până la 30 de minute, trebuie luate în considerare alte măsuri terapeutice. Doza totală în decurs de 4 ore nu trebuie să depășească 0,5 mg.
notă: produsele medicamentoase parenterale trebuie inspectate vizual pentru particule și decolorare înainte de administrare, ori de câte ori soluția și recipientul permit acest lucru.
cum se administrează terbutalina
injectarea sulfatului de terbutalină, USP, 1 mg / mL, este furnizată la un volum de 1 mL conținut într-un flacon de sticlă de culoare brună de 2 mL. Fiecare flacon conține 1 mg de sulfat de terbutalină per 1 mL de soluție; 0,25 mL de soluție va furniza doza clinică uzuală de 0,25 mg.
NDC 0143-9375-10 cutie cu 10 flacoane.
A se depozita la 20 la 25 la 25 la 28 la 77 la 7) .
A se proteja de lumină prin păstrarea flacoanelor în cutia originală până la eliberare.
a nu se utiliza dacă soluția este decolorată.
A se arunca porțiunea neutilizată după administrarea la un singur pacient.
fabricat de:
HIKMA farmaceutica (Portugalia), S. A..
Estrada do Rio da M, N, 8, 8a e 8b-Ferven,
2705 – 906 Terrugem SNT,
Portugalia
distribuit de:
Hikma Pharmaceuticals USA Inc.
Eatontown, NJ 07724 SUA
Novaplus este o marcă înregistrată a Vizient, Inc.
revizuit: Octombrie 2020
PIN552-NOV/2
panoul principal de afișare
NDC 0143-9375-01 numai RX
terbutalină
sulfat
injecție, USP
1 mg/mL
numai pentru administrare subcutanată

Panou principal de afișare
NDC 0143-9375-10 numai RX
terbutalină
sulfat
injecție, USP
1 mg/ml
pentru administrare subcutanată
A se utiliza numai 10 flacoane unidoză x 1 ml
soluție apoasă sterilă, nepirogenă, pentru administrare subcutanată.
A nu se utiliza dacă soluția este decolorată.notă: doza unică uzuală este de o pătrime din conținutul flaconului. SEE PRESCRIBING
INFORMATION.
SERIALIZATION IMAGE
| Terbutaline SULFATE Terbutaline sulfate injection |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
Labeler – Hikma Pharmaceuticals USA Inc. (001230762)
Registrant – HIKMA FARMACEUTICA (Portugalia), S. A. (452742943)
mai multe despre terbutalină
- efecte secundare
- în timpul sarcinii sau alăptării
- informații despre dozare
- imagini de droguri
- interacțiuni medicamentoase
- comparați Alternative
- prețuri& cupoane
- în engleză
- 11 recenzii
- clasa de droguri: bronhodilatatoare adrenergice
- alerte FDA (1)
resurse pentru consumatori
- informații pentru pacienți
- terbutalină (citire avansată)
- terbutalină subcutanată (citire avansată)
resurse profesionale
- informații de prescriere
- terbutalină (consiliere profesională pentru pacienți)
- comprimate de terbutalină (FDA)
ghiduri de tratament conexe
- travaliu prematur
- astm alergic
- astm, întreținere
- astm, acut
disclaimer medical