inleiding
overgevoeligheid voor een levensmiddel omvat elke meetbare en reproduceerbare bijwerking als gevolg van de inname van dat levensmiddel in een door normale personen getolereerde dosis. Het onderscheid wordt gemaakt tussen allergische overgevoeligheid, die reacties zijn waar een immunologisch mechanisme wordt ontdekt, en binnen deze IgE-gemedieerde en niet-IgE-gemedieerde allergie, afhankelijk van hun mechanisme. Niet-allergische overgevoeligheidsreacties zijn die waarbij het immunologisch mechanisme is uitgesloten 1.
koemelkeiwitten nemen de derde plaats in frequentie in als oorzaak van voedselallergie tijdens de kindertijd, na eieren en vissen 2. Hoewel het niet de meest voorkomende oorzaak van voedselallergie is, trekt koemelk de aandacht van de kinderarts omdat het het eerste voedsel is dat vreemd is aan zijn soort waarmee het kind in contact komt, na borstvoeding of vanaf de eerste dag van het leven wanneer dit niet mogelijk is. Ontwikkeling van sensibilisatie en koemelkeiwitallergie (cmpa) hangt af van de interactie tussen genetische aanleg en factoren van blootstelling aan koemelkeiwitten (antigeendosis, aard van het antigeen, blootstelling van de moeder tijdens de zwangerschap, overdracht van koemelkeiwitten (CMP) door de moedermelk, frequentie van toediening, enz.) 3. De gegevens die door de internationale literatuur worden verstrekt over de incidentie ervan zijn zeer uiteenlopend, als gevolg van conceptuele verschillen, diagnostische methodologie en bestudeerde leeftijden, en ze variëren tussen 0,3 en 7,5% 4. In een van de meest recente prospectieve studies die internationaal zijn gepubliceerd en die in Denemarken door Host et al zijn uitgevoerd, werd een incidentie van door IgE tot CMP gemedieerde allergie van 1,2% waargenomen in het eerste levensjaar 5. In een prospectief onderzoek dat in de regio Valencia werd uitgevoerd, werd een incidentie van 0,36% waargenomen in het eerste levensjaar 6 en in een daaropvolgende studie met een vergelijkbare methodologie in het gebied dat wordt bestreken door het ziekenhuis Sant Joan de Déu de Manresa, werd een incidentie van 0,67% waargenomen 7. Cijfers lager dan die welke onlangs zijn waargenomen bij baby ‘ s die zijn geboren in Hospital Infantil La Paz over een periode van één jaar, voor wie een incidentie van ten minste 1,9% 8 is berekend.om onze kennis over deze belangrijke voedselallergie te verbeteren, heeft het Comité voor voedselallergie van de Spaanse Vereniging voor Klinische Immunologie en pediatrische Allergologie besloten een klinische en diagnostische en monitoringstudie te starten bij zuigelingen met CMPA. Het is een multicentrisch onderzoek waaraan de pediatrische Allergiesecties van 14 ziekenhuizen deelnamen.
in dit onderzoek hebben we het over zuigelingen met CMPA. De gevallen van intolerantie voor andere koemelkproducten (bijv. lactose) of van allergische reacties op toegevoegde producten (bijv. penicilline) worden niet in aanmerking genomen.
Deze prospectieve studie heeft de volgende doelstellingen:
1. Evalueer verschillende epidemiologische factoren met betrekking tot het optreden van CMPA: anamnese van atopie, aanvangsleeftijd en type voeding.
2. Observeer hoe het wordt gepresenteerd en wat de klinische manifestaties zijn.
3. Bestudeer de waarde van de huidtesten en de bepaling van melkspecifieke serum-IgE en zijn fracties bij de diagnose, evenals de indicatie en het nut van de challenge-test bij de diagnose van onmiddellijke overgevoeligheid voor CMP bij de zuigeling.
4. Zie of er andere voedselsensibilisaties zijn (rundvlees, soja, ei en vis) en hun klinische relevantie.
5. Prospectieve studie van de natuurlijke geschiedenis van CMPA, om te zien op welke leeftijd tolerantie is vastgesteld en de mogelijke associatie met andere allergische aandoeningen (astma, rhinitis enz.) gedurende een controleperiode van 4 jaar met deze kinderen.
Dit is de eerste publicatie van dit werk en verwijst naar de eerste twee punten van de genoemde doelstellingen.
METHODEN
Onderwerpen
in totaal 409 kinderen (213 jongens en 196 meisjes), die gekomen was om de Anti-Eenheden van de Universiteit in het Algemeen Ziekenhuis van Valencia, Sant Joan de Déu van Barcelona, Miguel Servet in Zaragoza, San Joan de Déu de Manresa, Universitario Infantil La Paz, Madrid, Severo Ochoa de Leganés, Niño Jezus, Madrid, Algemene Universitario de Elche, Germans Trias i Pujol, Badalona, Algemene Igualada, Sant Joan de Déu de Martorell, Klinische Maagd van de vlakte van Murcia, Universitair ziekenhuis van Pamplona voor de eerste keer en die waren geselecteerd achtereenvolgens gedurende een periode van 3 jaar, vanwege symptomen die wijzen op onmiddellijke overgevoeligheid voor CMP (urticaria, angio-oedeem, erythemateuze uitslag, braken, diarree, rhinoconjunctivitis, bronchospasmen of anafylactische shock) in de 2 uur na de inname van koemelk.
Procedures
de volledige medische voorgeschiedenis werd geregistreerd en een volledig lichamelijk onderzoek werd uitgevoerd.
Huidtesttechniek: Huidpriktesten werden uitgevoerd bij alle patiënten met volle koemelkextract (5 mg / ml) , met geïsoleerde CMPs: α-lactalbumine (5 mg/mL), β-lactoglobuline (5 mg/mL) en caseïne (10 mg/mL) en met andere levensmiddelen: runderserum (5% g/vol), soja (10 mg/ml), heek (1 mg/ml), schol (1 mg/ml), Eiwit (2 mg / ml) om andere mogelijke geassocieerde voedselsensibilisaties te bestuderen. Histaminedihydrochloride (10 mg/ml) werd gebruikt als een positieve controle, en glycerosaline werd gebruikt als een negatieve controle. Reacties werden na 15 minuten gelezen. Een netdiameter van 3 mm groter dan die van de negatieve controle werd als positief beschouwd. Extracten van Laboratorios Leti CBF (Barcelona, Spanje) werden gebruikt.
In-vitrotest: Serummonsters van alle patiënten werden geanalyseerd op serumspecifieke IgE-antilichamen tegen melk, α-lactalbumine, β-lactoglobuline en caseïne met behulp van het Cap-systeem FEIA (Pharmacia Diagnostics, Uppsala, Zweden). De test werd als positief beschouwd wanneer een resultaat van 0,35 kU / l werd verkregen.
Challenge test: Open gecontroleerde challenge tests met koemelk werden uitgevoerd met een formule van koemelk aangepast aan de leeftijd van de patiënt. Twee vrij door de onderzoekers gekozen regimes werden gebruikt: regime een eerste dag: 2 ml, 5 ml, 10 ml; tweede dag: 25 ml, 50 ml; derde dag: 100 ml en de laatste dosis om de hoeveelheid te voltooien die gelijk is aan één normaal voer werden gegeven met tussenpozen van 60 minuten. Regime B in een enkele dag, opeenvolgende doses van 2 ml, 5 ml, 10 ml, 25 ml, 50 ml, 100 ml. werden toegediend met tussenpozen van 30 minuten.
indien een klinische reactie optrad, werd de challenge gestaakt en werd indien nodig een behandeling gegeven. De challenge werd als positief beschouwd wanneer er huid (urticaria, angio-oedeem of erythemateuze uitslag), gastro-intestinale (braken of diarree), respiratoire (rhinoconjunctivitis of bronchospasmen) of gegeneraliseerde (anafylactische shock) manifestaties waren in de 2 uur na inname van het voedsel.
de challenge test werd gecontra-indiceerd geacht in gevallen van anafylactische shock en/of glottaal oedeem en niet geïndiceerd bij patiënten die aan alle volgende criteria voldeden:
1. Urticaria en / of angio-oedeem.
2. Optreden van symptomen in de eerste 60 minuten na inname.
3. Positieve huidtesten (≥ 3mm) en specifieke IgE ≥ 3 kU/l aan om het even welke proteã nen.
4. Minder dan 3 maanden sinds de laatste klinische reactie.
indien de zuigeling nog borstvoeding kreeg, werd de provocatietest uitgesteld tot het begin van de kunstmatige lactatie.
bij patiënten die allergisch zijn voor koemelk die gevoelig is voor rundvlees (positieve huidpriktest, CAP-systeem, of beide) werd de tolerantie voor dit voedsel bestudeerd op de leeftijd waarop de introductie ervan in het dieet werd aangetoond door middel van een open gecontroleerde challenge test met gekookt rundvlees tot een totale dosis die gelijk is aan een normale maaltijd.
alle uitdagingen werden uitgevoerd op de Allergieafdeling van het ziekenhuis, waar geschikte medicatie en reanimatieapparatuur direct beschikbaar was. Geà nformeerde toestemming werd eerder verkregen van de ouders. Elke patiënt bleef gedurende 3 uur onder observatie na de laatste inname van de melk alvorens naar huis te gaan.
de patiënt werd geacht IgE-gemedieerde CMP-allergie te vertonen wanneer aan de volgende criteria werd voldaan:
1. Een duidelijke voorgeschiedenis van onmiddellijke overgevoeligheid voor CMP.
2. Positieve huidpriktest, CAP-systeem, of beide, op volle koemelk, α-lactalbumine, β-lactoglobuline of caseïne.
3. Positieve test voor koemelk.
resultaten
in totaal werden 409 kinderen (52% mannen en 48% vrouwen) in de leeftijd tussen 8 dagen en 22 maanden met een gemiddelde van 5,5 maanden in deze studie opgenomen.
allergische IgE-gemedieerde Sensibilisatie (positieve huidpriktest, CAP-systeem, of beide) voor koemelkeiwitten werd waargenomen bij 327 patiënten (80 %) en afwezigheid van sensibilisatie bij 82 patiënten (20 %). De prik test was positief voor koemelk en/of een of meer van de eiwitten bij 289 patiënten (71 %). Serum-IgE specifiek voor melk en/of één van de eiwitten was ≥ 0,35 kU / l bij 280 patiënten (68 %).
in totaal werden 286 challenge tests uitgevoerd met koemelkformule, die positief bleken bij 126 (44 %) en negatief bij 160 (56%). De challenge test werd niet geïndiceerd geacht bij 123 patiënten (30% van de steekproefgroep). De challenge test werd uitgevoerd volgens schema A bij 134 patiënten (47 %) en schema B bij 152 patiënten (53 %).
positieve reactiesymptomen op de challenge test waren cutaan (urticaria, angio-oedeem, erytheem) in 94 gevallen (75 %), spijsvertering (braken, diarree) in 43 (34%) en respiratoire symptomen bij 10 (8%), terwijl 33 patiënten (26 %) in meer dan één shock-orgaan werden aangetast. Tien patiënten vertoonden respiratoire symptomen van rhinoconjunctivitis en / of hoest en in slechts vier van de gevallen kon de reactie als ernstig worden beschouwd omdat deze in verband werd gebracht met respiratoire stridor. Twee van deze ernstige reacties traden op met regime A (3% van alle positieve challenge testen met regime A) en de andere twee met regime B (3% van alle positieve challenge testen met regime B). Er ontstonden geen gevallen van bronchospasme of anafylactische shock.
Met deze resultaten werd IgEmediated CMPA gediagnosticeerd bij 234 (57 %), CMP tolerante sensibilisatie bij 93 (23 %), niet-IgE-gemedieerde overgevoeligheid voor CMP bij 15 (4%) en bij de overige 67 (16 %) werd de bijwerking in de challenge test of allergische Sensibilisatie niet bevestigd (fig. 1).
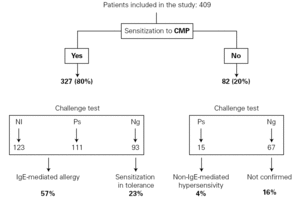
figuur 1.– Resultaat van de allergologische studie. NI: Challenge test niet geïndiceerd; Ps: positief; Ng: negatief.
patiënten met CMP-allergie
van de 409 patiënten die deelnamen aan de studie, werd bij 234 (57 %) CMP-allergie vastgesteld. De eerste reactie op koemelk vond in alle gevallen plaats in het eerste levensjaar, 95 % vóór de leeftijd van 6 maanden, met een gemiddelde leeftijd van 3,5 maanden en een bereik van 10 dagen tot 10 maanden (fig. 2).
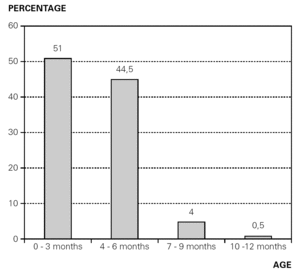
Figuur 2.– Patiënten gediagnosticeerd met CMP allergie. Procentuele verdeling in verhouding tot de leeftijd waarop de eerste reactie op CMP plaatsvond.
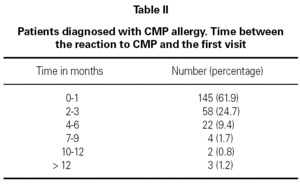
De gemiddelde leeftijd van het eerste consult voor allergologisch onderzoek was 5,4 maanden met een leeftijd variërend van 16 dagen tot 20 maanden. 93 % was aanwezig vóór de leeftijd van 9 maanden (tabel I). Er werd een gemiddelde vertraging van 2,2 maanden waargenomen tussen het verschijnen van de reactie en het eerste overleg (tabel II).

Van het totaal van die allergisch zijn voor CMP, 232 patiënten (99 %) waren borstvoeding voordat de reactie op koemelk ontstaan, tijdens een gemiddelde periode van 3,5 maanden met een range van tussen de 7 dagen en 10 maanden. Slechts twee patiënten (1 %) kregen vanaf de geboorte kunstmatige koemelkvoeding.
bij 44 % van de patiënten gaven de moeders aan aanvullend koemelkvoeding te hebben aangeboden tijdens de periode van borstvoeding (35% tijdens hun zwangerschapsverblijf in de onmiddellijke neonatale periode en 14% tijdens de periode van borstvoeding). 56 % van de moeders zei dat ze de borstvoeding tijdens de neonatale periode of later niet hadden aangevuld.
met betrekking tot het type bevalling werd 71% geboren door vaginale bevalling en 29% door keizersnede.
42 % van de patiënten met CMP-allergie heeft atopische aandoeningen (rhinitis, astma, atopische dermatitis en/of voedselallergie) gemeld bij leden van hun directe familie.
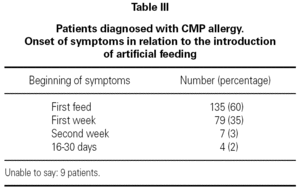
in de meeste gevallen (60 %) traden de eerste symptomen van een allergische reactie op CMP op met de eerste fles koemelkvoeding na de periode van borstvoeding en in 95% van de gevallen tijdens de eerste week na de introductie van aangepaste melkvoeding (tabel III).
klinische reactie verscheen in de meeste gevallen binnen een latentieperiode van 30 minuten na het voeden (fig. 3).
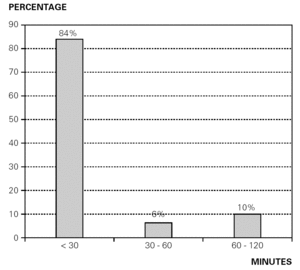
Figuur 3.– Patiënten gediagnosticeerd met CMP allergie. Procentuele verdeling vergeleken met de latentieperiode van het optreden van symptomen na toediening van CMP.
de meest voorkomende klinische manifestaties met koemelkformule waren cutaan (erytheem, urticaria, angio-oedeem), die verscheen bij 94% van de patiënten, gevolgd door spijsvertering (braken, diarree) bij 33 %, en respiratoire (hoesten, bronchospasmen, stridor) bij 8 %. Respiratoire symptomen werden in alle gevallen geassocieerd met klinische manifestaties in andere organen en slechts 4% van de patiënten vertoonde geïsoleerde klinische spijsverteringsverschijnselen. 25 % toonde afwijzing van aangepaste formule flesvoeding.
in bijna een derde van de gevallen (32%) werden klinische symptomen van anafylaxie waargenomen bij meer dan één orgaan, en slechts 12 patiënten (5 %) vertoonden ernstige reacties met bronchospasmen en respiratoire stridor. Geen enkele patiënt had een voorgeschiedenis van anafylactische shock.
21 % van de patiënten vertoonde geassocieerde atopische dermatitis, die was begonnen voordat een klinische reactie op koemelk optrad.
wat betreft sensibilisatie voor verschillende koemelkeiwitten werd 93 % gesensibiliseerd voor meer dan één eiwit (26% tot twee en 67% tot meer dan twee). 89% van de patiënten was gevoelig voor bèta-lactoglobuline, 79% voor caseïne en 79% voor Alfa-lactalbumine.
sensibilisatie voor andere voedingsmiddelen: sensibilisatie voor eieren werd waargenomen bij 30% van de patiënten met een allergie voor CMP voordat dit voedsel in het dieet werd geïntroduceerd. 42 % van de patiënten die gevoelig waren voor ei presenteerde atopische dermatitis, tegenover 15% van de patiënten die niet gevoelig waren voor ei.
sensibilisatie voor rundvlees werd waargenomen bij 29% van de onderzochte patiënten. Alle proefpersonen tolereerden gekookt rundvlees.
4 % van de patiënten met CMP-allergie vertoonde sensibilisatie voor soja. Ze verdroegen allemaal soja-formules. 3 % werd gevoelig gemaakt voor vis (heek en schol) die nog in het dieet moest worden opgenomen.
discussie
om een nauwkeurige diagnose van IgE-gemedieerde allergie te kunnen stellen, is het noodzakelijk dat er een compatibele klinische voorgeschiedenis bestaat, dat koemelkspecifieke anti-body ‘ s van het IgE-type worden aangetoond door middel van huidtests en / of de bepaling van specifiek ige-gemedieerd serum en de bevestiging ervan door middel van de challenge-test. De challenge test is gecontra-indiceerd bij de diagnose van patiënten met ernstige anafylactische reacties en is niet in alle gevallen noodzakelijk. In onze studie werd 3KU/l gekozen als het cut-off punt in de melk-specifieke IgE-waarden om de diagnostische challenge test of niet aan te bevelen, gebaseerd op een eerdere studie van zuigelingen die allergisch zijn voor CMP, waarin dit niveau een PPV van 91% voor een prevalentie van 44% liet zien 9.
Deze studie benadrukt de noodzaak om, indien aangewezen, de challenge test uit te voeren om een CMP-allergie te diagnosticeren, aangezien bij 39% van de in de studie opgenomen zuigelingen met een gegronde verdenking van een bijwerking op koemelk het bestaan van een klinische reactie na de inname van koemelk werd uitgesloten en zij daarom niet hoefden te worden uitgesloten van hun dieet.
huidverschijnselen (urticaria, angio-oedeem en erytheem) zijn de meest voorkomende en typische klinische expressie van IgE-gemedieerde CMP-allergie en waren aanwezig bij 94% van de patiënten die allergisch waren voor CMP in onze studie, vergelijkbaar met de 99% verkregen door Garcia-Ara et al 10.
een ander belangrijk klinisch teken is de afstoting door het kind van de aangepaste zuigelingenvoeding van koemelk, die werd aangetoond bij 25% van degenen die allergisch zijn voor CMP, wat een belangrijk klinisch teken is waarmee rekening moet worden gehouden.de resultaten van een recent gepubliceerde studie door Eggesbo et al gaven aan dat bij pre-disposed zuigelingen van wie de moeder allergisch was, de bevalling van een keizersnede het risico op het ontwikkelen van voedselallergieën zou kunnen verhogen, wat volgens de auteurs verband zou kunnen houden met de vertraging in de darmkolonisatie van het pasgeboren kind 11. Een hoger percentage van leveringen door keizersnede in onze studie dan in de algemene bevolking 12, werd niet waargenomen om ons te doen denken aan de invloed van deze factor in het uiterlijk van CMP Sensibilisatie.
volgens de resultaten van onze studie, die de resultaten van andere auteurs bevestigen 13,14, begint CMP-allergie klinisch aan te tonen gedurende het eerste levensjaar en treedt deze op na een min of meer lange periode van borstvoeding, in veel gevallen na het eerste voer met CMP aangepaste formule en in het algemeen in de eerste week nadat het in het dieet is opgenomen. Sensibilisatie kan zijn opgetreden tijdens de zwangerschap of na de geboorte, tijdens de periode van borstvoeding.
tijdens de zwangerschap kunnen kleine hoeveelheden voedseleiwitten de placenta passeren en de foetale circulatie bereiken om ige-Sensibilisatie te veroorzaken bij een genetisch gepredisponeerde foetus. De uitgevoerde tests hebben echter geen bescherming aangetoond tegen de ontwikkeling van CMP-allergie met een dieet met uitzondering van koemelk tijdens de zwangerschap. In het overzicht van de Cochrane Collaboration dat in 1999 werd uitgevoerd, werden geen aanwijzingen gevonden voor een vermindering van de prevalentie van CMP-huidtesten bij kinderen van moeders die tijdens de zwangerschap een uitsluitingsdieet volgden 15.
het belangrijkste voordeel van borstvoeding bij de preventie van voedselsensibilisatie is fundamenteel gebaseerd op het relatieve gebrek aan voedselallergenen in moedermelk. Dit is echter een tweesnijdend wapen, aangezien uit experimenteel onderzoek bij dieren blijkt dat kleine hoeveelheden antigeen, op microgram-tot picogramniveau, bij voorkeur ige-responsen 16 kunnen induceren, terwijl grotere hoeveelheden, op milligramniveau, de IgE-respons onderdrukken en de mate van onderdrukking afhankelijk is van de dosis 17.
experimentele studies hebben aangetoond dat orale tolerantie voor voedseleiwitten kan worden geïnduceerd 18. De leeftijd van het dier en de dosis van het voedselallergeen zijn kritiek voor tolerantie te worden veroorzaakt. De neonatale periode lijkt de optimale tijd 19. Hoe groter de dosis antigeen en de frequentie van toediening, hoe waarschijnlijker het is dat tolerantie wordt bereikt en de IgE-respons onderdrukt 20.
Er is aangetoond dat kleine hoeveelheden koemelkeiwitten en andere voedingsmiddelen zoals ei en pinda ‘ s de zuigeling kunnen bereiken via borstvoeding 21-23. De hoeveelheid bètalactoglobuline in een druppel koemelk is berekend op basis van de hoeveelheid bètalactoglobuline in 200 liter moedermelk. Maar toch bevat moedermelk ongeveer evenveel bèta-lactoglobuline per druppel als de hoeveelheid pollenallergeen die per dag wordt ingeademd tijdens het hooikoortseizoen. Daarom is het geenszins onmogelijk voor kinderen om gevoelig te worden voor koemelk, ook al krijgen ze uitsluitend borstvoeding 24.
in een recente prospectieve studie uitgevoerd door Saarinen et al, waarbij 6209 zuigelingen vanaf de geboorte werden gecontroleerd om het optreden van symptomen van CMP-allergieën te evalueren, bleek uitsluitend borstvoeding gedurende twee maanden een risicofactor te zijn voor een allergische IgE-gemedieerde respons op CMP 25. Høst en andere auteurs beweren dat dit alleen gebeurt als er tijdens de neonatale periode eerder aan dit voedsel is blootgesteld 26. Uit studies van Saarinen e.a. blijkt echter dat, hoewel voeding met aangepaste koemelkvoeding bij Moederschap het risico van allergie voor CMP verhoogt in vergelijking met andere voedingssupplementen, uitsluitend borstvoeding het risico niet elimineert en dat de gecumuleerde incidentie van CMP-allergie bij zuigelingen die tijdens het moederschap een supplement met aangepaste voeding kregen, vergelijkbaar was met die bij zuigelingen die uitsluitend borstvoeding kregen. In een gecontroleerd dubbelblind onderzoek dat onlangs werd uitgevoerd door de Jong et al, verhoogde het voeden met koemelk in de eerste twee levensdagen voor het begin van de borstvoeding het risico op het ontwikkelen van atopische ziekten in de eerste twee levensjaren niet 27.
in onze studie had slechts 41% van degenen die allergisch zijn voor CMP aanvullende voeding gekregen tijdens de zwangerschap of tijdens de periode van borstvoeding, waarvoor, in tegenstelling tot het werk van Høst, blootstelling tijdens de neonatale periode, hoewel deze kan samenwerken, niet doorslaggevend lijkt voor het ontstaan van CMP-allergie.
klinische ervaring geeft aan dat bij zuigelingen die vanaf de geboorte kunstmatig aangepaste koemelkvoeding krijgen, het optreden van CMP-allergie uitzonderlijk is 3,14. In onze studie, hadden slechts twee van de 234 zuigelingen gediagnosticeerd met CMP allergie kunstmatige melk vanaf de geboorte ontvangen. In deze twee gevallen werd de toediening van de aangepaste formule op de leeftijd van één maand onderbroken als gevolg van spijsverteringssymptomen, waarbij het werd vervangen door een uitgebreid hydrolysaat, met een allergische reactie op CMP ocurring wanneer aangepaste koemelkformule opnieuw werd ingevoerd. Onlangs gepubliceerde experimentele studies tonen aan dat bij niet-gesensibiliseerde muizen, die slechts één week lang een aangepaste koemelkformule of 4 weken lang een gedeeltelijk hydrolysaat gebruiken, orale tolerantie ontstaat voor ige-respons op CMP 28. Degenen die met extensief hydrolysaat-of caseïneserum werden gevoerd, ontwikkelden echter geen tolerantie, hetgeen eerdere studies bevestigde 17. Kleine peptiden en aminozuren in extensieve hydrolysaten lijken geen van beide toleranties of immunogenen te zijn.het introduceren van grote hoeveelheden CMP vanaf de geboorte en de daaropvolgende ononderbroken toediening ervan lijkt de inductie en handhaving van tolerantie te stimuleren en het optreden van allergische reacties op dit voedsel te voorkomen.
onderbreking van de blootstelling aan het voedselallergeen bij gesensibiliseerde en tolerante patiënten kan leiden tot verlies van tolerantie, zoals is aangetoond met sommige levensmiddelen zoals vis en pinda ‘ s 29,30.
slechts 4% werd gesensibiliseerd voor soja, waarbij deze allemaal tolerant waren. Soja-allergie komt zeer zelden voor bij kinderen met atopische aandoeningen en in een groep van 243 kinderen met atopische ouders, die gedurende de eerste 6 maanden van hun leven werden gevoed met soja-formule en gedurende 5 jaar werden gecontroleerd, vertoonde slechts één gedocumenteerde allergie voor soja door middel van huidtesten en dubbelblinde challenge tests 31.
ei was niet geïntroduceerd in het dieet van de zuigelingen in onze studie, hoewel sensibilisatie voor eiwit werd aangetoond in 30% van hen. Deze gegevens bevestigen het belang van het bestuderen van sensibilisatie aan ei in die allergisch zijn voor CMP om de verschijning van een reactie te verhinderen wanneer het aan dieet 32 wordt geïntroduceerd.
sensibilisatie voor rundvlees werd waargenomen bij 29% van de onderzochte patiënten, hoewel ze allemaal gekookt rundvlees verdroegen. Dit is toe te schrijven aan het allergeen verantwoordelijk voor sensibilisatie aan rundvlees die een runderserumalbumine zijn dat thermolabile is, wat betekent dat zijn allergisch potentieel door het koken 33 wordt vernietigd en het slechts een reactie veroorzaakt wanneer gegeten ruw of gedeeltelijk ruw 34. Dit betekent dat rundvlees niet hoeft te worden uitgesloten van het dieet van kinderen die allergisch zijn voor CMP, zolang het gekookt wordt gegeten.
De CMPA treedt fundamenteel op tijdens het eerste halfjaar van het leven en valt samen met de introductie ervan in het dieet van het kind, na een min of meer lange periode van borstvoeding. Sensibilisatie voor CMP kan optreden na uitsluitend borstvoeding, hoewel het kind geen aanvullende voeding van aangepaste koemelkformule heeft ontvangen tijdens het geven van borstvoeding. Bij die patiënten met CMPA, sensibilisatie voor ei kan worden gezien vóór zijn inleiding tot het dieet. Het uitvoeren van een geschikt Diagnostisch protocol bij zuigelingen die voor een verdacht risico van koemelkallergieën bijwonen maakt allergie om in een hoog percentage van gevallen worden verdisconteerd.