Grotere Arenes
De meeste arenes die een enkele zes-membered ring bevatten, zijn vluchtige vloeistoffen, zoals benzeen en de xylenen, hoewel sommige arenes met substituenten op de ring vaste stoffen zijn bij kamertemperatuur. In de gasfase is het dipoolmoment van benzeen nul, maar de aanwezigheid van elektronegatieve of elektropositieve substituenten kan resulteren in een netto dipoolmoment dat de intermoleculaire aantrekkingskracht verhoogt en het smelt-en kookpunt verhoogt. Zo heeft 1,4-dichloorbenzeen, een verbinding die wordt gebruikt als alternatief voor naftaleen bij de productie van mottenballen, een smeltpunt van 52,7°C, wat aanzienlijk hoger is dan het smeltpunt van benzeen (5,5°C).bepaalde aromatische koolwaterstoffen, zoals benzeen en benzpyreen, zijn krachtige levertoxinen en carcinogenen. In 1775 beschreef een Britse arts, Percival Pott, de hoge incidentie van kanker van het scrotum onder kleine jongens gebruikt als schoorsteenveger en toegeschreven aan hun blootstelling aan roet. Zijn conclusies waren juist: benzpyreen, een component van roet uit de schoorsteen, houtskool-gegrild vlees en sigarettenrook, was het eerste chemische carcinogeen dat werd geïdentificeerd.
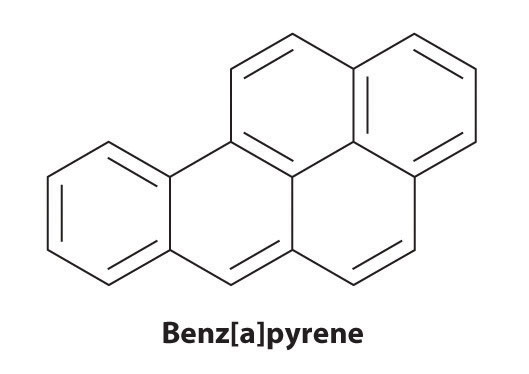
hoewel arenes gewoonlijk met drie C=C-bindingen worden getrokken, is benzeen ongeveer 150 kJ/mol stabieler dan verwacht zou worden indien het drie dubbele bindingen bevat. Deze verhoogde stabiliteit is toe te schrijven aan de delokalisatie van de elektronendichtheid π over alle atomen van de ring. Vergeleken met alkenen zijn arenes slechte nucleofielen. Daarom ondergaan ze geen additie-reacties zoals alkenen; in plaats daarvan ondergaan ze een verscheidenheid aan elektrofiele aromatische substitutiereacties waarbij –H op het arene wordt vervangen door een groep –E, zoals –NO2, –SO3H, een halogeen of een alkylgroep, in een tweestapsproces. De eerste stap omvat toevoeging van de elektrofiel (E) aan het π-systeem van benzeen, die een carbocatie vormen. In de tweede stap gaat er een proton verloren van de aangrenzende koolstof op de ring:
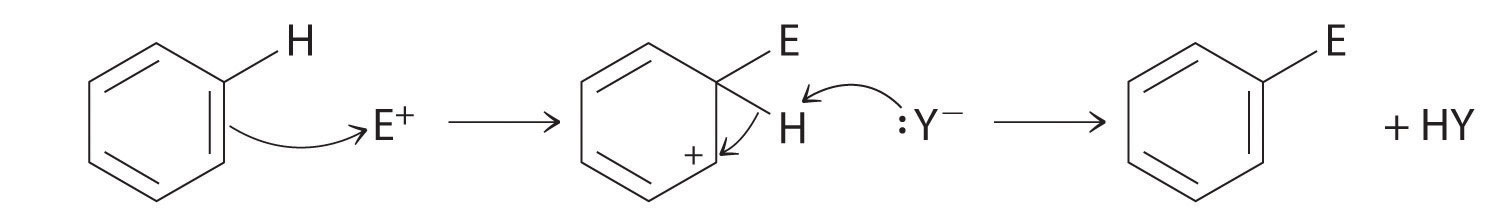
De in de eerste stap gevormde carbocatie wordt gestabiliseerd door resonantie.
Arenes ondergaan eerder substitutiereacties dan eliminatie vanwege verhoogde stabiliteit als gevolg van delokalisatie van hun π elektronendichtheid.
veel gesubstitueerde arenes hebben een krachtige biologische activiteit. Sommige voorbeelden omvatten gemeenschappelijke drugs en antibiotica zoals aspirine en ibuprofen, illegale drugs zoals amfetamines en peyote, het aminozuur fenylalanine, en hormonen zoals adrenaline zoals hieronder getoond.
aspirine (antifever activiteit), ibuprofen (antifever en anti-inflammatoire activiteit) en amfetamine (stimulerend middel) hebben farmacologische effecten. Fenylalanine is een aminozuur. Adrenaline is een hormoon dat de “strijd of vlucht” reactie op stress lokt.