Så Som du vet, Dmitri Mendeleev er far til periodic table. Men visste Du At Det Moderne Periodiske Bordet vi bruker faktisk ble utviklet av en forsker Ved Navn Henry Moseley? La oss lære den fascinerende historien bak det periodiske bordet.
Suggested Videos
moderne periodisk tabell
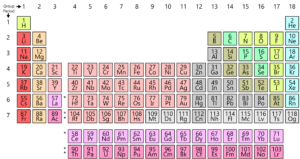
som du vet, er alle elementene som finnes på jorden arrangert i et rutenett eller matrise kalt det moderne periodiske bordet. Disse elementenes arrangement er i henhold til et mønster. Det periodiske bordet ble faktisk utviklet Og Av Mendeleev tidlig på 1800-tallet. Imidlertid ble Det faktisk perfeksjonert Av Henry Moseley, en engelsk fysiker i 1913. Ved å gjøre tilpasninger til den periodiske loven, forbedret han på alle feilene I Mendeleev-bordet. La oss se på denne utviklingen.
Bla gjennom Flere Emner Under Periodisk Klassifisering Av Elementer
- Tidligere Forsøk På Klassifisering Av Elementer
- Posisjon Av Elementer i Den Moderne Periodiske Tabellen
- Trender i Den Moderne Periodiske Tabellen
Ved Hjelp Av Atomnummer
Først, la Oss ta en titt på et atom struktur. Hvert atom består av en kjerne som består av protoner og nøytroner. Her har protonene en positiv ladning og et nøytron har ingen ladning. Nå omgir elektroner (som bærer en negativ ladning) kjernen. Nå er atommassenummeret det totale antallet protoner og nøytroner i et atom. Atomnummeret er antallet protoner i et atom. Dette atomnummeret er helt unikt for hvert element, noe som betyr at hvert element på planeten har sitt eget unike atomnummer.Det Var Henry Moseley som foreslo et bedre arrangement enn Mendeleev. Han arrangerte elementene i Henhold Til Deres Atomnummer i stedet for Deres atommasse. Ved å gjøre dette forbedret han på forrige bord og fjernet noen av sine vanskeligheter og anomalier.
Posisjon Av Hydrogen
Mendeleev kunne aldri finne Ut Riktig Posisjon Av Hydrogen i hans bord. Siden hydrogen kan enten få eller miste et elektron, kan det finne et sted i Gruppe 1 eller 17. Den elektroniske konfigurasjonen ligner den av alkalimetaller. Selv om det også kan kombinere med metaller og ikke-metaller som danner kovalente bindinger som Halogener.
Men i det moderne periodiske bordet er det ikke noe dilemma. Siden Atomnummeret til hydrogen er 1, er Det der Det finner sitt passende sted ved starten av bordet.
Isotoper
Isotoper Er forskjellige atomer av et element som hver har samme antall protoner, men et annet antall nøytroner i deres kjerner. Dette innebærer at selv om deres atommasse varierer, er deres atomnummer det samme. Som For eksempel Er Karbon-14 en radioaktiv isotop av karbonatomet som har åtte nøytroner.Mens Dette presenterte Et problem For Mendeleev, siden tabellen var avhengig av atommasse, er det ikke et problem med Det Moderne Periodiske bordet. Alle isotoper av elementene har ikke separate steder på bordet.
Rekkefølge av visse elementer
Mendeleev Ved bruk av atommasse for å ordne elementer møtte et annet problem. Det var visse tilfeller der det var en bryte av denne ordningen så elementer med lignende egenskaper var i en gruppe sammen. Ta eksemplet På Jod og Tellurium. Nå er jodens atommasse lavere enn tellurium. Og Likevel satte Mendeleev det etter tellur, slik at det kunne være i samme gruppe som fluor og klor.
i den moderne periodiske tabellen blir atommassen irrelevant og elementer grupperes med lignende elementer basert på deres atomnummer.
Sjeldne Jordelementer
det moderne periodiske bordet løste et annet problem ved å plassere sjeldne jordelementer som Cerium, Lantan, Erbium etc i et eget bord nederst I Det Periodiske bordet, for ikke å forstyrre Den Periodiske Loven.
Løst Eksempel for deg
Q: Av alle de 118 elementene som er kjent for oss, hvor mange elementer forekommer naturlig?