Nøkkelbegreper
Pass på at du kan definere og bruke nøkkelbegrepene nedenfor i sammenheng.
- Adams’ katalysator
- hydrogenering
Studienoter
Kjemiske reaksjoner som er heterogene har reaktanter som er i minst to forskjellige faser (f.eks. gass med et fast stoff), mens homogene reaksjoner forekommer i en enkelt fase (f. eks. gass med en annen gass).
noe forvirring kan oppstå fra beskrivelsen av katalysatoren som brukes i reaksjonen mellom alkener og hydrogen. Tre metaller-nikkel, platina og palladium-brukes ofte—men en kjemiker kan ikke bare plassere et stykke av en av disse metallene i en blanding av alken og hydrogen og få en reaksjon. Hver metallkatalysator må fremstilles på en spesiell måte:
- nikkel brukes vanligvis i en finfordelt form kalt » Raney nickel.»Det er forberedt ved å reagere En Ni-Al legering Med NaOH .
- palladium oppnås kommersielt «støttet» på en inert substans, slik som kull, (Pd / C). Alken oppløses vanligvis i etanol når Pd / C brukes som katalysator.platina brukes Som PtO2, Adams ‘ katalysator, selv om det faktisk er platinametall som er katalysatoren. Hydrogenet som brukes til å legge til karbon-karbon dobbeltbinding reduserer også platina (IV) oksydet til fint delt platinametall. Etanol eller eddiksyre brukes som løsningsmiddel for alken.
Andre typer forbindelser som inneholder flere bindinger, som ketoner, estere og nitriler, reagerer ikke med hydrogen under betingelsene som brukes til å hydrogenere alkener. Eksemplene nedenfor viser reduksjon av et alken, men keton-og nitrilgruppene som er tilstede forblir intakte og reduseres ikke.

Aromatiske ringer blir heller ikke redusert under de forhold som brukes til å redusere alkener, selv om disse ringene ser ut til å inneholde tre karbon-karbon dobbeltbindinger. Som du vil se senere, inneholder aromatiske ringer egentlig ikke noen dobbeltbindinger, og mange kjemikere foretrekker å representere benzenringen som en sekskant med en sirkel inne i den

i stedet for som en sekskant med tre vekslende dobbeltbindinger.
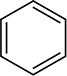
representasjonen av benzenringen vil bli diskutert videre I Avsnitt 15.2.reaksjonen mellom karbon-karbon dobbeltbindinger og hydrogen gir en metode for å bestemme antall dobbeltbindinger tilstede i en forbindelse. For eksempel reagerer en mol cykloheksen med en mol hydrogen for å produsere en mol cykloheksan:

men en mol 1,4-cykloheksadien reagerer med to mol hydrogen for å danne en mol cykloheksan:
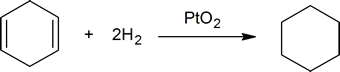
en kjemiker vil si at cykloheksen reagerer med en ekvivalent av hydrogen, og 1,4-cykloheksadien reagerer med to ekvivalenter av hydrogen. Hvis du tar en kjent mengde av et ukjent, umettet hydrokarbon og bestemmer hvor mye hydrogen det vil absorbere, kan du lett bestemme antall dobbeltbindinger som er tilstede i hydrokarbonet(se spørsmål 2 nedenfor).
Tilsetning av hydrogen til en karbon-karbon dobbeltbinding kalles hydrogenering. Den samlede effekten av et slikt tillegg er reduktiv fjerning av dobbeltbindingsfunksjonsgruppen. Regioselektivitet er ikke et problem, siden samme gruppe (et hydrogenatom) er bundet til hver av dobbeltbindingskarbonene. Den enkleste kilden til to hydrogenatomer er molekylært hydrogen (H2), men blanding av alkener med hydrogen resulterer ikke i noen merkbar reaksjon. Selv om den totale hydrogeneringsreaksjonen er eksoterm, forhindrer en høy aktiveringsenergi at den finner sted under normale forhold. Denne begrensningen kan omgåes ved bruk av en katalysator, som vist i følgende diagram.
et eksempel på en alken addisjon reaksjon er en prosess som kalles hydrogenation.In en hydrogeneringsreaksjon, to hydrogenatomer tilsettes over dobbeltbindingen av en alken, noe som resulterer i en mettet alkan. Hydrogenering av en dobbeltbinding er en termodynamisk gunstig reaksjon fordi den danner et mer stabilt (lavere energi) produkt. Med andre ord er energien til produktet lavere enn reaktantens energi; dermed er det eksoterm (varme frigjøres). Varmen som frigjøres kalles varmen av hydrogenering, som er en indikator på et molekyls stabilitet.


Katalysatorer Er stoffer som endrer hastigheten (hastigheten) av en kjemisk reaksjon uten å bli konsumert eller vises som en del av produktet. Katalysatorer virker ved å senke aktiveringsenergien til reaksjoner, men de endrer ikke den relative potensielle energien til reaktantene og produktene. Finfordelte metaller, som platina, palladium og nikkel, er blant de mest brukte hydrogeneringskatalysatorene. Katalytisk hydrogenering foregår i minst to trinn, som vist i diagrammet. Først må alken adsorberes på overflaten av katalysatoren sammen med noe av hydrogenet. Deretter skifter to hydrogen fra metalloverflaten til karbonene i dobbeltbindingen, og det resulterende mettede hydrokarbonet, som er svakere adsorbert, forlater katalysatoroverflaten. Den nøyaktige naturen og tidspunktet for de siste hendelsene er ikke godt forstått.

som vist i energidiagrammet er hydrogeneringen av alkener eksoterm, og varme frigjøres tilsvarende DEN Δ (farget grønn) i diagrammet. Denne reaksjonsvarmen kan brukes til å evaluere den termodynamiske stabiliteten til alkener som har forskjellige antall alkylsubstituenter på dobbeltbindingen. For eksempel viser tabellen nedenfor hydrogeneringsvarmen for tre c5h10 alkener som gir det samme alkanproduktet (2-metylbutan). Siden en stor reaksjonsvarme indikerer en høy energireaktant, er disse varmene omvendt proporsjonale med stabilitetene til alken-isomerer. Til en grov tilnærming ser vi at hver alkylsubstituent på en dobbeltbinding stabiliserer denne funksjonelle gruppen med litt mer enn 1 kcal / mol.
| Alkene Isomer | (CH3)2CHCH=CH2 3-methyl-1-butene |
CH2=C(CH3)CH2CH3 2-methyl-1-butene |
(CH3)2C=CHCH3 2-methyl-2-butene |
|---|---|---|---|
| Heat of Reaction ( ΔHº ) |
–30.3 kcal/mole | –28.5 kcal/mole | –26.9 kcal/mole |

fra mekanismen som vises her, forventer vi at tilsetning av hydrogen skal skje med syn-stereoselektivitet. Dette er ofte sant, men hydrogeneringskatalysatorene kan også forårsake isomerisering av dobbeltbindingen før hydrogentilsetning, i så fall kan stereoselektivitet være usikker.

Øvelser
- i reaksjonen
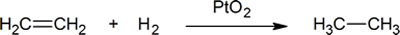
- 0,500 mol av eten reagerer med _ _ _ _ _ _ mol av hydrogen. Dermed kan en kjemiker si at eten reagerer med en _ _ _ _ _ _ _ av hydrogen.
- eten blir_______; mens _ _ _ _ _ _ _ blir oksidert.
- oksidasjonstallet av karbon i eten er_______; i etan er det_______.
- når 1.000 g av et bestemt triglyserid (fett) behandles med hydrogengass i Nærvær Av Adams katalysator, er det funnet at volumet av hydrogengass som forbrukes ved 99,8 kPa Og 25,0°C Er 162 mL. Et separat eksperiment indikerer at fettens molare masse er 914 g mol−1. Hvor mange karbon-karbon dobbeltbindinger inneholder forbindelsen?
Svar:
-
Vis Svar
Examples
Question
Predict the products if the following alkenes were reacted with catalytic hydrogen.

Solution

Contributors
- Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
- Prof. Steven Farmer (Sonoma State University)
- Organisk Kjemi med Biologisk Vekt Av Tim Soderberg (University Of Minnesota, Morris)