개념의 열기 원(“원”)
원자(또는 원자가)의 요소를 측정의 결합력으로 다른 원자 할 때 그것을 형태의 화학 화합물 또는 분자. 원자가 개념은 19 세기 마지막 절반에 개발되었으며 많은 유기 화합물의 분자 구조를 설명하는 데 성공했습니다. 퀘스트에 대한 근본 원인의 원도 현대적인 이론의 화학적 결합을 포함하여 루이스 구조(1916),원자가 결합이론(1927),molecular orbitals(1928),원자의 껍질 electron 쌍 반발 이론(1958 년)그리고 모든 고급 방법 quantum chemistry.
의 힘을 결합하거나의 선호도는 원자의 요소가의 수에 의해 결정된 수소 원자는 그것을 결합니다. 메탄에서 탄소는 4 의 원자가;암모니아에서 질소는 3 의 원자가;물에서는 산소가 2 의 원자가; 그리고 염화수소에서 염소는 원자가 1 입니다. 염소는 원자가 1 을 가지므로 수소로 치환 될 수 있으므로 인은 5 염화인 인 PCl5 에서 5 의 원자를 갖는다. 원자 다이어그램의 화합물을 나타내는 연결성의 요소인 사이에는 두 가지 요소라고 하는 채권에 표시되는 포화된 원자가 각 요소입니다. 예는 다음과 같습니다:-
| Compound | H2 | CH4 | C3H8 | C2H2 | NH3 | NaCN | H2S | H2SO4 | Cl2O7 |
| Diagram |  |
 |
 |
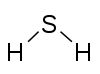 |
 |
 |
|||
| Valencies | Hydrogen 1 | Carbon 4 Hydrogen 1 |
Carbon 4 Hydrogen 1 |
Carbon 4 Hydrogen 1 |
Nitrogen 3 Hydrogen 1 |
Sodium 1 Carbon 4 Nitrogen 3 |
Sulfur 2 Hydrogen 1 |
Sulfur 6 Oxygen 2 Hydrogen 1 |
Chlorine 7 Oxygen 2 |
원자가만을 설명한 연결을 설명하지 않는 형상의 분자 화합물로,또는 어떤 지금은 것으로 알려진 이온화합물 또는 거대한 공유 구조물입니다. 원자 사이의 선은 루이스 다이어그램에서와 같이 한 쌍의 전자를 나타내지 않습니다.
Further Reading
Khan Academy
Valence Electrons
Cliffs Notes
Valence Electrons
Contributors
- Wikipedia