정상적인 세포 물질 대사에 따라 유지 보수 혈액의 pHwithin 매우 좁은 제한(7.35-7.45).
도 상대적으로 mildexcursions 외부 이 정상 pH 범위에 있을 수 있습 deleteriouseffects 포함하여,감소된 산소 전달을 조직,electrolytedisturbances 변화와 심장 근육의 수축,생존 israre 면 혈액의 pH 를 아래로 떨어지 6.8 또는 상승 7.8.
problemfor 몸은 정상적인 대사 관련 withcontinuous 수소의 생산이온(H+)과 이산화탄소(CO2),모두의는 경향을 줄이 pH. 이 mechanismwhich 이 문제를 극복하고를 제공해 혈액의 pH(즉,보존 산-염기성)는 복잡한 시너지 효과 ofaction 와 관련된 화학 버퍼에 혈액의 붉은 세포(적혈구)를 순환 혈액에 함수의 threeorgans:폐,신장,뇌.
는 방법을 설명하기 전에 이러한 fiveelements 에 기여하는 전반적인 유지보수 혈액의 pH,itwould 도움이 될을 신속하게 확인하려면 몇 가지 기본적인 개념입니다.
산이란 무엇이며,염기는 무엇이며 pH 는 무엇입니까?
산은 해결책에 있는 해리에 relaseshydrogen 이온(H+)물질입니다.예를 들어
: 염산(HCl)dissociates 을 hydrogenions 및 염화물 이온
HCl![]() H++Cl-
H++Cl-
탄산(H2CO3) dissociates tohydrogen 이온 그리고 중탄산이온
H2CO3![]() H++HCO3–
H++HCO3–
우리는 우리 사이 구별 강산화산 andweak 와 같은 지방산 탄산입니다. 차이점은 강산약산보다 더 많이 분리됩니다. 결과적으로 수소 이온강산의 농도는 약산보다 훨씬 높습니다.
염기는 용액에서 수산화 이온을 수용하는 물질입니다.
예를 들어,기본 중탄산염(HCO3–)지 수소이온 양식을 탄산:
HCO3–+H+![]() H2CO3
H2CO3
pH 의 가늠자 0-14 이며의 산과 알칼리성이다. 순수한 물에는 pH 가 7 이며 중성(산성도 알칼리성도 아님)입니다. ph 위 7is 알칼리성 아래 7 산성. 따라서 혈액의 pH(7.35-7.45)isslightly 알칼리지에 있는 임상 의학 장 alkalosisis,아마도 오인을 위해 예약,혈액보다 큰 pH7.45 산증이라는 용어는 7.35 미만의 혈액 pH 를 위해 예약되어 있습니다.
pH 는 수소 이온 농도(H+)의 척도입니다.두 가지가 관련이 있는 에 따라 followingequation:
pH=-log10
곳은 농도의 수소이온 inmoles 리터당(mol/L)
에서 이 방정식
pH7.4=H+농도의 40nmol/L
pH7.0=H+농도의 100nmol/L
pH6.0=H+농도의 1000nmol/L
그것은 분명:
- 두 개의 매개 변수를 변경에 반비례; 으로 수소이온 농도가 증가,pH 포
- 인해 로그 관계에 큰 변화 수소이온 농도를 실제로 작은 변화에 pH. 예를 들어,배로 수소이온농도 원 pH 로 0.3
What is a 버퍼? –는 중탄산염 완충 시
버퍼는 화학 물질에 솔루션을 최소화하는 변경에서 pH 발생하는 경우 산에 추가된’정리 ‘hydrogen 이온입니다. 완충액은 약산 및 그 용액이다.콘쥬게이트 염기. 혈액에서 원리 완충 시스템은 약합니다.산,탄산(h2co3)및 그 접합체,중탄산염(HCO3–). 설명 howthis 시스템을 최소화의 변화에서 pH 가정을 우리는 강산,예를 들어,HCl,하는 중탄산염 완충기:
산 것입니다 해리를 해제,수소이온:
HCl![]() H++Cl–
H++Cl–
중탄산 버퍼런’흡수하는’수소이온,formingcarbonic 산 과정에서:
HCO3–+H+![]() H2CO3(탄산)
H2CO3(탄산)
중요한 포인트이기 때문에 수소이온에서 HClhave 되었으로 통합된 약 탄산가 notdissociate 으로 쉽게 총수의 수소이온에서 solutionand 따라서 pH 변경되지 않는 한 많은 것 occurredin 부재의 버퍼입니다.
완충제는 변화를 크게 최소화하지만,약산(likecarbonic acid)조차도 어느 정도 해리되기 때문에 그것을 제거하지 못합니다. Buffersolution 의 pH 는 weakacid 와 그 conjugate base 의 상대 농도의 함수입니다.
pH=6.1+로그(/)
어디=농도 ofbicarbonate
=농도의 탄산
이 관계로 알려져 있는 헨더슨-Hasselbalch 방정식,보여주는 pH 의 적용을 받는 비율의료(HCO3–)농축산(H2CO3)니다.
수소 이온이 중탄산염 완충액에 첨가됨에 따라:
H++HCO3–![]() H2CO3
H2CO3
중탄산염(base)소비(농도를 감소)andcarbonic 산은 생산(농도가 증가). 는 경우 hydrogenions 는 것을 계속 추가되는 모든 중탄산 결국 beconsumed(로 변환하여 탄산)와있을 것입 nobuffering 효력–pH 다음이 급격히 떨어지면 더산 wereadded.
경우,탄산이 될 수 있는 지속적으로 제거에서 시스템과 중탄산 끊임없이 생성,다음 thebuffering 용량 및 그러므로 pH 를 유지될 수 있 despitecontinued 추가 수소이온.
As 는 생리학의 세부 사항으로 명확해질 것입니다.산-염기 균형,즉 사실상 신체에서 일어나는 일들. Inessence,폐는 탄산(carbonic acid)의 제거를 보장하고 신장은 지속적인 재생을 보장합니다.탄산.
이 폐의 역할은 중탄산염 완충 시스템의 단일성에 의존하며 이는 탄산이 이산화탄소와 물로 전환 될 수있는 가능성입니다.
다음 방정식의 관계에 대해 설명합니다 allelements 의 중탄산 버퍼링 시스템에서 작동으로 thebody
H++HCO3–![]() H2CO3
H2CO3![]() H2O+CO2
H2O+CO2
이 주목하는 것이 중요하의 반응은 뒤집을 수 있습니다.방향은 각각의 상대 농도에 따라 달라집니다.요소. 그래서 예를 들어,상승 탄소 dioxideconcentration 힘의 반응 왼쪽으로 증가 formationof 탄산과 궁극적으로 수소이온.
이것은 이산화탄소의 산성화 가능성을 설명하고 폐와 적혈구가 전반적인 산-염기 균형을 이루는 중요한 원인으로 우리를 데려옵니다.
이 폐기능,수송의 CO2 및 산 basebalance
은 일정한 양의 CO2 혈액에서 필수적인 normalacid 기초 균형,반영하는 사이에 균형을 생산하는 결과적으로 조직의 세포 물질 대사 및 배설하여 폐 inexpired air.
이산화탄소가 배출되는 속도를 변화시킴으로써 폐는 혈액의 이산화탄소 함량을 조절합니다.만료 된 공기에서의 이산화탄소 생산에서 제거까지의 사건 순서는도 2 에 기술되어있다. 1.이산화탄소는 조직 세포에서 주변으로 확산됩니다.모세포 혈액(그림 1). 1a). 작은 비율은 혈액에 용해됩니다.플라스마는 변하지 않은 폐로 운반됩니다.
그러나 대부분은 물과의 결합이 탄산을 형성하는 적혈구에 확산됩니다.산은 수소 이온의 생산과 함께 해리되고비카보네이트. 수소이온과 결합 대비가 헤모글로빈(헤모글로빈은 행동으로 버퍼 여기)방 dangerousfall 에서 셀룰러 pH,그리고 중탄산염 확산을 따라 concentrationgradient 에 빨간색 셀룰라 플라즈마.
따라서 조직에서 생산되는 대부분의 탄소 디 옥시 드는 중탄산염 혈장으로 폐로 운반됩니다.
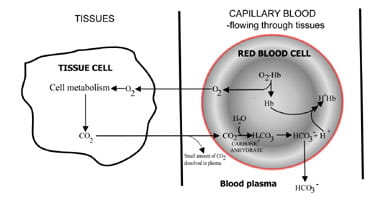
도. 1a.tissuescovered 에서 생성되는 이산화탄소폐로 운반하기 위해 중탄산염으로 변환됩니다.
|
|
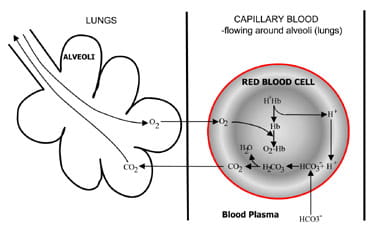
Fig. 1b. At the lungs bicarbonate convertedback to CO2 and eliminated by the lungs.
폐의 폐포에서 그 과정은 역전된다(그림 1). 1b).수소 이온은 산소를 차지함에 따라 헤모글로빈에서 변위됩니다.영감을받은 공기에서. 수소 이온은 이제 플라즈마에서 적혈구로 다시 확산되는 바이 카보네이트에 의해 완충되고,카보 닉산이 형성된다. 이것의 농도가 상승함에 따라 물 및 이산화탄소로 전환됩니다. 마지막으로,탄소 디 옥시드는적혈구에서 폐포로의 농도 구배를 낮추어 만료 된 공기에서 배출하십시오.
뇌 줄기의 호흡 화학 수용체는 변화에 반응합니다.혈액 중 이산화탄소 농도가 상승하면 호흡(호흡)이 증가하고 이산화탄소가 떨어지면 환기가 증가합니다.
신장과 산-염기 균형
정상적인 세포 대사는 수소 이온의 지속적인 생산을 초래합니다. 우리는 결합함으로써이 수소 이온,혈액의 중탄산염 완충액이 최소화됩니다.그들의 효과. 그러나 완충 작용은 단기간에만 유용하며 궁극적으로 수소 이온은 신체에서 제거되어야합니다.또한,사용되는 중탄산염이 중요합니다.수소 이온을 지속적으로 대체한다.
이 두 가지 작업,수소 이온의 제거와 중탄산염의 재생은신장에 의해 수행됩니다. 신장 세뇨관 세포는효소 탄산 탈수 효소가 풍부하여 이산화탄소와 물으로부터 카보 산 형성을 촉진합니다. 탄산은 해리된다.탄산 및 수소 이온. 중탄산염은 안으로 재흡수되고 수소 이온은 세뇨관의 루멘으로 통과하고 소변에서 몸에서 제거됩니다.
이 소변 제거는충충,주로 인산 및 암모니아 이온의 소변에서의 존재에 의존한다.
장애의 산-염기 평형
대부분이 산-염기 결과 장애에서
- 질병 또는 장기에 손상을(신장,폐,뇌)누구의 정상적인 기능을 위해 필요한 산-염기성,
- 질병의 원인이 증가 비정상적으로 생산의 대사산는 항상성 메커니즘은 압도
- 의학 작업(예: 기계 환기,일부 약물)
동맥혈 가스는 andmonitor 산-염기 장애를 식별하는 데 사용되는 혈액 검사입니다. 세 개의 매개변수를 측정 duringblood 가스 분석,동맥 혈액의 pH(pH),부분 압력 ofcarbon 이산화탄소에서 동맥혈(pCO2(a))andconcentration 의 중탄산염(HCO3–)는 ofcrucial 중요성(표 참조 참조(일반)의 범위).이 세 가지의 결과는 4 가지 병인학 적 범주 중 하나에 대한 산-염기성의 분류를 허용한다:
- Respiratory acidosis
- Respiratory alkalosis
- Metabolic acidosis
- Metabolic alkalosis
|
Adults |
Neonates |
|
|
pH |
7.35-7.45 |
7.30-7.40 |
|
pCO2 (kPa) |
4.7-6.0 |
3.5-5.4 |
|
Bicarbonate |
22-28 |
15-25 |
TABLE I. 대략적인 참조(정상)범위
는 방법을 이해하는 결과의 pH,pCO2(a)및 중탄산은 분류하는 데 사용되는 산-염기에서 장애 thisway,우리에게 반환해야 하 헨더슨-Hasselbalch 식
pH=6.1+로그(/)
우리는 pH 측정 및 중탄산나지 않는 탄산(H2CO3). 그러나,relationshipbetween pCO2(a)및 H2CO3which 허용하도록 재작성의 헨더슨-Hasselbalch 방정식 interms 세 개의 매개변수(pH,pCO2(a)andbicarbonate)측정하는 동안 혈액 가스 분석:
pH=6.1+로그(/(pCO2(a)×0.월 23 일))
제거하여 모든 상수에서 이 방정식,relationshipbetween 세 개의 측정 매개 변수가 될 수 있습니다 더 simplystated:
pH∝/pCO2(a)
이 관계에 중요한 이해의 모든 thatfollows 산에 관한 기본 장애,국는 arterialblood pH 에 비례 비율의 중탄산 concentrationto pCO2(a). 할 수 있습 followingdeductions:
- pH 정상적인 유지 너무 오랫동안 비율:pCO2(a)정상적인 유지
- pH 증가(즉,알칼리증 발생합니다)하거나 증가시키거나 피 co2(a)감소한다.
- pH 감소(즉 혈증 발생합니다)하거나 감소 또는 피 co2(a)증가
- 두 경우 모두 pCO2(a)과는 증가에 의해 상대적으로 동일한 금액 비율에 따라서 pH 는 정상
- 두 경우 모두 pCO2(a)및 감소하여 상대적으로 동일한 금액 비율에 따라서 pH 은 정상적입니다.
산-염기 장애는 주로 eitherpCO2(a)에 영향을 미치며,이 경우 호흡 장애라고 부르거나,이 경우 anon-respiratory 또는 metabolicdisturbance 라고합니다:
- 경우 기본 장애 발생 pCO2(a)(는 원인증–보상),조건이라고 호흡기 증
- 경우 주 소요 감소 pCO2(a)(는 원인은 알칼리증–보상),조건이라고 호흡 알칼리증
- 경우 기본 방해를 감소와 관련이 있는 중탄산염(는 결과를 증–위 참조), 조건이라고 대사성 산증
- 경우 기본 장애와 연관된 제기 중탄산염(는 결과 알칼리증–보상),조건은 불 대사 알칼리증
의 원인이 산-염기 장애
호흡 산증–(기 pCO2(a)감소,pH)
호흡 산증에 의해 특징입 increasedpCO2(a)로 인해 부적절한 폐기는 환기(저 환기)및 감소에 따른 제거 ofCO2 에서 혈액입니다. 호흡기 질환,이러한 asbronchopneumonia,폐기종,기관지 천식과 만성 폐쇄성 airwaysdisease 수 있습니다,모두 관련된 저 환기 충분 tocause 호흡기 증.약물 복용을 중단하지 않으려면 의사와상의해야합니다. 모르핀 andbarbiturates)는 뇌에 있는 therespiratory 센터를 우울하게 해서 호흡 산증을 일으키는 원인이 될 수 있습니다. 흉벽의 손상 또는 외상그리고 호흡의 역학에 관여하는 근육 조직은 환기 속도를 감소시킬 수 있습니다. 이 호흡기 acidosisthat 복잡하게 할 수 있습니다 물론과 같은 질병의 소아마비,Guillain-Barre syndrome 및 복구에서 심한 흉부 외상입니다.
호흡 알칼리증–(reducedpCO2(a),증가 pH)
대조적으로,호흡 알칼리증에 의해 특징입 decreasedpCO2(a)때문에 과도한 폐 ventilationand 결 과의 제거 CO2 에서 혈액입니다.혈액의 산소 감소(저산소 혈증)로 인해 호흡 센터가 자극되는 질병은 호흡 곤란을 초래할 수 있습니다.
여기의 예는 심한 빈혈,폐색전증 및 성인 호흡기 증후군을 포함한다. 과 호흡 충분히호흡기 알칼리증은 불안 발작의 특징 일 수 있으며심각한 통증에 반응합니다. 덜 환영받는 특성 중 하나살리 실 레이트(아스피린)는 호흡기에 대한 자극 효과입니다. 이 효과는 호흡기 알칼리증을 설명합니다.살리실산 과다 복용에 따라 발생합니다. 마지막으로,과열기계적 환기는 호흡 성 알칼리증을 유발할 수 있습니다.
대사성 산증–(감소 된 hco3–,pH 감소)
감소 된 중탄산염은 항상 대사 산증의 특징입니다. 이 중 하나가 발생합니다 두 가지 이유:사용이 증가 ofbicarbonate 버퍼링에서의 비정상적인산 부하거나 증가 lossesof 중탄산합니다. 당뇨병 케톤 산증 및 lacticacidosis 은 두 가지 조건을 특징으로 과잉 생산 ofmetabolic 산과 그에 따른 피로의 중탄산.
에서 첫 번째 경우,비정상적으로 높은 혈중 농도의 케토-산(b-hydroxybutyric acid 및 acetoacetic 산)반영 severemetabolic 혼란의 결과 insulindeficiency.
모든 세포 생산 락트산 불충분한 경우에,그래서 산소가 증가 젖산 생산 및 결과 metabolicacidosis 에서 발생하는 모든 조건에서 산소 전달을 thetissues 이 심각하게 손상됩니다.
예로는 심장 피뢰기 저 혈량 성 쇼크(예:massivefluid 손실)와 관련된 모든 상태가 있습니다. 간에 중요한 역할을 제거하 smallamount 의 젖산 생산되는 동안 정상적인 cellmetabolism 도록 유산증할 수 있는 기능의 liverfailure.
몸에서 중탄산염의 비정상적인 손실은 설사 중에 발생할 수 있습니다. 검사하지 않으면 대사성 산증으로 이어질 수 있습니다.중탄산염을 재생하고 수소 이온을 배설하지 못함 renalfailure 에서 발생하는 대사성 산증을 유발합니다.
대사성 알칼리증–(증가 된 hco3–,증가 된 pH)
중탄산염은 항상 대사성 알칼리증에서 발생합니다. 드물게 중탄산염의 과도한 투여 또는 중탄산염 제산 제제의 섭취는 대사성 알칼리증을 유발할 수 있지만 이는 일시적입니다. 몸에서 수소 이온의 비정상적인 손실은일차적 인 문제가 될 수 있습니다. 그렇지 않으면 beconsumed 것 중 탄산염 버퍼링 이러한 손실 수소 이온 결과적으로혈액. 위액은 산성 및 위산성 또는 위 내용물이있는 모든 질병 과정몸에서 수소 이온의 손실을 나타냅니다.예를 들어,위액의 발기 성 구토는 유문증 환자에서 발생할 수있는 대사성 알칼리증을 설명합니다. 심한 칼륨 고갈은 대사성 알칼로이드를 유발할 수 있습니다.수소와 칼륨 사이의 상호 관계 때문에.
보상의 결과산-basedisturbance
그것은 중요한 생활 pH 하지 않는 면제는 너무 멀리서 정상적인,그리고 몸은 항상 시도를 반환하는 비정상적인 pH towardsnormal 때 산-염기 평형을 방해한다. 보상은이생명 보존 과정에 주어진다. 이해하려면 ph 가 theratio:pCO2(a)에 의해 지배된다는 것을 상기하는 것이 중요합니다.비율이 정상인 한 pH 는 정상일 것입니다.
ph 가 낮은 대사성 산증 환자를 고려하십시오.중탄산염이 낮습니다. Tocompensate 낮은 및 복원정상을 향한 모든 중요한 비율은 환자가 hispco2(a)를 낮춰야합니다. 호흡기의 화학 수용체뇌의 중심부는 상승하는 수소 이온 농도(낮은 pH)에 반응하여 증가 된 환기(과 환기)를 유발하고 이산화탄소의 제거를 증가시킵니다.
보상에 대한 고혈당에서는,높은 대조적으로,involvesdepression 의 호흡과 그로 인하여 보존의 탄소 dioxideso 는 pCO2(a)상승과 일치하 있. 그러나,우울증감소증은 조직의 적정성을 위협하는 환영받지 못하는 부작용을 가지고 있습니다. 이러한 이유로 호흡기 보상메타볼 릭 알칼리증은 제한적입니다.
주의 장애 pCO2(a)(respiratoryacidosis 과 알칼리증)는 보상하여 신장 조 ofhydrogen 이온 배설하는 결과 변화하는 보상을 적절하게 forprimary 에서 변경 pCO2(a). 따라서 renalcompensation 한 호흡증(raisedpCO2(a)를)포함한 재 흡수가 증가 ofbicarbonate,그리고 신에 대한 보상 호흡 알칼리증(감소 pCO2(a)를)포함한 감소 bicarbonatereabsorption.
보상 중 산-염기 균형의 개념은도 1 에서 시각적으로 전달된다. 2. 표 II 는 보상 전 4 가지 산-염기 장애를 모두 특징 짓는 혈액 가스를 요약 한 것입니다.
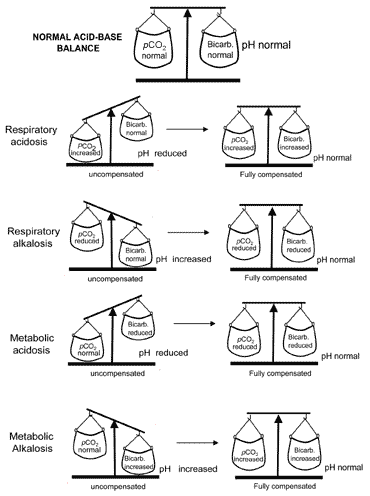
도. 2. “산-염기 균형” : compensationrestores normal pH
|
Primary disturbance |
||||
|
Respiratory |
Repiratory |
Metabolic |
Metabolic |
|
|
Some |
Emphysema |
Hyper- |
Renal failure |
Bicarbonate Potassium |
|
Compen- |
RENAL |
RENAL |
RESPIRA- |
RESPIRA- |
|
Initial blood |
pH |
pH |
pH |
pH |
|
Blood gas |
pH 피 co2 |
pH 피 co2 |
pH 피 co2 |
제한 |
|
Blood gas |
pH normal |
pH normal |
pH normal |
Limited |
테이블의 Printfriendly 버전,pdf.
TABLE II. 혈액 가스 결과 장애 ofacid 기초 균형
호흡기 보상에 대한 기본 대사 disturbanceoccurs 는 것보다 훨씬 더 빠르게 대사(신)에 대한 보상 aprimary 호흡 등이 있습니다. 두 번째 경우에는 보상시간이 아닌 며칠에 걸쳐 발생합니다.
보상 결과 ph 가 정상으로 돌아 오면 환자는 fullycompensated 라고한다. 그러나 많은 경우에 보상은 실제로 정상 성을 달성하지 않고 pHtowards 정상을 반환합니다; 그러한 경우환자는 부분적으로 보상받을 수 있다고합니다.
Forreasons 상술 한 바와 같이,대사성 알칼리증은 매우 드물게 충만하다.보상.
Mixed acid-base 장애
이것은 추측 수 있습니다 위에서 토론 thatall 환자산 기초 장애로 고통에서만 하나의 thefour 카테고리의 산-염기 평형. 이것은 잘 될 수 있지만,특정 상황에서 환자는 하나 이상의 방해와 함께 제시 할 수 있습니다.
예를 들어,폐기종과 같은 만성적 인 병이있는 환자를 고려합니다. 이 환자들도 adiabetic 했던 촬영하지 않은 자신의 정상적인 인슐린을 복용량으로 resultwas 의 상태에서 당뇨병 케톤 산증,혈액 가스 결과 wouldreflect 의 결합된 효과 호흡기 모두 증 andmetabolic 증.
이러한 혼합 된 산-염기 교란은 그렇지 않습니다.빈번하고 동맥혈 가스 결과만으로는 해명하기 어려울 수 있습니다.
요약
정비의 정상적인 혈액의 pH 를 포함하는 여러 기관이 systemsand 에 따라 순환기 무결성이 있습니다. 그것은 놀라운 일이 아닙 thenthat 장애 산-염기 평형의 복잡하게 할 수 있습니다 물론 ofwidely 다양한 질병 뿐 아니라 외상의 많은 부분 thebody. 몸은 혈액 pH 를 보존하기 위해 상당한 힘을 가지고 있으며지역은 일반적으로 심각한 만성 질환 또는 급성 질환을 의미합니다.
동맥혈 가스 분석의 결과는 산-염기 교란을 식별 할 수 있으며 그 원인 때문에 귀중한 정보를 제공합니다.
일부는 furtherreading
- Thomson WST,Adams JF,Cowan RA 를 제안했습니다. 임상 산-염기 균형. 옥스포드:옥스포드 의학 간행물 1997
- 해리슨 RA. 산-염기 균형. Respir Care Clin n.America1995;1,1:7-21
- Woodrow P. 동맥혈 가스 분석. 간호 표준 2004;18,21:45-52
- Sirker AA,Rhodes A,Gounds RM,Bennet ED. 산-염기 생리학:’전통적’과’현대적’접근법. 마취 2002;57:348-56