Così come sai, Dmitri Mendeleev è il padre della tavola periodica. Ma lo sapevate che la Tavola periodica moderna che usiamo è stato infatti sviluppato da uno scienziato di nome Henry Moseley? Impariamo l’affascinante storia dietro la tavola periodica.
Suggested Videos
la Moderna Tavola Periodica
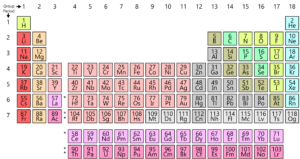
Come sapete, tutti gli elementi che si trovano sulla terra sono disposte in una griglia o matrice chiamato la Moderna Tavola Periodica. La disposizione di questi elementi è secondo uno schema. La tavola periodica fu effettivamente sviluppata e da Mendeleev nei primi anni del 1800. Tuttavia, è stato infatti perfezionato da Henry Moseley, un fisico inglese nel 1913. Apportando modifiche alla legge periodica, ha migliorato tutti i difetti del tavolo Mendeleev. Diamo un’occhiata a questo sviluppo.
Sfoglia altri argomenti sotto Classificazione periodica degli elementi
- Precedenti tentativi di classificazione degli elementi
- Posizione degli elementi nella tavola periodica moderna
- Tendenze nella Tavola periodica moderna
Usando il numero atomico
Per prima cosa, diamo un’occhiata alla struttura di un atomo. Ogni atomo è costituito da un nucleo costituito da protoni e neutroni. Qui i protoni hanno una carica positiva e un neutrone non ha carica. Ora gli elettroni (che trasportano una carica negativa) circondano il nucleo. Ora il numero di massa atomica è il numero totale di protoni e neutroni in un atomo. E il numero atomico è il numero di protoni in un atomo. Questo numero atomico è completamente unico per ogni elemento, il che significa che ogni elemento sul pianeta ha il proprio numero atomico unico.
Fu Henry Moseley a suggerire un arrangiamento migliore di Mendeleev. Ha organizzato gli elementi secondo il loro numero atomico piuttosto che la loro massa atomica. In questo modo ha migliorato la tabella precedente e rimosso alcune delle sue difficoltà e anomalie.
Posizione dell’idrogeno
Mendeleev non è mai riuscito a capire la posizione corretta dell’idrogeno nella sua tabella. Poiché l’idrogeno può guadagnare o perdere un elettrone può trovare un posto nel Gruppo 1 o 17. La sua configurazione elettronica ricorda quella dei metalli alcalini. Sebbene possa anche combinarsi con metalli e non metalli formando legami covalenti come gli alogeni.
Ma nella moderna tavola periodica, non c’è dilemma. Poiché il numero atomico dell’idrogeno è 1, è lì che trova il suo posto appropriato all’inizio della tabella.
Isotopi
Gli isotopi sono atomi diversi di un elemento ognuno dei quali ha lo stesso numero di protoni, ma un diverso numero di neutroni nei loro nuclei. Ciò implica che anche se la loro massa atomica varia, il loro numero atomico è lo stesso. Come ad esempio, il carbonio-14 è un isotopo radioattivo dell’atomo di carbonio che ha otto neutroni.
Mentre questo presentava un problema per Mendeleev, poiché la tabella dipendeva dalla massa atomica, non è un problema con la tavola periodica moderna. Tutti gli isotopi degli elementi non hanno posti separati sul tavolo.
Ordine di alcuni elementi
Mendeleev quando si utilizza la massa atomica per organizzare gli elementi affrontato un altro problema. Ci sono stati alcuni casi in cui c’è stata una rottura di questa disposizione quindi elementi con proprietà simili erano in un gruppo insieme. Prendi l’esempio di iodio e Tellurio. Ora la massa atomica di iodio è inferiore al tellurio. Eppure Mendeleev l’ha messo dopo il tellurio in modo che potesse essere nello stesso gruppo del fluoro e del cloro.
Nella tavola periodica moderna, la massa atomica diventa irrilevante e gli elementi sono raggruppati con elementi simili in base al loro numero atomico.
Elementi delle Terre rare
La moderna tavola periodica ha risolto un altro problema posizionando gli elementi delle terre rare come Cerio, Lantanio, Erbio ecc. in una tabella separata nella parte inferiore della tavola periodica, in modo da non interferire con la Legge periodica.
Esempio risolto per te
Q: Di tutti i 118 elementi a noi noti, quanti elementi si verificano naturalmente?