Tehát, mint tudod, Dmitrij Mendelejev az időszakos táblázat apja. De tudta, hogy a modern periódusos rendszert, amelyet használunk, valójában egy Henry Moseley nevű tudós fejlesztette ki? Tanuljuk meg a periódusos rendszer lenyűgöző történetét.
Suggested Videos
a Modern Periódusos
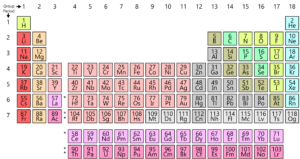
Mint tudod, minden elem megtalálható a földön vannak elrendezve egy rács, vagy a mátrix úgynevezett Modern Periódusos rendszer. Ezek az elemek elrendezése egy minta szerint történik. A periódusos rendszert valójában Mendelejev fejlesztette ki az 1800-as évek elején. Valójában azonban Henry Moseley, egy angol fizikus tökéletesítette 1913-ban. Az időszakos törvény kiigazításával javította a Mendelejev táblázat összes hibáját. Vessünk egy pillantást erre a fejlődésre.
további témák böngészése az elemek időszakos osztályozása alatt
- az elemek osztályozására irányuló korábbi kísérletek
- az elemek helyzete a Modern periódusos rendszerben
- trendek a Modern periódusos rendszerben
először nézzük meg az atom szerkezetét. Minden atom protonokból és neutronokból álló magból áll. Itt a protonok pozitív töltéssel rendelkeznek,a neutron pedig nem töltődik fel. Most az elektronok (negatív töltéssel) körülveszik a magot. Most az atomtömegszám az atomban lévő protonok és neutronok teljes száma. Az atomszám pedig az atomban lévő protonok száma. Ez az atomszám teljesen egyedülálló minden elemhez, ami azt jelenti, hogy a bolygó minden elemének megvan a saját egyedi atomszáma.
Henry Moseley volt az, aki jobb elrendezést javasolt, mint Mendelejev. Az elemeket atomszámuk szerint rendezte el, nem pedig Atomtömegük szerint. Ezzel javította az előző táblázatot, és eltávolította néhány nehézségét és anomáliáját.
A hidrogén helyzete
Mendelejev soha nem tudta kitalálni a hidrogén helyes helyzetét a táblázatában. Mivel a hidrogén elektront nyerhet vagy veszíthet, helyet találhat az 1.vagy a 17. csoportban. Elektronikus konfigurációja hasonlít az alkálifémekéhez. Bár a kovalens kötéseket alkotó fémekkel és nemfémekkel, például halogénekkel is kombinálható.
de a modern periódusos rendszerben nincs dilemma. Mivel a hidrogén atomszáma 1, ott találja meg a megfelelő helyet a táblázat elején.
izotópok
az izotópok egy elem különböző atomjai, amelyek mindegyikének azonos számú protonja van, de más számú neutron a magjában. Ez azt jelenti, hogy bár atomtömegük változik, atomszámuk megegyezik. Mint például a Carbon-14 a szénatom radioaktív izotópja, amelynek nyolc neutronja van.
míg ez problémát jelentett Mendelejev számára, mivel a táblázat az atomtömegtől függött, ez nem jelent problémát a Modern periódusos rendszerben. Az elemek összes izotópjának nincs külön helye az asztalon.
bizonyos elemek sorrendje
Mendelejev, amikor az atomtömegeket az elemek rendezésére használják, egy másik problémával szembesültek. Voltak olyan esetek, amikor ez az elrendezés megszakadt, így a hasonló tulajdonságokkal rendelkező elemek egy csoportban voltak. Vegyük például a jódot és a Telluriumot. Most a jód atomtömege alacsonyabb, mint a tellurium. Mendelejev mégis telluriumra tette, hogy ugyanabba a csoportba tartozzon, mint a fluor és a klór.
a modern periódusos rendszerben az atomtömeg irrelevánssá válik, és az elemeket atomszámuk alapján hasonló elemekkel csoportosítják.
a ritkaföldfémek
A modern periódusos sikerült megoldani egy problémát azáltal, hogy a ritkaföldfém elemek, mint például a Cérium, Lantán, Erbium stb egy külön táblázat alján, a Periódusos rendszer, így nem zavarja a Periódusos Törvény.
megoldott példa az Ön számára
Q: A számunkra ismert 118 elem közül hány elem fordul elő természetesen?