A nyitott Valence (“Valence”)
az elem valenciája (vagy valenciája) az elem más atomokkal való kombinációjának mértéke, amikor kémiai vegyületeket vagy molekulákat képez. A valence fogalmát a 19. század utolsó felében fejlesztették ki, és sikeresen elmagyarázta számos szerves vegyület molekuláris szerkezetét. A quest, a mögöttes oka valence vezet a modern elméletek, a kémiai kötés, beleértve Lewis struktúrák (1916), valence bond elmélet (1927), molekuláris elektronpályák (1928), valence shell elektron pár taszítás elmélet (1958), valamint a speciális módszerek a quantum chemistry.
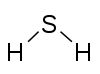
egy elem atomjának egyesítő erejét vagy affinitását az általa kombinált hidrogénatomok száma határozta meg. A metánban a szén valenciája 4; ammóniában a nitrogén valenciája 3; vízben az oxigén két vegyértékkel rendelkezik; a hidrogén-kloridban a klór valenciája 1. A klór, mivel egy vegyértékkel rendelkezik, helyettesíthető hidrogénnel, így a foszfor 5-ös valenciája a foszfor-pentakloridban, PCl5-ben. Valence diagramok egy vegyület képviseli a kapcsolat az elemek, vonalak két elem között, néha kötések, képviselt telített Valenciát minden elem. Példák:-
| Compound | H2 | CH4 | C3H8 | C2H2 | NH3 | NaCN | H2S | H2SO4 | Cl2O7 |
| Diagram |  |
 |
 |
 |
 |
 |
|||
| Valencies | Hydrogen 1 | Carbon 4 Hydrogen 1 |
Carbon 4 Hydrogen 1 |
Carbon 4 Hydrogen 1 |
Nitrogen 3 Hydrogen 1 |
Sodium 1 Carbon 4 Nitrogen 3 |
Sulfur 2 Hydrogen 1 |
Sulfur 6 Oxygen 2 Hydrogen 1 |
Chlorine 7 Oxygen 2 |
Valence csak a kapcsolatot írja le, nem írja le a molekuláris vegyületek geometriáját, vagy azt, amelyről ma ismert, hogy ionos vegyületek vagy óriási kovalens szerkezetek. Az atomok közötti vonal nem jelent elektronpárt, mint a Lewis diagramokban.
Further Reading
Khan Academy
Valence Electrons
Cliffs Notes
Valence Electrons
Contributors
- Wikipedia