vektorivälitteinen tauti (erityisesti biologinen siirto mekaanisen sijaan) on sairaus, jossa tartunnan leviäminen populaatiossa (isäntäpopulaatiossa) tapahtuu vain toisen populaation (vektoreilla) kautta. Tartunnanlevittäjät ovat yleensä verta syöviä niveljalkaisia, kuten hyttysiä, hietakärpäsiä tai punkkeja. Tällaisia tauteja on monia, joiden dynamiikka on erittäin kiinnostava infektion torjunnan kannalta. Malaria, leishmaniaasi, denguekuume ja Länsi-Niilin virus ovat vain muutamia, joilla on tällä hetkellä valtava yhteiskunnallinen vaikutus ihmispopulaatioihin.
joka vuosi Alueella 225 miljoonaa ihmistä saa malarialoisen tartunnan, ja vuonna 2009 noin 781 000 näistä johti taudin aiheuttamaan kuolleisuuteen. Tarina on samanlainen leishmaniaasi, jossa on noin 12 miljoonaa ihmistä maailmanlaajuisesti, joiden uskotaan olevan tartunnan milloin tahansa ja noin 80,000 ihmiset kuolevat vuosittain vakavin muoto, viskeraalinen leishmaniaasi. Tällaiset sairaudet ovat yleisiä kehitysmaissa; yhdistelmä optimaalinen elinympäristö vektoreille trooppisilla alueilla ja puute lääketieteellisen avun johtaa laajamittaiseen endemics siellä.
ihmisten taudit eivät ole ainoa huolenaihe, vaan monet muutkin tartuttavat muita isäntäluokkia, jotka ovat myös kiinnostavia erityisesti uhanalaisten lajien säilyttämisen kannalta.
tyypillinen tartunnankulku vektorivälitteisessä tartunnassa, jossa ei oteta huomioon tauteja, isäntäeläimiä tai vektorityyppejä, alkaa siten, että tartunnan saanut vektori (verta ruokkiva tai imevä AIKUINEN niveljalkainen) ottaa veriaterian isäntäpopulaation herkältä jäseneltä. Pureman jälkeen isännällä on mahdollisuus sairastua tautiin. Tässä vaiheessa, jos tartunta on saatu, isäntä katsotaan altistuneeksi, mutta ei aiheuta haitallisia vaikutuksia tartunnasta eikä voi levittää tautia. Aikaa tartunnan saamisen jälkeen, mutta ennen tartuntaa, kutsutaan latenssijaksoksi. Kun loinen on saavuttanut tietyn vaiheen lisääntymissyklissään, isäntä tulee tarttuvaksi, minkä jälkeen, jos se on purrut, se voi siirtää taudin alttiiseen vektoriin loisen saastuttaman veren kautta ja suorittaa siirtosyklin (esitetty alla olevassa kuvassa).
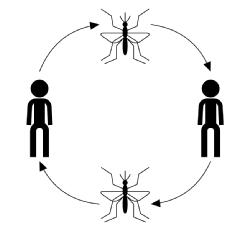
taudin tarttumista kuvataan yleensä:
- sekä isäntien että vektorien runsaus ja alueellinen leviäminen
- väestötiedot
- syöttönopeus tai vektorihalu purra
- tartunnan onnistuminen tai epäonnistuminen
tyypillisesti vektorivälitteisten tautien matemaattiset mallit perustuvat kahden populaation si(R)-malliin, jossa esiintyy ”Ristikkäiset” infektiotermit, missä ja
ovat termien tartuntavoima isännille ja vektoreille vastaavasti:
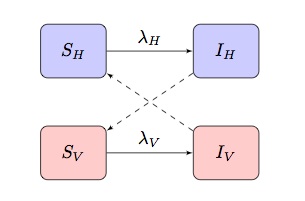
riippuen taudista ja populaatiosta, sitä voidaan mukauttaa sisällyttämään muita erityispiirteitä.
vektorivälitteisten tautien dynamiikan mallintaminen
vektorivälitteisten tautien leviämiselle on monia erityyppisiä matemaattisia malleja; ihannetapauksessa ne pyritään pitämään matemaattisesti jäljitettävinä ja mahdollisimman yksinkertaisina säilyttäen samalla biologisen järjestelmän yleinen dynamiikka. Yllättäviä malleja kirjallisuuden valikoimasta suuresti; deterministisestä stokastiseen, endeemiseen (mukaan lukien syntymä-ja kuolleisuusluvut) tai epidemiaan (rajattu epidemia), joka sisältää spatiaalisen leviämisen, spatiaalisen heterogeenisuuden, latenssijaksot, ikärakenteen, immuniteetin saamisen ja menetyksen, useita kantoja ja monia muita. Vaikka tarkasteltaisiin vain yhtä tiettyä tautia, taudin vaihtelut eri populaatioissa voivat johtaa muutoksiin parametrisoinnin lisäksi myös siinä, miten mallintamiseen voidaan suhtautua.
osa Katin töistä keskittyy yksinkertaistuksiin, joita usein tehdään mallien monimutkaisuuden vähentämiseksi. Tässä työssä tarkastellaan vaikutuksia käyttämällä ”isäntä-vain” transmission malleja, kuten kvasitasapaino oletus taudin dynamiikkaa ja myös vaikutusta jättämällä latenssijakso kun epidemia ennusteita.
leishmaniaasi
Erin
ihmisen Afrikkalainen Trypanosomiaasi (hattu)
ihmisen Afrikkalainen trypanosomiaasi (hattu), puhekielessä unitauti, on tappava tauti, joka on endeeminen suuressa osassa Saharan eteläpuolista Afrikkaa. Yli puolentoista miljoonan neliökilometrin riskialueilla asuu 70 miljoonaa ihmistä. Vaikka Hatin esiintyvyys ei ole yhtä suuri kuin muiden vektorivälitteisten tautien, kuten malarian tai denguekuumeen, esiintyvyys (HAT-tauteja oli hieman yli 7000, mutta 207 miljoonaa arvioitua malariatapausta vuonna 2012), kemiallisen ennaltaehkäisyn puute, erittäin epämiellyttävä (ja usein tappava) hoito ja huomattavan tieteellisen tutkimuksen puute ovat nyt nostaneet Hatin WHO: n laiminlyötyjen trooppisten sairauksien listalle.
Hatin vektori on tsetse; sen tarve veriruokintaan nälkiintymisen estämiseksi ja ainutlaatuinen vektori-loinen vuorovaikutus (aiheuttaen ”teneraalisen herkkyysilmiön”) tarkoittavat, että hatun mallinnus eroaa selvästi muista vektorivälitteisistä sairauksista, kuten malariasta.
alla oleva kuva on lokeroinen karikatyyri hatusta, joka sisältää:
- (osittainen) teneraalikärpäsherkkyys
- monen isäntälajin alttius (mukaan lukien reservoir ja muut kuin reservoir-isännät)
- tsetsen ruokintasuositus
- unfed tsetsen nälkiintyminen
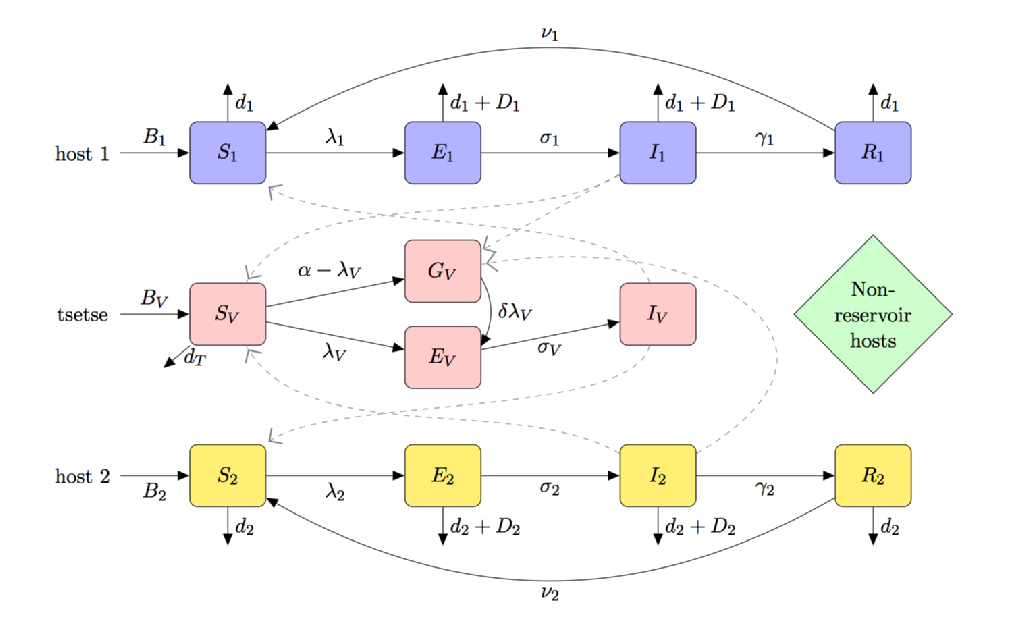
Bluetongue-tauti (BTV)
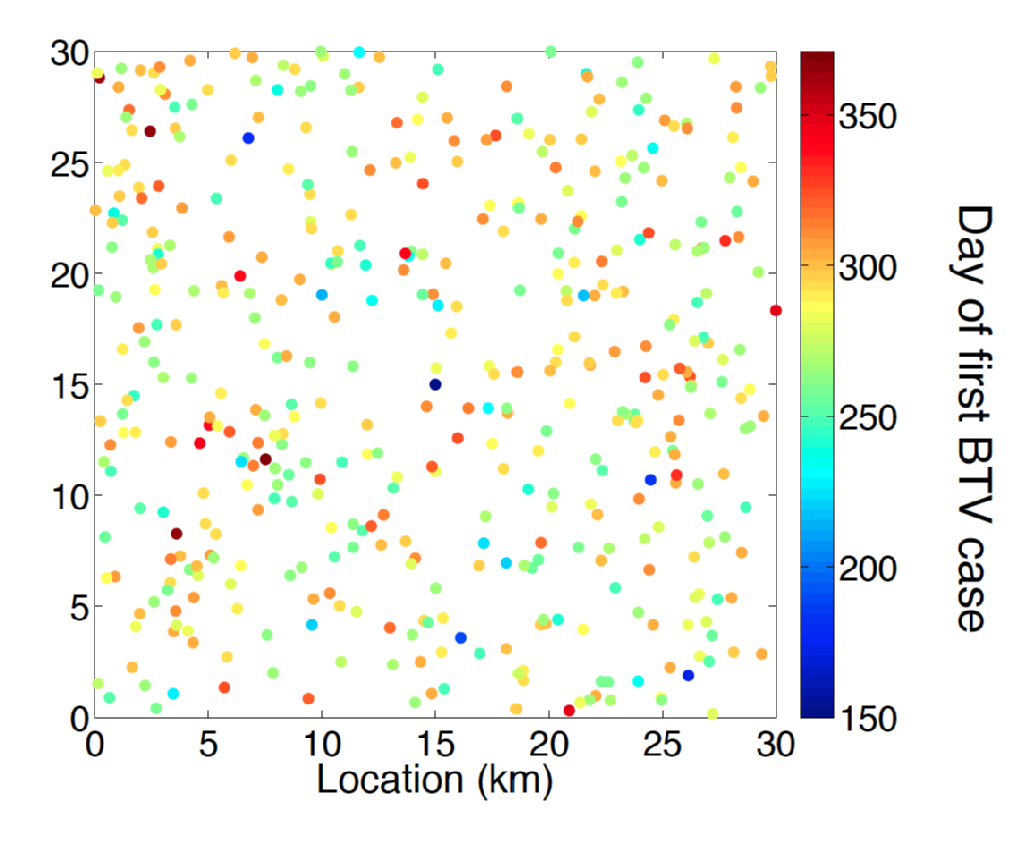
Bluetongue-tauti on eri culicoides-suvun purevien Midge-lajien välittämä märehtijöiden virustauti (BTV). BTV: tä sairastavan karjan oireita olivat epämukavuus, korkea kuume ja kielen syanoosi, josta tauti on saanut nimensä. Lampaiden keskuudessa BTV-tautiin liittyy korkea kuolleisuus. 1990-luvun loppupuolelle asti BTV: n eurooppalainen levinneisyysalue liittyi kokonaan midge-vektorin C. Imicola kantamaan. 90-luvun lopussa ja 2000-luvun alussa BTV: n levinneisyys on aiemmin ollut ennennäkemätöntä Euroopan alueilla, jotka kuuluvat muiden midgelajien, kuten C. Obsoletus complex-lajin ja läheistä sukua olevien midgelajien, levinneisyysalueeseen. Erityisesti Alankomaista vuonna 2006 alkanut taudinpurkaus on ensimmäinen kirjattu esimerkki BTV: n tunkeutumisesta 50 astetta pohjoista leveyttä. Seuraavina kesinä havaittiin BTV-tapauksia Pohjois-Euroopassa, mukaan lukien Belgiassa, Saksassa, Yhdistyneessä kuningaskunnassa ja Tanskassa, jotka osoittivat Bluetongue-taudin kyvyn ylitalveen Pohjois-Euroopan ympäristössä. Pohjois-Euroopan Bluetongue-taudin serologian hämmentävä piirre on se, että taudin aiheutti eri kanta (BTV-8) kuin Etelä-Eurooppaan tunkeutuneet eli Espanja (BTV-4) ja Italia (BTV-2).
BTV: n tunkeutumisen vaikutusten ennustaminen ja karjanhoidon ja tautien torjunnan paras suunnittelu edellyttävät huipputason mallintamismenetelmiä. BTV: n epidemiologiasta tiedetään paljon, kuten vankka käsitys nautaeläinten ja lampaiden isäntien odotetusta viremiakaudesta ja ilmaston lämpötilan vaikutuksesta Bluetongue-taudin itämisaikaan sen midge-vektorilla. Tartunnanlevittäjien leviämisestä pois tartunnan saaneista isäntäeläimistä aiheutuvan alue-ja ajallisen riskin arviointi on kuitenkin edelleen merkittävä haaste. Päättelyongelma tässä on monitekijäinen, joka vaatii parametrin päättelyn lisäksi myös tilastollisesti periaatteellista mallivalintaa.
Malaria
Malaria seuraa edellä kuvattua geneeristä siirtosykliä; vektorina on hyttysnaaras, joka ottaa veriateriansa osana lisääntymisprosessia; lajin koiraat ovat nektavorioisia eikä niillä siten ole osaa siirtosykliin. Ruokintatiheys määräytyy tämän biologisen tarpeen mukaan, joten keskimääräinen ruokintatiheys on yleensä noin kerran neljässä päivässä, ja yleensä oletetaan, että yhden munaerän kylläisyys saavutetaan tämän yhden aterian aikana. On olemassa monia erilaisia malarian, jotkut vaikuttavat ihmisiin (tämä voi johtua yhdestä neljästä eri Plasmodium) ja toiset vaikuttavat eläimiin. Anopheles-suku on vastuussa tarttumisesta ihmisiin, joista noin 30 400: sta lajista aiheuttaa pääasiallisesti tartunnan leviämisen.
keskeinen malariaan vaikuttava piirre on lämpötila; vaikka hyttynen asuisikin annetulla alueella, ulkolämpötilat ovat alle 16C (lauhkea on riippuvainen loislajista), se ei ole tarpeeksi lämmin, jotta se voisi kehittyä. Yleensä, koska lämpötila nousee 16C lyhyempi itämisaika äkkipysähdyksellä yli noin 32C, koska loinen ei pysty selviytymään yli tämän lämpötilan.
Lintumalaria ja Havaijin Hunajamalaria
jotkin järjestelmät saattavat kuitenkin olla paljon monimutkaisempia kuin aiemmin annettu yleinen esimerkki. Yksi tällainen esimerkki on Havaijin Hunajakennomalaria (Drepanididae); se ei kärsi ainoastaan hyttysen (Culex quinquefasciatus) välityksellä leviävän Lintumalarian (Plasmodium relictum) haittavaikutuksista vaan myös ilmastonmuutoksesta ja saalistuksesta. Näiden hallitsevien tekijöiden välinen vuorovaikutus on suuri, sillä lämpötila ja petoeläinten runsaus vaikuttavat taudin kulkuun ja lintujen kykyyn (tai kykyyn) vastustaa sukupuuttoa. Lisäksi joillakin hunajakennon lajeilla on kyky antaa vastustuskykyä malarialle, sillä ne eivät kärsi taudin haitallisista vaikutuksista samalla kun ne pysyvät tarttuvina (näitä kutsutaan yleisemmin taudinkantajiksi ja aiheuttavat tahattomasti infektiosäiliön selviytymällä normaalista ”taudista vapaasta” eliniästä mutta levittämällä tartuntaa.
Tämä teos on julkaistu nimellä:
K. S. Rock et al. ”Modelling the Future of the Hawaiian Honeycreeper: an Ecological and Epidemiological Problem”. Ecological Modelling (kesäkuu 2012)