determinarea anumitor parametri, cum ar fi dimensiunea, lungimea și unghiul la scară atomică, nu este ușoară. Datorită importanței acestor parametri, oamenii de știință au dezvoltat metode pentru a deduce sau calcula parametrii la nivel atomic. Ordinea legăturii și lungimea legăturii sunt doi parametri atât de importanți care indică tipul și puterea legăturilor dintre o pereche de atomi.
Acest articol explică,
1. Care sunt ordinea legăturii și lungimea legăturii
2. Cum se calculează ordinea obligațiunilor și lungimea obligațiunilor– cum se calculează ordinea obligațiunilor– cum se calculează lungimea obligațiunilor
care sunt ordinea obligațiunilor și lungimea obligațiunilor
lungimea obligațiunilor și ordinea obligațiunilor sunt doi parametri care sunt asociați cu legăturile covalente. Ordinea legăturii este numărul de legături chimice dintre doi atomi, iar lungimea legăturii este distanța dintre doi nuclei de atomi care sunt legați covalent împreună. Acest articol explică cum se calculează ordinea legăturii și lungimea legăturii la un nivel atomic.
cum se calculează ordinea legăturii
ordinea legăturii este numărul de legături chimice dintre doi atomi. Aceasta indică stabilitatea unei legături. În legăturile covalente, ordinea legăturii este numărul de electroni împărțiți. De exemplu, ordinea de legătură a unei perechi de atomi legați de o singură legătură este una, în timp ce ordinea de legătură a unei perechi de atomi legați de o legătură dublă este de două. Ordinea legăturii Zero indică faptul că nu există nicio legătură între atomi. Stabilitatea unei molecule crește odată cu creșterea ordinii de legătură. Moleculele cu legătură de rezonanță nu trebuie să fie un număr întreg. În compușii covalenți cu doi atomi, ordinea legăturii dintre o pereche de atomi este determinată mai întâi prin desenarea structurii Lewis și apoi prin determinarea tipului de legături dintre atomi – legătură zero, legătură unică, dublă sau triplă. De exemplu, ordinea de legătură a hidrogenului gazos este determinată după cum urmează.
- desenați structura Lewis
H: H
- determinați numărul de legături/pereche de electroni de valență
o pereche de electroni, prin urmare ordinea legăturii este 1.
dacă există mai mult de doi atomi, ordinea legăturii este determinată după cum urmează. Vezi exemplul: Ion nitrat.
- desenați structura Lewis
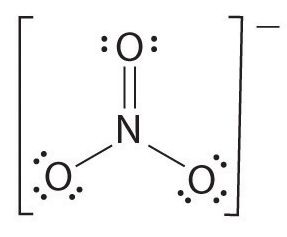
- numărați numărul total de legături (în funcție de ionul nitrat, 4)
- numărul de grupuri de legături între atomii individuali (conform amoniacului, its 3)
- prin urmare, ordinea legăturii = numărul total de legături/ numărul de grupuri de legături
= 4/3
= 1,33
prin urmare, ordinea legăturii ionului nitrat este 1.33
cum se calculează lungimea legăturii
lungimea legăturii este distanța dintre doi nuclei de atomi care sunt legați covalent împreună. Lungimea legăturii este de obicei cuprinsă între 0,1 și 0,2 nm. Când doi atomi similari sunt legați împreună, jumătate din lungimea legăturii este denumită rază covalentă. Lungimea legăturii depinde de numărul de electroni legați de doi atomi sau de ordinea legăturii. Mai mare ordinea legăturii, mai scurtă lungimea legăturii se va datora forțelor puternice de tragere a nucleelor încărcate pozitiv. Unitatea de lungime a legăturii este picometru. În legături simple, duble și triple, lungimea legăturii crește în ordinea
legătură triplă<legătură dublă<legătură unică
electronegativitatea poate fi utilizată pentru a calcula lungimea legăturii între doi atomi cu electronegativități diferite. Următoarea formulă empirică a fost propusă de Shoemaker și Stevenson pentru a calcula lungimea legăturii.
dA-B = rA + rB – 0.09(xA – xB)
dA-b este distanța legăturii dintre doi atomi a și b, rA și rB sunt raze covalente ale lui a și B și
(xA – xB) este diferența de electronegativitate dintre a și B.
o altă metodă este utilizată pentru a calcula lungimea aproximativă a legăturii. În această metodă, prima structură Lewis este trasată pentru a determina tipul legăturii covalente. Apoi, folosind o diagramă * realizat pe studiile efectuate de Cordero și colab., și Pyykk XV și Atsumi, sunt determinate razele corespunzătoare ale legăturilor făcute de fiecare atom. Apoi, lungimea legăturii este determinată luând suma celor două raze. De exemplu, atunci când se determină lungimea legăturii dioxidului de carbon, se trasează prima structură Lewis.
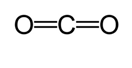
conform graficului, raza covalentă a dublei legături de carbon este de 67 picometri, iar cea a dublei legături de oxigen este de 57 picometri. Prin urmare, lungimea legăturii dioxidului de carbon este de aproximativ 124 picometri (57 pm+ 67 pm).
*diagrama covalentă se găsește aici
referință:
Cordero, Beatriz și colab. „Razele covalente revizuite.”Tranzacții Dalton 21 (2008): 2832-2838.
librete. „Ordinea Bond și lungimi.”Librete De Chimie. Libretexte, 05 Decembrie. 2016. Web. 10 ianuarie. 2017.Lister, Ted și Janet Renshaw. Înțelegerea chimie pentru Nivel avansat. N. p.: Nelson Thornes, 2000. Print.
Pratiyogita Darpan. „Proprietățile elementelor în raport cu structura lor Electronică .”Concurență Știință Viziune Aug. 1998: n.pag. Print.
Pyykk, Pekka și Michiko Atsumi. „Raze covalente moleculare cu dublă legătură pentru elementele Li–E112.”Chimie-O Revistă Europeană 15.46 (2009): 12770-12779.
![]()