câtă energie este eliberată în hidroliza ATP?
modul cititor
ATP este adesea denumit moneda energetică a celulei. Sute de reacții din celulă de la transformările metabolice la evenimentele de semnalizare sunt cuplate la hidroliza (literalmente însemnând „slăbirea apei”) a ATP de apă . Reacția ATP + H2O <> ADP + Pi transformă adenozin trifosfatul (ATP) în adenozin difosfat (ADP) și fosfat anorganic (Pi). Schimbarea energiei libere asociată cu această reacție conduce o mare parte din reacțiile celulare cu potențialul membranei și reducerea puterii fiind celelalte două surse de energie dominante. Dar exact cât valorează această monedă energetică și ce dezvăluie despre tranzacțiile chimice care pot fi achiziționate? Desigur, nu există un răspuns la această întrebare, deoarece cantitatea de energie eliberată de această reacție de hidroliză depinde de condițiile intracelulare, dar este posibil să obțineți un sentiment pentru „valoarea” aproximativă a acestei monede prin recurgerea la câteva estimări simple.

Figura 1: relația energiei libere Gibbs a hidrolizei ATP în condiții standard cu constanta de echilibru și relația energiei libere a hidrolizei în condiții fiziologice cu concentrațiile reactanților fiziologici.
variația energiei libere Gibbs (ECTA) datorată hidrolizei ATP depinde de concentrațiile diferiților participanți la reacție, așa cum este descris în Figura 1. Atunci când concentrațiile sunt mai îndepărtate de valorile lor de echilibru, valoarea absolută a lui ECUG este mai mare. În condiții „standard” (i. e. 1m pentru toți reactanții, cu excepția apei, care este luată la concentrația sa caracteristică de 55M) energia liberă Gibbs a hidrolizei ATP variază de la -28 la -34 kJ/mol (adică 12 KBT, BNID 101989) în funcție de concentrația cationului Mg2+. Dependența de ionii Mg apare deoarece ionii de magneziu încărcați pozitiv ajută la stabilizarea moleculei ATP. Cu toate acestea, în celulă condițiile nu sunt niciodată apropiate de valorile standard de stare. De exemplu, o concentrație de 1m ATP ar însemna că masa solutului ar fi similară cu cea a solventului de apă în sine. În Figura 1 se arată derivarea adesea confuză a energiei libere fiziologice (HECTOG), dată fiind raportul concentrațiilor față de valoarea standard (Octoggo). Împărțirea prin termeni precum sunt necesari pentru a avea grijă de unități, deoarece un logaritm ar trebui să conțină întotdeauna un termen fără unitate. Uneori este surprinzător să ne gândim că, dacă celula ar fi în echilibru, valoarea lui ECUG ar fi fost zero și nu ar exista energie de câștigat prin hidroliza ATP. Din fericire, acest lucru nu este niciodată cazul organismelor vii. .
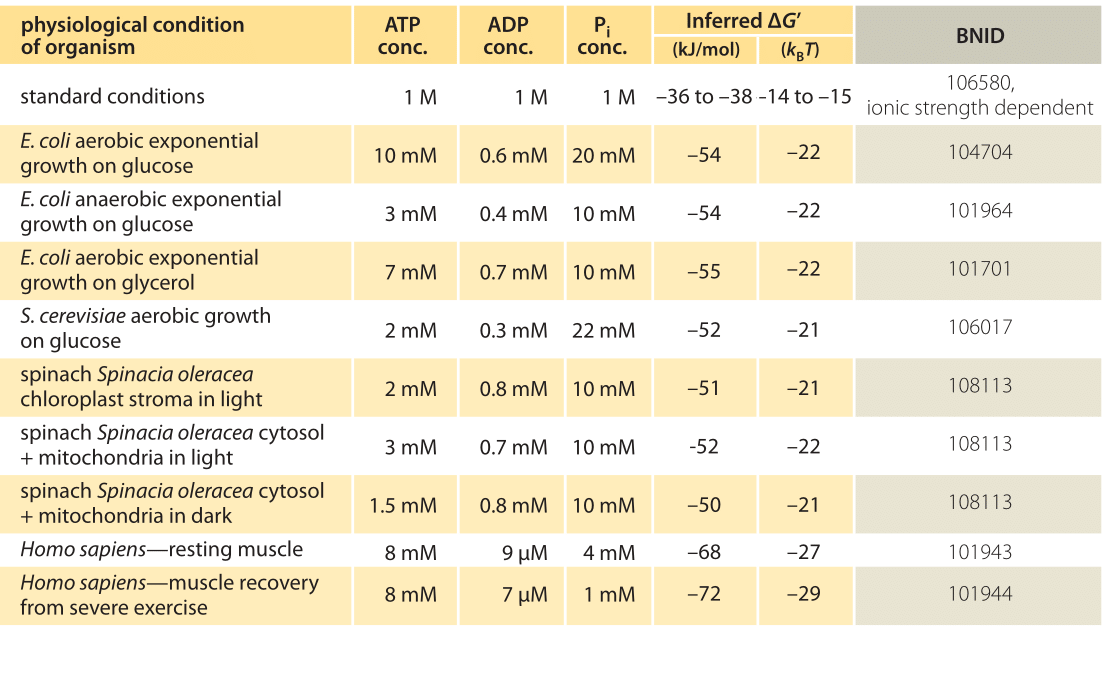
Tabelul 1: Energie liberă pentru hidroliza ATP în diferite organisme și în diferite condiții fiziologice. S-au dedus calcule de la valoarea de -37,6 kJ/mol a lui hectar’ 0 pe baza unei valori de -37,6 kJ / mol. Acest lucru face ca valorile tabelului să fie consecvente între ele, dar creează mici abateri de la valorile de la 7GF raportat în sursele primare. Astfel de abateri pot rezulta din variații ale rezistenței ionice, ale pH-ului și ale metodelor de măsurare prejudecăți. Valorile sunt rotunjite la una sau două cifre semnificative. La spanac, unde concentrația Pi nu a fost raportată, a fost utilizată o valoare caracteristică de 10 mM (BNID 103984, 103983, 111358, 105540).
în practică, condițiile fiziologice depind de organismul studiat, de țesutul sau compartimentul din interiorul celulei luate în considerare și de cerințele actuale de energie pentru reacții metabolice și alte reacții. De exemplu, în ficatul de șobolan perfuzat, raportul ATP-ADP s-a dovedit a fi de aproximativ 10:1 în citosol, dar 1:10 în mitocondrii sub rate ridicate de glicoliză și sub rate scăzute de glicoliză, ambele rapoarte au fost mult apropiate de 1 (BNID 111357). Prin urmare, se preconizează un interval de valori pentru cantitatea de oxid nitric. Cheia pentru înțelegerea acestui interval este de a înțelege cât de mult Q diferă de K, adică cum diferă concentrațiile de condițiile standard. Concentrațiile intracelulare tipice ale tuturor componentelor relevante (ATP, ADP și Pi) sunt în intervalul mM, mult mai mici decât condițiile standard. Raportul / cu concentrații în intervalul mM este mult mai mic decât unul, iar reacția va fi energetic mai favorabilă decât în condiții standard, așa cum se arată în tabelul 1. Cea mai mare valoare a cifrei de afaceri -70 kJ/mol (30kbt) a fost calculată pe baza valorilor din mușchiul uman al sportivilor care se recuperează în urma efortului fizic (BNID 101944). În celulele E. coli care cresc pe glucoză, a fost raportată o valoare de -47 kJ/mol (20kbt, BNID 101964). Pentru a pune aceste numere în perspectivă, un motor molecular care exercită o forță de aproximativ 5 pN (BNID 101832) peste o dimensiune de pas de 10 nm (BNID 101857) funcționează de ordinul 50 PN nm, necesitând puțin mai mult de 10 kBT de energie, bine în intervalul a ceea ce poate furniza un singur ATP.
calculele pentru cantitatea de HECTOLITRINĂ necesită o măsurare exactă a concentrațiilor intracelulare relevante. Astfel de concentrații sunt măsurate in vivo la om prin utilizarea rezonanței magnetice nucleare. Forma naturală a fosforului (31P) are proprietăți magnetice, deci nu este nevoie să adăugați nicio substanță externă. Țesutul de interes, cum ar fi mușchiul, este plasat într-un câmp magnetic puternic și schimbările de frecvență ale impulsurilor radio sunt utilizate pentru a deduce concentrația de ATP și Pi direct din vârfurile spectrelor RMN. În E. coli, concentrațiile de ATP pot fi măsurate mai direct cu un test de bioluminescență ATP. Un eșantion de bacterii în creștere eliminate din cultură poate fi testat folosind luciferaza, o proteină din bacteriile care trăiesc în simbioză cu calmarii, dar care s-a alăturat până acum setului de instrumente al biologilor ca reporter molecular. Enzima luciferază folosește ATP într-o reacție care produce lumină care poate fi măsurată folosind un luminometru, iar concentrația ATP poate fi dedusă din puterea semnalului. Deci avem conținutul celulei ca intrare, luciferaza ca „dispozitiv” care transformă cantitatea de ATP în emisie de lumină care servește ca ieșire măsurată. Folosind instrumente precum acestea, se constată că în „viața reală” ATP valorează aproximativ de două ori mai mult decât în condiții „standard”, din cauza concentrațiilor fiind mai favorabile pentru reacția înainte.
terminăm observând că este o întrebare permanentă cu privire la motivul pentru care nucleotida adenină a fost desemnată pentru a servi drept monedă principală de energie cu GTP și celelalte nucleotide care servesc roluri mult mai minore. Este un caz de alegere aleatorie care mai târziu a devenit „accident înghețat” sau a existat un avantaj selectiv pentru ATP față de GTP, CTP, UTP și TTP?




