określenie pewnych parametrów, takich jak rozmiar, długość i kąt w skali atomowej, nie jest łatwe. Ze względu na istotne z tych parametrów naukowcy opracowali metody dedukcji lub obliczenia parametrów na poziomie atomowym. Porządek wiązania i długość wiązania są dwoma tak ważnymi parametrami, które wskazują na rodzaj i siłę wiązań między parą atomów.
Ten artykuł wyjaśnia,
1. Czym jest kolejność wiązania i długość wiązania
2. Jak obliczyć kolejność obligacji i długość obligacji
– Jak obliczyć kolejność obligacji
– Jak obliczyć długość obligacji
czym są kolejność obligacji i długość obligacji
Długość obligacji i kolejność obligacji to dwa parametry, które są związane z wiązaniami kowalencyjnymi. Porządek wiązania to liczba wiązań chemicznych między dwoma atomami, a długość wiązania to odległość między dwoma jądrami atomów, które są kowalencyjnie połączone ze sobą. W tym artykule wyjaśniono, jak obliczyć kolejność wiązania i długość wiązania na poziomie atomowym.
Jak obliczyć kolejność wiązania
kolejność wiązania to liczba wiązań chemicznych między dwoma atomami. Oznacza stabilność wiązania. W wiązaniach kowalencyjnych porządek wiązań jest liczbą współdzielonych elektronów. Na przykład, kolejność wiązania pary atomów związanych pojedynczym wiązaniem jest jedna, podczas gdy kolejność wiązania pary atomów związanych podwójnym wiązaniem jest dwa. Zerowy porządek wiązań wskazuje, że nie ma wiązania między atomami. Stabilność cząsteczki wzrasta wraz ze wzrostem rzędu wiązania. Cząsteczki z wiązaniem rezonansowym nie muszą być liczbą całkowitą. W związkach kowalencyjnych z dwoma atomami porządek wiązań między parą atomów określa się najpierw rysując strukturę Lewisa, a następnie określając rodzaj wiązań między atomami-Wiązanie zerowe, Wiązanie pojedyncze, podwójne lub potrójne. Na przykład kolejność wiązania gazu wodorowego określa się w następujący sposób.
- narysuj strukturę Lewisa
H: H
- określ liczbę wiązań/parę elektronów walencyjnych
Jedna para elektronów, stąd kolejność wiązań wynosi 1.
Jeśli istnieje więcej niż dwa atomy, kolejność wiązania określa się w następujący sposób. Zobacz przykład: jon azotanowy.
- narysuj strukturę Lewisa
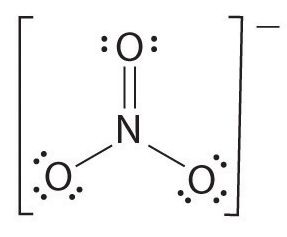
- Policz całkowitą liczbę wiązań (według jonu azotanowego, jego 4)
- liczba
- w związku z tym kolejność wiązań = całkowita liczba wiązań/liczba grup wiązań
= 4/3
= 1,33
w związku z tym kolejność wiązań jonów azotanowych wynosi 1.33
Jak obliczyć długość wiązania
długość wiązania to odległość między dwoma jądrami atomów, które są kowalencyjnie połączone ze sobą. Długość wiązania zwykle mieści się w zakresie od 0,1 do 0,2 nm. Gdy dwa podobne atomy są połączone ze sobą, połowa długości wiązania jest określana jako promień kowalencyjny. Długość wiązania zależy od liczby połączonych elektronów dwóch atomów lub kolejności wiązania. Wyższa kolejność wiązania, krótsza długość wiązania będzie spowodowana silnymi siłami ciągnącymi dodatnio naładowanych jąder. Jednostką długości wiązania jest pikometr. W wiązaniach pojedynczych, podwójnych i potrójnych długość wiązania wzrasta w kolejności
wiązania potrójnego<wiązania podwójnego<wiązania pojedynczego
elektroujemność może być wykorzystana do obliczenia długości wiązania między dwoma atomami o różnej elektroujemności. Następujący wzór empiryczny został zaproponowany przez Shoemakera i Stevensona do obliczenia długości wiązania.
dA-B = rA + RB – 0.09(xA – xB)
dA-B to odległość wiązania między dwoma atomami a i B, rA i rB to promienie kowalencyjne A i B, A
(xA – xB) to różnica elektroujemności między A I B.
do obliczenia przybliżonej długości wiązania stosuje się inną metodę. W tej metodzie rysuje się pierwszą strukturę Lewisa w celu określenia typu wiązania kowalencyjnego. Następnie za pomocą wykresu * wykonane na badaniach wykonanych przez Cordero et al., oraz Pyykkö i Atsumi, określa się odpowiednie promienie wiązań wytworzonych przez każdy atom. Następnie długość wiązania jest określana przez wzięcie sumy dwóch promieni. Na przykład przy wyznaczaniu długości wiązania dwutlenku węgla rysowana jest pierwsza struktura Lewisa.
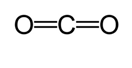
zgodnie z wykresem promień kowalencyjny wiązania podwójnego węgla wynosi 67 pikometrów, a promień wiązania podwójnego tlenu wynosi 57 pikometrów. Dlatego długość wiązania dwutlenku węgla wynosi około 124 piksometrów (57 pm+ 67 pm).
*Wykres kowalencyjny znajduje się tutaj
odniesienie:
Cordero, Beatriz, et al. „Covalent radii revisited.”Dalton Transactions 21 (2008): 2832-2838.
Librettexts. „Kolejność i długości obligacji.”Chemistry LibreTexts. Librettexts, 05.12.2010 2016. Www. 10 sty 2017.
Lister, Ted i Janet Renshaw. Zrozumienie chemii na poziomie zaawansowanym. N. P.: Nelson Thornes, 2000. Druk.
Pratiyogita Darpan. „Właściwości elementów w stosunku do ich struktury elektronicznej .”Konkurs Nauka Wizja Sierpień 1998: N. pag. Druk.
Pyykkö, Pekka i Michiko Atsumi. „Molekularne wiązania podwójne kowalencyjne promienie dla pierwiastków Li–E112.”Chemistry–A European Journal 15.46 (2009): 12770-12779.
![]()