Generisk Navn: Terbutaline sulfate
Doseringsform: injeksjon, løsning
Medisinsk anmeldt Av Drugs.com. sist oppdatert Sep 1, 2020.
- Oversikt
- Dosering
- Profesjonell
- Interaksjoner
- Mer
en steril vandig løsning for subkutan injeksjon
Rx Only
ADVARSEL: LANGVARIG TOCOLYSIS
Terbutalinsulfat er ikke godkjent og bør ikke brukes til langvarig tocolysis (utover 48-72 timer). Spesielt Bør Terbutalinsulfat ikke brukes til vedlikeholdstokolyse i ambulant eller hjemmeinnstilling. Alvorlige bivirkninger, inkludert død, er rapportert etter administrering Av Terbutalinsulfat til gravide kvinner. I moren inkluderer disse bivirkningene økt hjertefrekvens, forbigående hyperglykemi, hypokalemi, hjertearytmier, lungeødem og myokardisk iskemi. Økt føtal hjertefrekvens og neonatal hypoglykemi kan oppstå som følge av mors administrasjon(SE KONTRAINDIKASJONER: Langvarig Tokolyse).
- Terbutalin Beskrivelse
- Terbutalin-Klinisk Farmakologi
- Prekliniske
- Farmakokinetikk
- Indikasjoner og Bruk For Terbutalin
- Kontraindikasjoner
- Advarsler
- Forverring Av Astma
- Bruk av Antiinflammatoriske Midler
- Kardiovaskulære Effekter
- Anfall
- Forholdsregler
- Generelt
- Legemiddelinteraksjoner
- Karsinogenese, Mutagenese, Nedsatt Fertilitet
- Graviditet-Teratogene Effekter
- Bruk Ved Fødsel
- Ammende Mødre
- Pediatrisk Bruk
- Geriatrisk Bruk
- Bivirkninger
- Overdosering
- Terbutalin Dosering og Administrasjon
- Hvordan Leveres Terbutalin
- HOVED SKJERM PANEL
- principal display panel
- SERIALIZATION IMAGE
- Mer om terbutalin
- Forbruker ressurser
- Faglige ressurser
- relaterte behandlingsveiledninger
Terbutalin Beskrivelse
TERBUTALINSULFAT, USP, Den aktive ingrediensen I Terbutalinsulfatinjeksjon, USP, ER en beta-adrenerg agonistbronkodilator tilgjengelig som en steril, ikke-pyrogen, vandig løsning i hetteglass, for subkutan administrering. Hver milliliter oppløsning inneholder 1 mg Terbutalinsulfat, USP (0,82 mg fri base), natriumklorid for isotonisitet, 0,055% edetat dinatriumdihydrat som stabiliseringsmiddel og saltsyre for justering til en mål pH på 4. Terbutalinsulfat er (±) – a–3,5-dihydroxybenzyI alkoholsulfat (2:1) (salt). Molekylformelen er (C12H19N03) 2•H2SO4 og strukturformelen er:
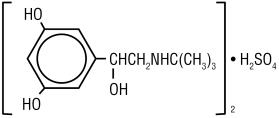
Terbutalinsulfat, USP er et hvitt til gråhvitt krystallinsk pulver. Det er luktfritt eller har en svak lukt av eddiksyre. Det er løselig i vann og i 0,1 n saltsyre, litt løselig i metanol og uoppløselig i kloroform. Dens molekylvekt er 548,65.
Terbutalin-Klinisk Farmakologi
Terbutalinsulfat injeksjon er en beta-adrenerg reseptoragonist. In vitro og in vivo farmakologiske studier har vist At Terbutalin har en fortrinnsvirkning på beta2‑adrenerge reseptorer. Mens det er anerkjent at beta2-adrenerge reseptorer er de dominerende reseptorene i bronkial glatt muskel, indikerer data at det er en populasjon av beta2-reseptorer i det menneskelige hjerte, som eksisterer i en konsentrasjon mellom 10% til 50%. Den nøyaktige funksjonen til disse reseptorene er ikke fastslått (SE ADVARSLER). Kontrollerte kliniske studier hos Pasienter Gitt Terbutalin subkutant har ikke vist en fortrinnsrett beta2-adrenerg effekt.
de farmakologiske effektene av beta-adrenerge agonister, inkludert Terbutalin, skyldes i det minste delvis stimulering via beta-adrenerge reseptorer av intracellulær adenylcyklase, enzymet som katalyserer omdannelsen av adenosintrifosfat (ATP) til syklisk 3′,5′-adenosinmonofosfat (cAMP). Økte cAMP-nivåer er forbundet med avslapning av glatt muskulatur i bronkiene og hemming av frigjøring av mediatorer med umiddelbar overfølsomhet fra celler, spesielt fra mastceller.Kontrollerte kliniske studier har vist At Terbutalinsulfatinjeksjon lindrer bronkospasme ved akutt og kronisk obstruktiv lungesykdom ved signifikant økende lungestrømningshastighet (f. eks. en økning på 15% eller mer I FEV1). Etter subkutan administrering av 0,25 mg Terbutalinsulfat injeksjon, skjer en målbar endring i ekspiratorisk strømningshastighet vanligvis innen 5 minutter, og en klinisk signifikant økning I FEV1 oppstår innen 15 minutter. Maksimal effekt oppstår vanligvis innen 30 til 60 minutter, og klinisk signifikant bronkodilatoraktivitet kan fortsette i 1,5 til 4 timer. Varigheten av klinisk signifikant forbedring er sammenlignbar med den som ble observert med equimilligram-doser av epinefrin.
Prekliniske
Studier på laboratoriedyr (minigriser, gnagere og hunder) har vist forekomst av hjertearytmier og plutselig død (med histologiske tegn på myokardnekrose) når beta-agonister og metylxantiner administreres samtidig. Den kliniske signifikansen av disse funnene er ukjent.
Farmakokinetikk
Subkutan administrering av 0,5 mg Terbutalinsulfat til 17 friske, voksne, mannlige forsøkspersoner resulterte i gjennomsnittlig (SD) maksimal plasmakonsentrasjon Av Terbutalin på 9,6 (3,6) ng/mL, som ble observert ved en median (område) tid på 0,5 (0,08 til 1,0) timer etter dosering. Gjennomsnittlig (SD) AUC (0 til 48) og total clearance var henholdsvis 29,4 (14,2) timer•ng/mL og 311 (112) mL/min. Terminal halveringstid ble bestemt hos 9 av de 17 pasientene og hadde et GJENNOMSNITT (SD) på 5,7 (2,0) timer.
etter subkutan administrering av 0,25 mg Terbutalinsulfat til to mannlige individer, ble det observert maksimale Serumkonsentrasjoner Av Terbutalin på 5,2 og 5,3 ng / mL omtrent 20 minutter etter dosering.
eliminasjonshalveringstid av legemidlet hos 10 av 14 pasienter var omtrent 2,9 timer etter subkutan administrering, men lengre eliminasjonshalveringstid (mellom 6 til 14 timer) ble funnet hos de andre 4 pasientene. Omtrent 90% av legemidlet ble utskilt i urinen 96 timer etter subkutan administrering, med omtrent 60% av dette uendret legemiddel. Det ser ut til at sulfatkonjugatet er En hovedmetabolitt Av Terbutalin, og urinutskillelse er den primære eliminasjonsveien.
Indikasjoner og Bruk For Terbutalin
TERBUTALINSULFAT Injeksjon, USP er indisert for forebygging og reversering av bronkospasme hos pasienter 12 år og eldre med astma og reversibel bronkospasme assosiert med bronkitt og emfysem.
Kontraindikasjoner
1. Langvarig Tocolysis
Terbutalinsulfat er ikke godkjent og bør ikke brukes til langvarig tocolysis (utover 48-72 timer). Spesielt Bør Terbutalinsulfat ikke brukes til vedlikeholdstokolyse i poliklinisk eller hjemmeinnstilling (se BOKS ADVARSEL: Langvarig Tokolyse).
2. Hypersensitivitet
Injeksjon Av Terbutalinsulfat er kontraindisert hos pasienter som er kjent for å være overfølsomme for sympatomimetiske aminer eller noen av komponentene i dette legemidlet.
Advarsler
Forverring Av Astma
Astma kan forverres akutt over en periode på timer eller kronisk over flere dager eller lenger. Hvis pasienten trenger flere Doser Terbutalinsulfat enn vanlig, kan dette være en markør for destabilisering av astma og krever revurdering av pasienten og behandlingsregimet, og det tas særlig hensyn til mulig behov for antiinflammatorisk behandling, f.eks. kortikosteroider.
Bruk av Antiinflammatoriske Midler
bruk av bronkodilatatorer med beta-adrenerge agonister alene er kanskje ikke tilstrekkelig til å kontrollere astma hos mange pasienter. Tidlig vurdering bør tas for å tilsette antiinflammatoriske midler, f. eks. kortikosteroider.
Kardiovaskulære Effekter
Terbutalinsulfat, som alle andre beta-adrenerge agonister, kan gi en klinisk signifikant kardiovaskulær effekt hos noen pasienter målt ved pulsfrekvens, blodtrykk og / eller symptomer. Selv om slike effekter er uvanlige etter administrering Av Terbutalinsulfat i anbefalte doser, kan det hende at stoffet må avbrytes hvis de oppstår. I tillegg er det rapportert at beta‑agonister gir endringer i elektrokardiogram (EKG), som utflating Av T-bølgen, forlengelse Av QTc-intervallet og ST-segmentdepresjon. Den kliniske signifikansen av disse funnene er ukjent. Derfor Bør Terbutalinsulfat, som alle sympatomimetiske aminer, brukes med forsiktighet hos pasienter med kardiovaskulære sykdommer, spesielt koronarinsuffisiens, hjertearytmier og hypertensjon.
Anfall
det har vært sjeldne rapporter om anfall hos Pasienter som får Terbutalin; anfall kom ikke tilbake hos disse pasientene etter seponering.
Forholdsregler
Generelt
Terbutalin, som med alle sympatomimetiske aminer, bør brukes med forsiktighet hos pasienter med kardiovaskulære sykdommer, inkludert iskemisk hjertesykdom, hypertensjon og hjertearytmier; hos pasienter med hypertyreose eller diabetes mellitus; og hos pasienter som er uvanlig lydhør overfor sympatomimetiske aminer eller som har konvulsive lidelser. Signifikante endringer i systolisk og diastolisk blodtrykk er sett og kan forventes å forekomme hos noen pasienter etter bruk av en hvilken som helst beta-adrenerg bronkodilator.
Umiddelbare overfølsomhetsreaksjoner og eksaserbasjoner av bronkospasme er rapportert etter Terbutalinadministrasjon.
beta-adrenerge agonistmedikamenter kan gi signifikant hypokalemi hos noen pasienter, muligens gjennom intracellulær bypass operasjon, som har potensial til å gi uønskede kardiovaskulære effekter. Nedgangen er vanligvis forbigående, og krever ikke tilskudd.
Store Doser Av intravenøs Terbutalin har blitt rapportert å forverre eksisterende diabetes mellitus og ketoacidose.
Legemiddelinteraksjoner
samtidig Bruk Av Terbutalinsulfatinjeksjon med andre sympatomimetiske midler anbefales ikke, da den kombinerte effekten på kardiovaskulærsystemet kan være skadelig for pasienten.Monoaminoksidasehemmere Eller Trisykliske Antidepressiva:Terbutalin bør administreres med ekstrem forsiktighet til pasienter som behandles med monoaminoksidasehemmere eller trisykliske antidepressiva, eller innen 2 uker etter seponering av slike midler, da Virkningen Av Terbutalin på det vaskulære systemet kan forsterkes.
Betablokkere: Beta-adrenerge reseptorblokkerende midler blokkerer ikke bare den pulmonale effekten av beta-agonister, slik Som Terbutalinsulfat injeksjon, men kan gi alvorlig bronkospasme hos astmapasienter. Pasienter med astma bør derfor normalt ikke behandles med betablokkere. Under visse omstendigheter, f.eks. som profylakse etter hjerteinfarkt, kan det imidlertid ikke finnes akseptable alternativer til bruk av beta-adrenerge blokkere hos pasienter med astma. I denne situasjonen kan kardioselektive betablokkere vurderes, selv om de bør administreres med forsiktighet.
Diuretika: EKG-forandringer og / eller hypokalemi som kan oppstå ved administrering av ikke-kaliumsparende diuretika (som loop-eller tiaziddiuretika) kan forverres akutt av beta-agonister, spesielt når den anbefalte dosen av beta-agonisten overskrides. Selv om den kliniske signifikansen av disse effektene ikke er kjent, anbefales forsiktighet ved samtidig administrering av beta-agonister og ikke-kaliumsparende diuretika.
Karsinogenese, Mutagenese, Nedsatt Fertilitet
I en 2-årig studie med sprague-Dawley‑rotter forårsaket Terbutalinsulfat en signifikant og doserelatert økning i insidensen av benigne leiomyomer i mesovariet ved diettdoser på 50 mg/kg og over (omtrent 810 ganger maksimal anbefalt daglig subkutan (s.c.) dose for voksne på mg/m2 basis). I en 21-måneders studie med CD-1-mus viste Terbutalinsulfat ingen tegn på tumorigenisitet ved diettdoser opp til 200 mg / kg (omtrent 1600 ganger maksimal anbefalt daglig dose for voksne på mg/m2 basis). Mutagenitetspotensialet Til Terbutalinsulfat er ikke fastslått.Reproduksjonsstudier hos rotter med Terbutalinsulfat viste ingen nedsatt fertilitet ved orale doser opp til 50 mg/kg (omtrent 810 ganger maksimal anbefalt daglig dose for voksne basert på mg / m2).
Graviditet-Teratogene Effekter
Graviditet Kategori C
det er ingen tilstrekkelige og velkontrollerte studier Av Terbutalinsulfat hos gravide kvinner. Publiserte dyrestudier viser at rotteavkom viser endringer i atferd og hjerneutvikling, inkludert redusert celleproliferasjon og differensiering når dammer ble behandlet subkutant med Terbutalin i sent stadium av graviditet og amming. Terbutalineksponeringer i rottedammer var omtrent 24 til 48 ganger den vanlige humane dosen hos voksne på 2-4 mg / dag, basert på mg / m2.
Terbutalinsulfat er ikke godkjent og bør ikke brukes til langvarig tokolyse (utover 48-72 timer). Spesielt Bør Terbutalinsulfat ikke brukes til vedlikeholdstokolyse i ambulant eller hjemmeinnstilling. Alvorlige bivirkninger, inkludert død, er rapportert etter administrering Av Terbutalinsulfat til gravide kvinner. I moren inkluderer disse bivirkningene økt hjertefrekvens, forbigående hyperglykemi, hypokalemi, hjertearytmier, lungeødem og myokardisk iskemi. Økt føtal hjertefrekvens og neonatal hypoglykemi kan oppstå som følge av mors administrasjon( se BOKS ADVARSEL: Langvarig Tokolyse og KONTRAINDIKASJONER: Langvarig Tokolyse).
i embryoføtale utviklingsstudier hos dyr ble det ikke observert teratogene effekter hos avkom når drektige rotter og kaniner fikk Terbutalinsulfat ved orale doser opp til 50 mg/kg/dag, henholdsvis ca. 810 og 1600 ganger den maksimale anbefalte daglige subkutane dosen for voksne, basert på mg / m2.Terbutalinsulfat bør kun brukes under graviditet dersom de potensielle fordelene begrunner den potensielle risikoen for fosteret.
Bruk Ved Fødsel
På grunn av muligheten for betaagonistinterferens med livmorkontraktilitet, bør Bruk Av Terbutalinsulfat til lindring av bronkospasme under fødsel begrenses til de pasientene hvor nytten klart oppveier risikoen.
Terbutalin krysser morkaken. Etter enkeltdose I. v. administrering Av Terbutalin til 22 kvinner i sen graviditet som ble Gitt ved elektiv Keisersnitt på grunn av kliniske årsaker, ble umbilical blodnivåer Av Terbutalin funnet å variere fra 11% til 48% av mors blodnivåer.
Ammende Mødre
det er ikke kjent om dette legemidlet utskilles i morsmelk. Derfor Bør Terbutalinsulfatinjeksjon kun brukes under amming dersom den potensielle fordelen begrunner den mulige risikoen for nyfødte.
Pediatrisk Bruk
terbutalinsulfatinjeksjon anbefales ikke til pasienter under 12 år på grunn av utilstrekkelige kliniske data for å fastslå sikkerhet og effektivitet.
Geriatrisk Bruk
Kliniske studier av Terbutalinsulfatinjeksjon inkluderte ikke tilstrekkelig antall forsøkspersoner i alderen 65 år og eldre til å avgjøre om de responderer annerledes enn yngre forsøkspersoner. Annen rapportert klinisk erfaring har ikke identifisert forskjeller i respons mellom eldre og yngre pasienter. Generelt bør dosevalg for eldre pasienter være forsiktig, vanligvis ved den lave enden av doseringsområdet, noe som gjenspeiler den større frekvensen av nedsatt lever -, nyre-eller hjertefunksjon, og samtidig sykdom eller annen legemiddelbehandling.
Bivirkninger
Bivirkninger observert Med Terbutalinsulfat injeksjon er lik de som vanligvis ses med andre sympatomimetiske midler. Alle disse reaksjonene er forbigående og krever vanligvis ikke behandling.tabellen nedenfor sammenligner bivirkninger sett hos pasienter behandlet Med Terbutalinsulfat (0,25 mg og 0,5 mg), med de sett hos pasienter behandlet med adrenalin (0,25 mg og 0,5 mg), i åtte dobbeltblinde crossover-studier med totalt 214 pasienter.
| Incidence (%) of Adverse Reactions | |||||
| Terbutaline (%) | Epinephrine (%) | ||||
|
0.25 mg |
0.5 mg N = 205 |
0.25 mg N = 153 |
0.5 mg N = 61 |
||
| Reaction Central Nervous System |
|||||
| Tremor | 7.8 | 38.0 | 16.3 | 18.0 | |
| Nervousness | 16.9 | 30.7 | 8.5 | 31.1 | |
| Dizziness | 1.3 | 10.2 | 7.8 | 3.3 | |
| Headache | 7.8 | 8.8 | 3.3 | 9.8 | |
| Drowsiness | 11.7 | 9.8 | 14.4 | 8.2 | |
| Cardiovascular | |||||
| Palpitations | 7.8 | 22.9 | 7.8 | 29.5 | |
| Tachycardia | 1.3 | 1.5 | 2.6 | 0.0 | |
| Respiratory | |||||
| Dyspnea | 0.0 | 2.0 | 2.0 | 0.0 | |
| Chest discomfort | 1.3 | 1.5 | 2.6 | 0.0 | |
| Gastrointestinal | |||||
| Nausea/vomiting | 1.3 | 3.9 | 1.3 | 11.5 | |
| Systemic | |||||
| Weakness | 1.3 | 0.5 | 2.6 | 1.6 | |
| Flushed feeling | 0.0 | 2.4 | 1.3 | 0.0 | |
| Sweating | 0.0 | 2.4 | 0.0 | 0.0 | |
| Pain at injection site | 2.6 | 0.5 | 2.6 | 1.6 | |
Merk: noen pasienter fikk mer enn en doseringsstyrke av terbutalinsulfat og epinefrin. I tillegg var det rapporter om angst, muskelkramper og tørr munn (< 0,5%). Det har vært sjeldne rapporter om forhøyede leverenzymer og hypersensitivitetsvaskulitt ved Bruk Av Terbutalin.
for å rapportere MISTENKTE BIVIRKNINGER, kontakt Hikma Pharmaceuticals USA Inc.. på 1-877-233-2001, ELLER FDA på 1-800-FDA-1088 eller www.fda.gov/medwatch
Overdosering
median dødelig dose Terbutalinsulfat i modne rotter var omtrent 165 mg/kg (omtrent 2700 ganger maksimal anbefalt daglig dose for voksne basert på mg / m2). Median dødelig dose Terbutalinsulfat i sc hos unge rotter var omtrent 2000 mg/kg (omtrent 32000 ganger maksimal anbefalt daglig dose for voksne basert på mg / m2).
de forventede symptomene ved overdosering er de som skyldes overdreven beta-adrenerg stimulering og / eller forekomst eller overdrivelse av noen av symptomene listet under BIVIRKNINGER, f.eks. kramper, angina, hypertensjon eller hypotensjon, takykardi med hastigheter opptil 200 slag per minutt, arytmier, nervøsitet, hodepine, tremor, tørr munn, hjertebank, kvalme, svimmelhet, tretthet, utilpasshet og søvnløshet. Hypokalemi kan også forekomme. Det er ingen spesifikk motgift. Behandlingen består av seponering Av Terbutalinsulfatinjeksjon sammen med passende symptomatisk behandling. Den fornuftige bruken av en kardioselektiv beta-reseptorblokker kan vurderes, med tanke på at slik medisinering kan produsere bronkospasme. Det er ikke tilstrekkelig bevis for å avgjøre om dialyse er gunstig for overdosering Av Terbutalinsulfat injeksjon.
Terbutalin Dosering og Administrasjon
Hetteglass skal kun brukes til subkutan administrering og ikke intravenøs infusjon.
Sterilitet og nøyaktig dosering kan ikke garanteres hvis hetteglassene ikke brukes I HENHOLD TIL DOSERING og ADMINISTRASJON.
kast ubrukt porsjon etter bruk av en enkelt pasient.
Den vanlige subkutane dosen Terbutalinsulfatinjeksjon er 0,25 mg injisert i det laterale deltoidområdet. Hvis signifikant klinisk forbedring ikke forekommer innen 15 til 30 minutter, kan en andre dose på 0,25 mg gis. Hvis pasienten ikke responderer innen ytterligere 15 til 30 minutter, bør andre terapeutiske tiltak vurderes. Den totale dosen innen 4 timer bør ikke overstige 0,5 mg.
Merk: Parenterale legemidler bør inspiseres visuelt for partikler og misfarging før administrering, når oppløsning og beholder tillater det.
Hvordan Leveres Terbutalin
Terbutalinsulfatinjeksjon, USP, 1 mg/mL, leveres i et volum på 1 mL i et 2 mL gult hetteglass. Hvert hetteglass inneholder 1 mg Terbutalinsulfat per 1 mL oppløsning; 0,25 mL oppløsning vil gi den vanlige kliniske dosen på 0,25 mg.
NDC 0143-9375-10 Eske med 10 hetteglass.
Oppbevares fra 20° til 25°C (68° til 77°F).
Beskytt mot lys ved å oppbevare hetteglassene i originalemballasjen til de er utlevert.
skal ikke brukes hvis oppløsningen er misfarget.
kast ubrukt porsjon etter bruk av en enkelt pasient.
Produsert av:
HIKMA FARMACÊUTICA (PORTUGAL), S. A..
Generelt Om Rio Da Mó, nº 8, 8a e 8b-Fervenç,
2705 – 906 Terrugem SNT,
PORTUGAL
Distribuert av:
Hikma Pharmaceuticals USA Inc.
Eatontown, NJ 07724 USA
Novaplus Er et registrert varemerke for Vizient, Inc.
Revidert: Oktober 2020
PIN552-NOV/2
HOVED SKJERM PANEL
NDC 0143-9375-01 RX BARE
Terbutalin
SULFAT
INJEKSJON, USP
1 mg/mL
FOR SUBKUTAN
BRUK BARE

principal display panel
ndc 0143-9375-10 rx bare
TERBUTALIN
sulfat
INJEKSJON, usp
1 mg/ml
for subkutan
Bruk Bare
10 x 1 ML ENKELTDOSE HETTEGLASS
steril, nonpyrogen, vandig
oppløsning FOR SUBKUTAN INJEKSJON.
IKKE BRUK HVIS OPPLØSNINGEN ER MISFARGET.
MERK: VANLIG ENKELTDOSE ER EN FJERDEDEL
AV HETTEGLASSETS INNHOLD. SEE PRESCRIBING
INFORMATION.
SERIALIZATION IMAGE
| Terbutaline SULFATE Terbutaline sulfate injection |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
Labeler – Hikma Pharmaceuticals USA Inc. (001230762)
Registrant – HIKMA FARMACEUTICA (PORTUGAL), S. a. (452742943)
Mer om terbutalin
- Bivirkninger
- Under Graviditet eller Amming
- Doseringsinformasjon
- Legemiddelbilder
- Legemiddelinteraksjoner
- Sammenlign Alternativer
- Priser& Kuponger
- På engelsk
- 11 anmeldelser
- legemiddelklasse: adrenerge bronkodilatorer
- FDA Varsler (1)
Forbruker ressurser
- Pasientinformasjon
- Terbutalin (Avansert Lesing)
- Terbutalin Subkutan (Avansert Lesing)
Faglige ressurser
- Forskrivningsinformasjon
- Terbutalin (Profesjonell Pasient Råd)
- Terbutalin Tabletter (fda)
relaterte behandlingsveiledninger
- For tidlig fødsel
- allergisk astma
- astma, vedlikehold
- astma, akutt
medisinsk ansvarsfraskrivelse