VIVO Patofysiologi
Insulin Syntese og Sekresjon
Insulin Er et lite protein, med en molekylvekt på ca 6000 Dalton. Den består av to kjeder holdt sammen av disulfidbindinger. Figuren til høyre viser en molekylær modell av bovint insulin, Med a-kjeden farget blå og den større b-kjeden grønn. Du kan få en bedre forståelse for strukturen av insulin ved å manipulere en slik modell selv.aminosyresekvensen er sterkt konservert blant virveldyr, og insulin fra ett pattedyr er nesten helt sikkert biologisk aktivt i et annet. Selv i dag behandles mange diabetespasienter med insulin ekstrahert fra grispankreas.
Biosyntese Av Insulin
Insulin syntetiseres i betydelige mengder bare i beta-celler i bukspyttkjertelen. Insulin mRNA er oversatt som en enkeltkjedeforløper kalt preproinsulin, og fjerning av signalpeptidet under innføring i endoplasmatisk retikulum genererer proinsulin.
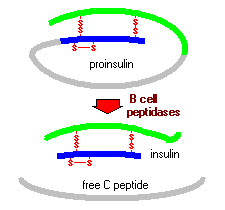 Proinsulin består av tre domener: en aminoterminal b-kjede, en karboksyterminal a-kjede og et forbindelsespeptid i midten kjent som C-peptidet. Innenfor endoplasmatisk retikulum, er proinsulin utsatt for flere spesifikke endopeptidaser som excise c peptid, og dermed generere moden form av insulin. Insulin og fritt c-peptid pakkes I Golgi til sekretoriske granulater som akkumuleres i cytoplasma.
Proinsulin består av tre domener: en aminoterminal b-kjede, en karboksyterminal a-kjede og et forbindelsespeptid i midten kjent som C-peptidet. Innenfor endoplasmatisk retikulum, er proinsulin utsatt for flere spesifikke endopeptidaser som excise c peptid, og dermed generere moden form av insulin. Insulin og fritt c-peptid pakkes I Golgi til sekretoriske granulater som akkumuleres i cytoplasma.
når betacellen er hensiktsmessig stimulert, blir insulin utskilt fra cellen ved eksocytose og diffunderer til kapillærblod i øy. C-peptid utskilles også i blod, men har ingen kjent biologisk aktivitet.
Kontroll Av Insulinsekresjon
Insulin utskilles hovedsakelig som respons på forhøyede blodkonsentrasjoner av glukose. Dette er fornuftig fordi insulin er «ansvarlig» for å lette glukoseinngang i celler. Noen nevrale stimuli (f. eks. syn og smak av mat) og økte blodkonsentrasjoner av andre brenselmolekyler, inkludert aminosyrer og fettsyrer, fremmer også insulinsekresjon. Vår forståelse av mekanismene bak insulinsekresjonen forblir noe fragmentarisk. Likevel har visse funksjoner i denne prosessen blitt tydelig og gjentatte ganger demonstrert, noe som gir følgende modell:
- Glukose transporteres inn i betacellen ved lettere diffusjon gjennom en glukosetransportør; forhøyede konsentrasjoner av glukose i ekstracellulær væske fører til forhøyede konsentrasjoner av glukose i betacellen.
- Forhøyede konsentrasjoner av glukose i betacellen fører til slutt til membrandepolarisering og en tilstrømning av ekstracellulært kalsium. Den resulterende økningen i intracellulært kalsium antas å være en av de primære utløserne for eksocytose av insulinholdige sekretoriske granulater. Mekanismene ved hvilke forhøyede glukosenivåer i betacellen forårsaker depolarisering er ikke klart fastslått, men synes å skyldes metabolisme av glukose og andre brenselmolekyler i cellen, kanskje oppfattet som en endring AV ATP:ADP-forhold OG transdusert til endringer i membranledningsevne.
- Økte nivåer av glukose i betaceller ser også ut til å aktivere kalsiumuavhengige veier som deltar i insulinsekresjon.
 Stimulering av insulinfrigivelse observeres lett hos hele dyr eller mennesker. Den normale fastende blodglukosekonsentrasjonen hos mennesker og de fleste pattedyr er 80 til 90 mg per 100 ml, assosiert med svært lave nivåer av insulinsekresjon.
Stimulering av insulinfrigivelse observeres lett hos hele dyr eller mennesker. Den normale fastende blodglukosekonsentrasjonen hos mennesker og de fleste pattedyr er 80 til 90 mg per 100 ml, assosiert med svært lave nivåer av insulinsekresjon.
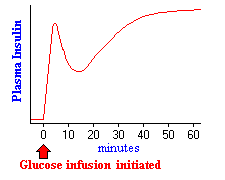
figuren til høyre viser effekten på insulinsekresjon når nok glukose er infundert for å opprettholde blodnivåer to til tre ganger fastende nivå i en time. Nesten umiddelbart etter at infusjonen begynner, øker plasmanivået av insulin dramatisk. Denne innledende økningen skyldes sekresjon av preformert insulin, som snart er betydelig utarmet. Den sekundære økningen i insulin reflekterer den betydelige mengden nylig syntetisert insulin som frigjøres umiddelbart. Klart, forhøyet glukose simulerer ikke bare insulinsekresjon, men også transkripsjon av insulingenet og oversettelse av mRNA.
Avanserte Og Supplerende Emner
- Strukturen Av Insulin