ATP加水分解でどのくらいのエネルギーが放出されますか?
リーダーモード
ATPは、多くの場合、セルのエネルギー通貨と呼ばれています。 代謝変換からシグナル伝達イベントへの細胞内の何百もの反応は、水によるATPの加水分解(文字通り「水の緩み」を意味する)に結合される。 反応ATP+H2O<>ADP+Piは、アデノシン三リン酸(ATP)をアデノシン二リン酸(ADP)および無機リン酸(Pi)に変換する。 この反応に関連する自由エネルギー変化は、膜電位と他の二つの支配的なエネルギー源である還元力を持つ細胞反応の大部分を駆動する。 しかし、このエネルギー通貨はどれくらいの価値があり、購入できる化学取引について何を明らかにしていますか? もちろん、この加水分解反応によって解放されるエネルギーの量は細胞内の条件に依存するので、この質問に対する答えは誰もありませんが、いくつかの簡単な見積もりに頼ることによって、この通貨のおおよその”価値”を感じることができます。

図1:標準条件下でのATP加水分解のギブス自由エネルギーと平衡定数との関係、および生理的条件下での加水分解の自由エネルギーと生理的反応物濃度との関係。
Atp加水分解によるギブス自由エネルギー変化(Δ G)は、図1に示すように、反応中の様々な参加者の濃度に依存する。 濃度が平衡値から遠い場合、Δ Gの絶対値はより大きくなります。 “標準的な”条件の下で(すなわち ATP加水分解のギブス自由エネルギーは、カチオンMg2+の濃度に応じて-28から-34kJ/mol(すなわち≤12kBT、BNID101989)に変化する。 Mgイオンへの依存性は、正に荷電したマグネシウムイオンがATP分子を安定化させるのに役立つために生じる。 ただし、セル内では、条件が標準状態値に近くなることはありません。 例えば、1MのATPの濃度は、溶質の質量が水溶媒自体の質量と同様であることを意味する。 図1では、標準値(Δ Go)からの濃度の比を考えると、生理学的自由エネルギー(Δ G)のしばしば混乱する導出を示しています。 対数としての単位の世話をするために必要とされるような項による除算には、常に単位のない項が含まれている必要があります。 細胞が平衡状態にあった場合、Δ Gの値はゼロであり、ATP加水分解によって得るエネルギーはないと考えることは時々驚くべきことである。 幸いなことに、これは生きている生物では決してそうではありません。 .P>
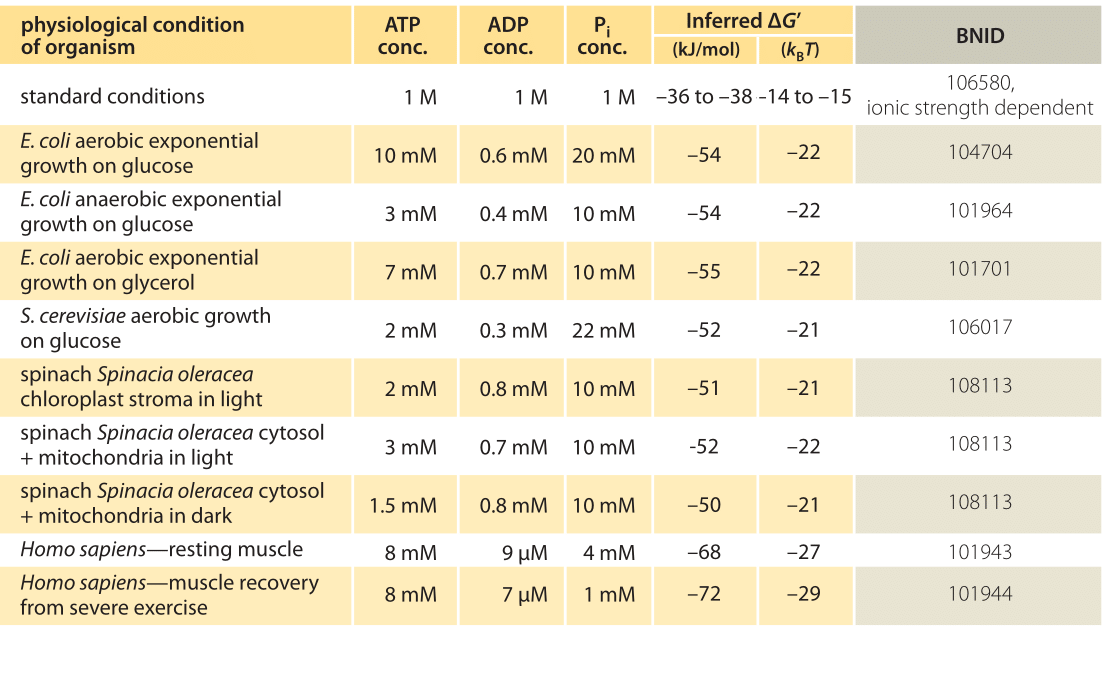
表1:様々な生物および異なる生理学的条件下でのATP加水分解のための自由エネルギー。 Δ G’0の-37.6kJ/molの値に基づいて推定されたΔ G’計算。 これにより、表の値はそれらの間で一貫していますが、一次情報源で報告されたΔ G’値からのわずかな偏差が作成されます。 このような偏差は、イオン強度、pHおよび測定方法の偏りの変動に起因する可能性がある。 値は1桁または2桁の有効数字に丸められます。 Pi濃度が報告されなかったホウレンソウでは、1 0m Mの特性値を使用した(BNID1 0 3 9 8 4、1 0 3 9 8 3、1 1 1 3 5 8、1 0 5 5 4 0)。実際には、生理学的条件は、研究されている生物、検討中の細胞内の組織または区画、および代謝および他の反応に対する現在のエネルギー要求に依存す 例えば、灌流ラット肝臓では、ATP対ADP比はサイトゾルでは約10:1であるが、解糖率が高い下ではミトコンドリアでは1:10であり、解糖率が低い下では両方の比は1に非常に近いことが分かった(BNID111357)。 したがって、Δ Gの値の範囲が予想されます。 この範囲を理解するための鍵は、QがKとどのくらい異なるか、すなわち濃度が標準条件とどのように異なるかを知ることです。 すべての関連成分(ATP、ADPおよびPi)の典型的な細胞内濃度は、標準条件よりもはるかに低いmM範囲にある。 M M範囲の濃度を有する比/は、1よりもはるかに低く、反応は、表1に示されるように、標準条件よりもエネルギー的により有利である。 最高値≥-70kJ/mol(≥30kbt)は、運動後に回復した運動選手の人間の筋肉の値から計算された(BNID101944)。 グルコース上で増殖している大腸菌細胞では、-47kJ/molの値が報告された(≧20kBT、BNID101964)。 これらの数値を視点に置くために、10nm(BNID101857)ステップサイズにわたって約5pN(BNID101832)の力を発揮する分子モーターは、50pN nmのオーダーで動作し、10kBTをわずかに
Δ Gの計算には、関連する細胞内濃度の正確な測定が必要です。 このような濃度は、核磁気共鳴を用いてヒトにおいてin vivoで測定される。 リン(31P)の天然の形態は磁気特性を有するので、外部物質を添加する必要はない。 筋肉のような目的のティッシュは強い磁界に置かれ、NMRスペクトルのピークからATPおよびPiの集中を直接推測するのに無線脈拍の頻度の転位が使用さ Eでは、 大腸菌では、ATPの濃度は、ATP生物発光アッセイを用いてより直接的に測定することができる。 培養物から除去された成長する細菌のサンプルは、イカと共生しているが、今では分子レポーターとして生物学者のツールボックスに参加している細菌 ルシフェラーゼ酵素は、光度計を用いて測定することができる光を生成する反応にATPを使用し、ATP濃度は信号強度から推測することができる。 だから我々は、入力としての細胞含有量、測定された出力として機能する発光にATPの量を変換する”デバイス”としてルシフェラーゼを持っています。 これらのようなツールを使用すると、「実際の」ATPは、濃度が前方反応により有利であるため、「標準」条件下での約2倍の価値があることがわかります。
私たちは、アデニンヌクレオチドがGTPと他のヌクレオチドがはるかにマイナーな役割を果たす主なエネルギー通貨として機能するように選ばれた理由については、立っている質問であることに注目して終わります。 後に「凍結事故」になったのはランダムな選択のケースですか、それともGTP、CTP、UTP、およびTTPよりもATPに選択的な利点がありましたか?










