normaali solujen metabolia riippuu veren pH-arvon säilymisestä hyvin kapeissa rajoissa (7, 35-7, 45).
tämän normaalin pH-alueen ulkopuolellakin suhteellisen miedolla excursiolla voi olla deleterioisia vaikutuksia, kuten vähentynyt hapensaanti kudoksiin, elektrolyyttiset häiriöt ja muutokset sydänlihaksen supistumiskyvyssä; eloonjääminen on mahdollista, jos veren pH laskee alle 6, 8: n tai nousee yli 7, 8: n.
kehon ongelmana on se, että normaaliin aineenvaihduntaan liittyy jatkuva vetyionien (H+) ja hiilidioksidin(CO2) tuotanto, jotka molemmat pyrkivät alentamaan pH: ta. mekanismi, joka voittaa tämän ongelman ja ylläpitää normaalia veren pH: ta(eli säilyttää happo-emäs-homeostaasin), on monimutkainen synergia, johon liittyy veren kemiallisia puskureita, veressä kiertäviä punasoluja(erytrosyyttejä) sekä kolmen elimen: keuhkojen, munuaisten ja aivojen toiminta.
ennen kuin selitetään, miten nämä viisi tekijää vaikuttavat veren pH: n yleiseen ylläpitoon, olisi hyödyllistä tarkastella pikaisesti joitakin peruskäsitteitä.
- mikä on happo, mikä on emäs ja mikä on pH?
- mikä on puskuri? – bikarbonaattipuskurijärjestelmä
- keuhkojen toiminta, hiilidioksidin kuljetus ja happo-emästasapaino
- munuaiset ja happo-emästasapaino
- happo-emästasapainon häiriöt
- happo-emäs – häiriöiden syyt
- Hengitysasidoosi – (kohonneet pCO2(a),alentunut pH)
- Hengitysalaloosi – (pelkistynyt pCO2(a), kohonnut pH)
- metabolinen asidoosi – (vähentynyt HCO3–, alentunut pH)
- metabolinen alkaloosi – (suurentunut HCO3– , kohonnut pH)
- kompensaatio – happopohjaisen häiriötilan seuraus
- happo-emäs-sekahäiriöt
- Yhteenveto
- jotkut ehdottivat jatkotoimia
mikä on happo, mikä on emäs ja mikä on pH?
happo on aine, joka vapauttaa vedyn ioneja (H+) dissosioituessaan liuoksessa.
esimerkiksi: Kloorivetyhappo (HCl) dissosioituu vedyksi ja kloridi-ioneiksi
HCl ![]() H+ + Cl–
H+ + Cl–
hiilihappo (H2CO3) dissosioi vedy-ioneiksi ja bikarbonaatti-ioneiksi
H2CO3 ![]() H+ +HCO3 –
H+ +HCO3 –
erotamme toisistaan vahvat hapot kuten suolahapon ja heikot hapot kuten hiilihapon. Erona on, että vahvat hapotsosioituvat enemmän kuin heikot hapot. Näin ollen vahvan hapon vetyionikonsentraatio on paljon suurempi kuin heikon hapon.
emäs on aine, joka liuoksessa hyväksyy shydrogen-ionit.
esimerkiksi emäksinen bikarbonaatti (HCO3–)hyväksyy vetyionit muodostaen hiilihappoa:
HCO3– + H+ ![]() H2CO3
H2CO3
pH on happamuuden ja emäksisyyden asteikolla 0-14. Puhtaan veden pH on 7 ja se on neutraali (ei hapan eikä emäksinen). pH yli 7is emäksinen ja alle 7 hapan. Siten veren pH (7,35-7,45) onhienosti emäksinen, vaikka kliinisessä lääketieteessä termi alkalosisis, ehkä hämmentävästi, on varattu veren pH: lle, joka on suurempi kuin 7.45ja termi asidoosi on varattu veren pH alle 7,35.
pH on vetyionipitoisuuden (H+) mitta.Nämä kaksi liittyvät toisiinsa seuraavan yhtälön mukaan:
pH = – log10
missä on vetyionien konsentraatio (mol/L)
tästä yhtälöstä
pH 7,4 = h+ konsentraatio 40 nmol/L
pH 7,0 = h+ konsentraatio 100 nmol/L
pH 6,0 = h+ konsentraatio 1000 nmol/L
on selvää, että:
- kaksi muuttujaa muuttuvat kääntäen; vetyionipitoisuuden kasvaessa, pH: n laskiessa
- logaritmisen suhteen vuoksi suuri muutos vetyionipitoisuudessa on itse asiassa pieni muutos pH: ssa. esimerkiksi vetyionipitoisuuden kaksinkertaistuminen saa pH: n laskemaan vain 0,3
mikä on puskuri? – bikarbonaattipuskurijärjestelmä
puskurit ovat liuoksessa olevia kemikaaleja, jotka minimoivat pH: ssa tapahtuvan muutoksen, joka syntyy, kun happoja lisätään ”moppaamalla” vetyioneja. Puskuri on heikon hapon ja senkonjugaattiemäksen liuos. Veressä pääpuskurijärjestelmä on heikkohappo, hiilihappo (H2CO3) ja sen konjugaattibikarbonaatti (HCO3–). Selittääksemme, miten tämä järjestelmä minimoi pH: n muutokset,oletetaan, että lisäämme bikarbonaattipuskuriin vahvan hapon, esim. HCl: n:
happo dissosioituu vapauttaen vetyioneja:
HCl ![]() H+ + Cl –
H+ + Cl –
bikarbonaattipuskuri sitten ”absorboi” vetyionit muodostaen prosessissa karbonihappoa:
HCO3– + H+ ![]() H2CO3 (hiilihappo)
H2CO3 (hiilihappo)
tärkeä seikka on, että koska Hclh: n vetyionit ovat liittyneet heikkoon hiilihappoon, joka ei liukene yhtä helposti, vedyn ionien kokonaismäärä liuoksessa ja siksi pH ei muutu niin paljon kuin puskurin puuttuessa olisi tapahtunut.
vaikka puskuri minimoi suuresti muutoksen, se ei poista sitä, koska heikkokin happo (kuten karbonihappo) dissosioituu jossain määrin. Puskuriliuoksen pH on heikon hapon ja sen konjugaattiemäksen suhteellisten pitoisuuksien funktio.
pH = 6, 1 + log (/)
Where = concentration of bikarbonate
= concentration of carbonic acid
tämä suhde,joka tunnetaan nimellä Hendersonin-Hasselbalchin yhtälö, osoittaa, että pH: ta säätelee emäspitoisuuden(HCO3–) suhde happokonsentraatioon(H2CO3).
koska bikarbonaattipuskuriin lisätään vetyioneja:
h+ +HCO3– ![]() H2CO3
H2CO3
bikarbonaattia (emästä) kulutetaan (pitoisuus laskee) ja tuotetaan karbonihappoa (pitoisuus kasvaa). Jos hydrogenioneja lisätään edelleen, kaikki bikarbonaatti lopulta konsonsuloituisi (muuttuisi hiilihapoksi) eikä sillä olisi mitään puskuroivaa vaikutusta – pH laskisi jyrkästi, jos siihen lisättäisiin enemmän happoa.
Jos hiilihappoa voitaisiin kuitenkin jatkuvasti poistaa järjestelmästä ja bikarbonaattia regeneroida jatkuvasti, puskurointikyky ja siten pH voitaisiin säilyttää vetyionien jatkuvasta lisäämisestä huolimatta.
kuten selviää tarkemmilla tarkennuksilla rasva-emästasapainon fysiologiasta, eli käytännössä siitä, mitä kehossa tapahtuu. Inessence, keuhkot varmistavat hiilihapon poistamisen (hiilidioksidina) ja munuaiset varmistavat jatkuvan regeneroinnin ofbikarbonaatti.
tämä keuhkojen rooli riippuu bikarbonaatin puskurointijärjestelmälle ominaisesta singularcharcharacteristicista eli hiilihapon muuntautumiskyvystä hiilidioksidiksi ja vedeksi.
seuraava yhtälö hahmottelee bikarbonaatin puskurointijärjestelmän kaikkien elementtien suhdetta, koska se toimii thebodyssa
h+ +HCO3– ![]() H2CO3
H2CO3 ![]() H2O + CO2
H2O + CO2
on tärkeää huomata että reaktiot ovat palautuvia.Suunta riippuu suhteellisesta konsentraatiosta kuhunkin. Siten, että esimerkiksi hiilidioksidikonsentraation nousu pakottaa reaktion vasemmalle lisääntyvällä hiilihapon ja lopulta vetyionien muodostumisella.
Tämä selittää hiilidioksidin happopotentiaalin ja johdattaa meidät tärkeään vaikutukseen, jonka keuhkot ja punasolut tekevät kokonaishappopohjaan.
keuhkojen toiminta, hiilidioksidin kuljetus ja happo-emästasapaino
vakio veren CO2-määrä, joka on välttämätön normaalille happo-emästasapainolle, kuvastaa tasapainoa kudossolujen metabolian tuloksena syntyneen hiilidioksidin ja keuhkojen kautta erittyvän ilman välillä.
vaihtelemalla hiilidioksidin erittymisnopeutta keuhkot säätelevät veren hiilidioksidipitoisuutta.Tapahtumasarja hiilidioksidintuotannosta poistumiseen uloshengitysilmassa on kuvattu kuvassa. 1.Hiilidioksidi diffundoituu ulos kudossoluista ympäröiväänkapillaariseen vereen (Kuva. 1 A). Pieni osa liukenee veriplasmaan ja kulkeutuu keuhkoihin muuttumattomana.
, mutta suurin osa diffuusioituu punasoluihin, joissa se yhdistyy veden kanssa muodostaen hiilihappoa.Happo dissosioituu tuottaen vetyioneja ja bikarbonaattia. Vetyionit yhdistyvät deoxygenated hemoglobiini (hemoglobiini toimii puskurina tässä), estää vaarallisen Fall solun pH, ja bikarbonaatti diffundoituu pitkin concentrationgradient punasolusta plasmaan.
näin suurin osa kudoksissa syntyvästä hiilidioksidista kulkeutuu keuhkoihin bikarbonaatti-veriplasmana.
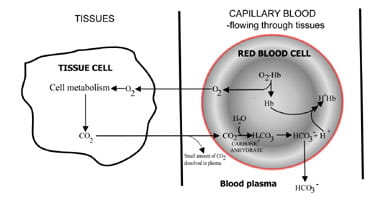
viikuna. 1A. kudoksissa tuotettu CO2, joka on muunnettu bikarbonaatiksi keuhkoihin kuljettamista varten.
|
|
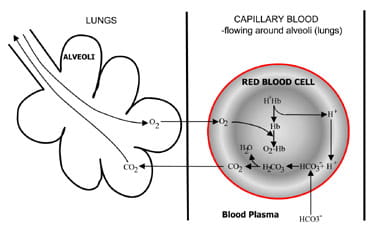
Fig. 1b. At the lungs bicarbonate convertedback to CO2 and eliminated by the lungs.
keuhkojen keuhkorakkuloissa prosessi on päinvastainen (kuva. 1b).Vetyionit siirtyvät hemoglobiinista, kun se ottaa happea inspiroidusta ilmasta. Vetyionit puskuroidaan nyt bybikarbonaatilla, joka diffundoituu plasmasta takaisin punasoluksi, jolloin muodostuu karbonihappoa. Kun tämän pitoisuus nousee, se muuntuu vedeksi ja hiilidioksidiksi. Lopuksi, hiili dioksididiffuusiota alas pitoisuus gradientti punasoluista keuhkorakkuloiden forexcretion uloshengitysilmassa.
aivorungon hengityselimistön kemoreseptorit reagoivat veren hiilidioksidipitoisuuden muutoksiin, mikä lisää ilmanvaihtoa (hengitystä), jos hiilidioksidipitoisuus nousee, ja vähentää ilmanvaihtoa, jos hiilidioksidi laskee.
munuaiset ja happo-emästasapaino
normaali solujen aineenvaihdunta johtaa vetyionien jatkuvaan muodostumiseen. Olemme nähneet, että yhdistämällä näiden vetyionien kanssa veren bikarbonaattipuskuri minimoi sen vaikutuksen. Puskuroinnista on kuitenkin hyötyä vain lyhyellä aikavälillä, ja lopulta vetyionit on poistettava kehosta.Lisäksi on tärkeää, että bikarbonaatti, jota käytetään puskuroimaan vetyioneja, korvataan jatkuvasti.
nämä kaksi tehtävää,vetyionien eliminointi ja bikarbonaatin regenerointi, hoidetaan munuaisten toimesta. Munuaisten tubulusoluissa on runsaasti teentsyymiä hiilihappoanhydraasia, joka helpottaa karbonikaasun muodostumista hiilidioksidista ja vedestä. Hiilihappo dissosioi tobikarbonaattia ja vetyioneja. Bikarbonaatti imeytyy takaisin vereen ja vetyionit kulkeutuvat tubuluksen lumeen ja poistuvat elimistöstä virtsaan.
tämä virtsan poistuminen riippuu puskurien, pääfosfaatti-ja ammoniakki-ionien esiintymisestä virtsassa.
happo-emästasapainon häiriöt
useimmat happo-emästasapainon häiriöt johtuvat
- sairaudesta tai sellaisten elinten (munuaisten, keuhkojen, aivojen) vaurioitumisesta, joiden normaali toiminta on välttämätön happo-emästasapainon kannalta,
- sairaudesta, joka aiheuttaa aineenvaihdunnan happojen poikkeavan lisääntymisen siten, että homeostaattiset mekanismit hukkuvat
- lääketieteellisiin toimenpiteisiin (esim. koneellinen ilmanvaihto, jotkut lääkkeet)
Valtimoverikaasut ovat verikoe, jota käytetään happo-emäs-häiriöiden tunnistamiseen ja monitorointiin. Kolme verikaasuanalyysin aikana mitattua muuttujaa, valtimoveren pH (pH), valtimoveren hiilidioksidin osapaine (pCO2(A)) ja bikarbonaatin pitoisuus (HCO3–) ovat erityisen tärkeitä (KS.taulukko I viitealue (normaali)).Näiden kolmen tulokset mahdollistavat happo-basedisturbanssin luokittelun johonkin neljästä etiologisesta kategoriasta:
- Respiratory acidosis
- Respiratory alkalosis
- Metabolic acidosis
- Metabolic alkalosis
|
Adults |
Neonates |
|
|
pH |
7.35-7.45 |
7.30-7.40 |
|
pCO2 (kPa) |
4.7-6.0 |
3.5-5.4 |
|
Bicarbonate |
22-28 |
15-25 |
TABLE I. Likimääräiset (normaalit) viitealueet
ymmärtääksemme, miten pH: n, pCO2(a): n ja bikarbonaatin tuloksia käytetään happo-emäs-häiriöiden luokitteluun tällä tavalla, meidän on palattava Hendersonin-Hasselbalchin yhtälöön
pH = 6.1 + log (/)
mitataan pH ja bikarbonaatti, mutta ei hiilihappoa(H2CO3). PCO2(A): n ja H2CO3: n välillä on kuitenkin suhde, joka mahdollistaa Verikaasuanalyysissä mitattujen kolmen parametrin (pH, pCO2(A) ja bikarbonaatti) Hendersonin-Hasselbalchin yhtälön toistamisen:
pH = 6.1 + log ( /( pCO2(a) × 0.23))
poistamalla kaikki vakiot tästä yhtälöstä voidaan kolmen mitatun parametrin välinen suhde yksinkertaistaa:
pH ∝ / pCO2(a)
tämä suhde, joka on ratkaisevan tärkeä kaikkien happo-emäshäiriöiden ymmärtämisen kannalta, toteaa, että arterialveren pH on verrannollinen bikarbonaattikonsentraation ja pCO2(A): n suhteeseen. Sen avulla seuraavat deduktiot:
- pH pysyy normaalina niin kauan kuin suhde : pCO2(a) pysyy normaalina
- pH nousee (eli alkaloosia esiintyy), jos joko nousee tai pCO2(a) laskee.
- pH laskee (ts. asidoosi tapahtuu) jos joko laskee tai pCO2(a) kasvaa
- Jos sekä pCO2(a) ja niitä nostetaan suhteellisen saman verran, suhde ja siten pH ovat normaalit
- Jos sekä pCO2(a) että pienenevät suhteellisen saman verran, suhde ja siten pH ovat normaalit.
happo-emäshäiriöt vaikuttavat ensisijaisesti eitherpCO2(a): iin, jolloin sitä kutsutaan respiratoriseksi häiriöksi, tai, jolloin sitä kutsutaan anon-respiratoriseksi tai metaboliseksi häiriöksi.:
- Jos ensisijainen häiriö on kohonnut pCO2(a) (joka aiheuttaa asidoosin – KS. yllä), tilaa kutsutaan hengitysasidoosiksi
- Jos ensisijainen häiriö on alentunut pCO2(a) (joka aiheuttaa alkaloosia – KS. yllä), tilaa kutsutaan hengitysalaloosiksi
- Jos primaarinen häiriö liittyy bikarbonaatin pienenemiseen (joka johtaa asidoosiin – KS. yllä), tilaa kutsutaan metaboliseksi asidoosiksi
- Jos primaarinen häiriö liittyy korotetulla bikarbonaatilla (joka johtaa alkaloosiin – KS. edellä), tilaa kutsutaan metabolinen alkaloosi
happo-emäs – häiriöiden syyt
Hengitysasidoosi – (kohonneet pCO2(a),alentunut pH)
Hengitysasidoosille on ominaista lisääntynyt pCO2(a), joka johtuu riittämättömästä alveolaarisesta ilmanvaihdosta(hypoventilaatiosta) ja siitä johtuvasta alentuneesta ofCO2: n poistumisesta verestä. Hengityselinsairauksiin, kuten keuhkoruttoon, keuhkolaajentumaan, astmaan ja krooniseen ahtauttavaan ilmasairauteen, voi kaikkiin liittyä riittävästi hypoventilaatiota hengitysasidoosin aiheuttamiseksi.
jotkut lääkkeet (esim. morfiini ja barbituraatit) voivat aiheuttaa hengitysasidoosia masentamalla aivojen respiratorista keskusta. Vahinko tai trauma rintakehän ja lihaksiston mukana mekaniikka hengitys voi vähentää ilmanvaihtoa nopeus. Tämä selittää hengitysilmahapotjotka voivat vaikeuttaa sairauksien kulkua, kuten poliomyeliitti, Guillain-Barren oireyhtymä ja toipuminen vakavasta rintakehän traumasta.
Hengitysalaloosi – (pelkistynyt pCO2(a), kohonnut pH)
sen sijaan hengitysalaloosille on ominaista heikentynyt pCO2(a), joka johtuu liiallisesta alveolaarisesta hengitysilmasta ja joka johtaa liialliseen hiilidioksidin poistumiseen verestä.Sairaus, jossa veren hapen vähenemisen vuoksi (hypoksemia), therespiratory keskus stimuloidaan voi johtaa respiratoryalkaloosi.
esimerkkejä Tässä ovat vaikea anemia, keuhkoembolismi ja aikuisen hengitysoireyhtymä. Hyperventilaatio riittää aiheuttamaan hengitysteiden alkaloosia voi olla ahdistuskohtausten ominaisuus ja vastata kovaan kipuun. Yksi vähemmän tervetullut ominaisuuksia salicylate (aspiriini) on sen stimuloiva vaikutus hengityssuojainkeskus. Tämä vaikutus selittää salisylaattiyliannostuksen jälkeisen hengitysteiden alkaloosin. Lopuksi ylienthusiastimekaaninen ilmanvaihto voi aiheuttaa hengitysteiden alkaloosia.
metabolinen asidoosi – (vähentynyt HCO3–, alentunut pH)
bikarbonaatin pieneneminen on aina metabolisen asidoosin piirre. Tämä johtuu kahdesta syystä: bikarbonaatin lisääntynyt käyttö epänormaalin happokuorman puskuroinnissa tai bikarbonaatin lisääntynyt häviö kehosta. Diabeettinen ketoasidoosi ja laktikasidoosi ovat kaksi tilaa, joille on ominaista metabolihappojen ylituotanto ja siitä johtuva bikarbonaatin uupuminen.
ensimmäisessä tapauksessa ketohappojen(B-hydroksivoihappo ja asetoetikkahappo) poikkeuksellisen korkeat pitoisuudet veressä kuvastavat eristyneisyydestä johtuvia vakavia metabolisia häiriöitä.
kaikki solut tuottavat maitohappoa,jos niillä on hapenpuute, joten lisääntynyttä maitohapon tuotantoa ja siitä johtuvaa metaboliasidoosia esiintyy kaikissa tiloissa, joissa hapensaanti on vakavasti heikentynyt.
esim.sydänpysähdys ja mikä tahansa hypovoleemiseen sokkiin liittyvä tila (esim. massivefluidin menetys). Maksalla on merkittävä rooli normaalin solumetabolian aikana syntyvän maitohapon pienen määrän poistamisessa, joten maitohappoasidoosi voi olla maksavaurion ominaisuus.
epänormaalia bikarbonaatin häviämistä kehosta voi esiintyä ripulin aikana. Ilman valvontaa tämä voi johtaa metaboliseen asidoosiin.Bikarbonaatin uusiutumisen ja vety-ionien erittämisen epäonnistuminen selittää renalfailuressa esiintyvää metabolista asidoosia.
metabolinen alkaloosi – (suurentunut HCO3– , kohonnut pH)
bikarbonaatti nousee aina metabolisessa alkaloosissa. Bikarbonaatin liiallinen annostelu tai bikarbonaattivalmisteen nauttiminen voi harvoin aiheuttaa metabolista alkaloosia, mutta tämä on yleensä ohimenevää. Epänormaali menetys vetyionien kehosta voion ensisijainen ongelma. Bikarbonaatti, joka muutoin tulisi ajatelleeksi näiden menetettyjen vetyionien puskuroimiseksi, kerääntyy näin ollen vereen. Mahaneste on hapanta ja gastricaspiration tai sairaus prosessi, jossa mahalaukun sisältö onlostin kehosta edustaa menetys vetyioneja.
esimerkiksi mahanesteen oksentaminen selittää pylorikstenoosipotilailla mahdollisesti ilmenevän metabolisen alkaloosin. Vakava kaliumvaje voi aiheuttaa metabolisia alkalooseja vedyn ja kaliumionien keskinäisen suhteen vuoksi.
kompensaatio – happopohjaisen häiriötilan seuraus
elämän kannalta on elintärkeää,että pH ei poikkea liian kauas normaalista, ja elimistö pyrkii aina palauttamaan epänormaalin pH: n normaalitasapainon häiriintyessä. Tästä elämän säilyttämisestä maksetaan korvauksia. Korvauksen ymmärtämiseksi on tärkeää muistaa, että pH: ta säätelee pCO2 (a). niin kauan kuin suhde on normaali, pH on normaali.
harkitse metabolista asidoosia sairastavaa potilasta, jonka pH on alhainen, koska bikarbonaatti on alhainen. Jotta voidaan kompensoida alhainen ja palauttaayleisen tärkeä suhde normaaliin potilaan on laskettava hispCO2 (a). Aivojen hengityskeskuksen kemoreseptorit reagoivat lisääntyvään vetyionipitoisuuteen (alhainen pH), mikä lisää ilmanvaihtoa (hyperventilaatio) ja lisää hiilidioksidin poistumista; pCO2(a) laskee ja suhde : pCO2(a) palautuu normaaliksi.
kompensaatio metaboliseen alkaloosiin, jossa on korkea, sen sijaan liittyy hengityksen heikentymiseen ja siten hiilidioksidien säilymiseen niin, että pCO2(a) nousee vastaamaan suurentumista . Hikoilun masennuksella on kuitenkin epätoivottu sivuvaikutus, joka uhkaa kudosten riittävää lisääntymistä. Tästä syystä hengitysteiden kompensointi metabolinen alkaloosi on rajoitettu.
pCO2(A): n (respiratoriasidoosi ja alkaloosi) Primaarihäiriöt kompensoidaan vedyionierityksen munuaismuutoksilla, jotka aiheuttavat muutoksia pCO2(A): n primaarisessa muutoksessa. Näin ollen hengitysasidoosin (raisedpCO2(a)) uudelleenkompensointiin liittyy bikarbonaatin lisääntynyt takaisinimeytyminen, ja hengitysteiden alkaloosin(reduced pCO2(a)) munuaisten kompensointiin liittyy bikarbonaattimabsorption väheneminen.
happo-emästasapainon käsite kompensaation aikana välittyy visuaalisesti kuviossa. 2. Taulukossa II esitetään yhteenveto veren kaasutuloksista, jotka luonnehtivat kaikkia neljää happo-emäshäiriötä ennen ja jälkeen kompensoinnin.
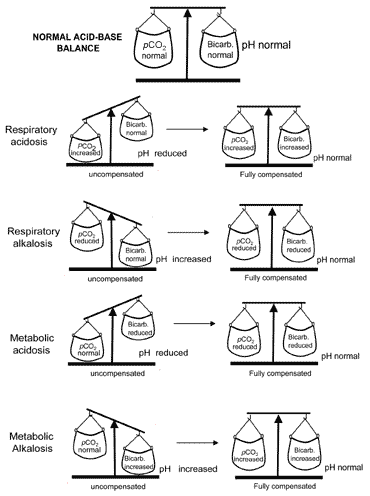
kuva. 2. ”Happo-emästasapaino” : compensationrestores normal pH
|
Primary disturbance |
||||
|
Respiratory |
Repiratory |
Metabolic |
Metabolic |
|
|
Some |
Emphysema |
Hyper- |
Renal failure |
Bicarbonate Potassium |
|
Compen- |
RENAL |
RENAL |
RESPIRA- |
RESPIRA- |
|
Initial blood |
pH |
pH |
pH |
pH |
|
Blood gas |
pH pCO2 |
pH pCO2 |
pH pCO2 |
Limited |
|
Blood gas |
pH normal |
pH normal |
pH normal |
Limited |
Tulostettava versio taulukosta, pdf.
taulukko II. Verikaasu aiheuttaa happiemästasapainon häiriöitä
primaarisen metabolisen häiriön Hengityskompensaatio tapahtuu paljon nopeammin kuin metabolinen (munuaisten) kompensaatio alkuhengityshäiriön vuoksi. Toisessa tapauksessa korvaukset tapahtuvatpäivinä tuntien sijaan.
Jos korvaus johtaa pH: n palautumiseen normaaliksi, potilaan sanotaan saavan täyden korvauksen. Mutta monissa tapauksissa korvaus palauttaa pHtowards normaali saavuttamatta normaaliutta; tällaisissa tapauksissa potilaan sanotaan saavan osittaisen korvauksen.
edellä kuvatuista syistä metabolinen alkaloosi on hyvin harvoin täysin korvattavissa.
happo-emäs-sekahäiriöt
edellä esitetyn perusteella voidaan olettaa, että kaikilla happo-emäs-häiriöistä kärsivillä potilailla on vain yksi happo-emästasapainon neljästä luokasta. Näin voi hyvinkin olla,mutta tietyissä olosuhteissa potilailla voi esiintyä enemmän kuin yksi häiriö.
esimerkiksi kroonisesta sairaudesta, kuten keuhkolaajentumasta, kärsivä potilas, jolla on pitkäaikainen osittain kompensoitu hengitysasidoosi. Jos tämä potilas oli myös adiabeettinen eikä ollut ottanut normaalia insuliiniannostaan ja oli sen vuoksi diabeettisessa ketoasidoosissa, verikaasutulokset heijastaisivat sekä hengitysasidoosin että metabolisen asidoosin yhteisvaikutusta.
tällaisia happo-emäs-sekahäiriöitä ei esiinny usein, ja niitä voi olla vaikea selvittää pelkän valtimoverikaasutuloksen perusteella.
Yhteenveto
veren normaalin pH: n ylläpitoon liittyy useita elinjärjestelmiä ja se riippuu verenkierron eheydestä. Ei ole yllättävää, ettähappo-emästasapainon häiriöt voivat vaikeuttaa kulkualaajasti erilaisia sairauksia sekä traumoja moniin kehon osiin. Elimistöllä on huomattava teho veren pH: n säilyttämisessä, ja häiriöt viittaavat yleensä joko vakavaan krooniseen sairauteen tai akuuttiin sairauteen.
valtimoverikaasuanalyysin tulokset voivat tunnistaa happo–emäshäiriön ja antaa arvokasta tietoa sen aiheuttajasta.
jotkut ehdottivat jatkotoimia
- Thomson WST, Adams JF, Cowan RA. Kliininen happo-emästasapaino. Oxford: Oxford Medical Publications 1997
- Harrison RA. Happo-emästasapaino. Respir Care Clin N. America 1995; 1,1: 7-21
- Woodrow P. Arterial blood gas analysis. Nursing Standard 2004; 18,21: 45-52
- Sirker AA, Rhodes A, Gounds RM, Bennet ED. Happo-emäsfysiologia: ”perinteinen” ja ”moderni” lähestymistapa. Anaesthesia 2002; 57: 348-56