generisk navn: Terbutalinsulfat
doseringsform: injektion, opløsning
medicinsk gennemgået af Drugs.com. sidst opdateret den 1. september 2020.
- oversigt
- bivirkninger
- dosering
- professionel
- interaktioner
- mere
en steril vandig opløsning til subkutan injektion
kun
advarsel: forlænget tocolyse
Terbutalinsulfat er ikke godkendt og bør ikke anvendes til langvarig tocolyse (ud over 48-72 timer). Især bør Terbutalinsulfat ikke anvendes til vedligeholdelse tocolyse i ambulant eller hjemme indstilling. Alvorlige bivirkninger, inklusive død, er rapporteret efter administration af Terbutalinsulfat til gravide kvinder. I moderen omfatter disse bivirkninger øget hjertefrekvens, forbigående hyperglykæmi, hypokalæmi, hjertearytmier, lungeødem og myokardisk iskæmi. Øget føtal hjertefrekvens og neonatal hypoglykæmi kan forekomme som følge af moderadministration (se kontraindikationer: langvarig tocolyse).
- Terbutalin beskrivelse
- Terbutalin – Klinisk Farmakologi
- Prækliniske
- farmakokinetik
- indikationer og anvendelse til Terbutalin
- kontraindikationer
- advarsler
- forværring af astma
- brug af antiinflammatoriske midler
- kardiovaskulære effekter
- anfald
- forholdsregler
- generelt
- lægemiddelinteraktioner
- carcinogenese, mutagenese, nedsat fertilitet
- graviditet-teratogene virkninger
- anvendelse ved fødsel og fødsel
- ammende mødre
- pædiatrisk brug
- geriatrisk anvendelse
- bivirkninger
- overdosering
- Terbutalin Dosering og Administration
- hvordan leveres Terbutalin
- PRINCIPAL displaypanel
- hoveddisplaypanel
- SERIALIZATION IMAGE
- mere om terbutalin
- Forbrugerressourcer
- professionelle ressourcer
- relaterede behandlingsvejledninger
Terbutalin beskrivelse
Terbutalinsulfat, USP, den aktive ingrediens i Terbutalinsulfatinjektion, USP, er en beta‑adrenerg agonistbronodilator tilgængelig som en steril, ikke-pyrogen, vandig opløsning i hætteglas til subkutan administration. Hver milliliter opløsning indeholder 1 mg Terbutalinsulfat, USP (0,82 mg af den frie base), natriumchlorid til isotonicitet, 0,055% edetatdinatriumdihydrat som stabiliseringsmiddel og saltsyre til justering til en mål-pH på 4. Terbutalinsulfat er-a–3,5-dihydroksybensy alkoholsulfat (2:1) (salt). Molekylformlen er (C12H19N03) 2 * H2SO4 og strukturformlen er:
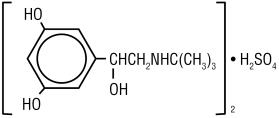
Terbutalinsulfat, USP er et hvidt til gråhvidt krystallinsk pulver. Det er lugtfri eller har en svag lugt af eddikesyre. Det er opløseligt i vand og i 0,1 N saltsyre, let opløseligt i methanol og uopløseligt i chloroform. Dens molekylvægt er 548,65.
Terbutalin – Klinisk Farmakologi
terbutalinsulfatinjektion er en beta-adrenerg receptoragonist. In vitro og in vivo farmakologiske undersøgelser har vist, at Terbutalin har en præferentiel virkning på beta2‑adrenerge receptorer. Mens det erkendes, at beta2-adrenerge receptorer er de dominerende receptorer i bronkial glat muskel, indikerer data, at der er en population af beta2-receptorer i det menneskelige hjerte, der findes i en koncentration mellem 10% og 50%. Den nøjagtige funktion af disse receptorer er ikke fastlagt (se advarsler). Kontrollerede kliniske studier hos patienter, der fik terbutalin subkutant, har ikke afsløret en præferentiel beta2-adrenerg effekt.de farmakologiske virkninger af beta-adrenerge agonister, herunder Terbutalin, kan i det mindste delvis tilskrives stimulering gennem beta-adrenerge receptorer af intracellulær adenylcyclase,som katalyserer omdannelsen af adenosintrifosfat (ATP) til cyklisk 3′, 5′-adenosinmonophosphat (cAMP). Øgede cAMP-niveauer er forbundet med afslapning af bronchial glat muskel og hæmning af frigivelse af mediatorer med øjeblikkelig overfølsomhed fra celler, især fra mastceller.
kontrollerede kliniske studier har vist, at Terbutalinsulfatinjektion lindrer bronkospasme ved akut og kronisk obstruktiv lungesygdom ved signifikant at øge lungestrømningshastighederne (f.eks. en stigning på 15% eller mere i FEV1). Efter subkutan administration af 0,25 mg terbutalinsulfatinjektion forekommer en målbar ændring i ekspiratorisk strømningshastighed normalt inden for 5 minutter, og en klinisk signifikant stigning i FEV1 forekommer inden for 15 minutter. Den maksimale effekt forekommer normalt inden for 30 til 60 minutter, og klinisk signifikant bronchodilatoraktivitet kan fortsætte i 1, 5 til 4 timer. Varigheden af klinisk signifikant forbedring er sammenlignelig med den, der observeres med ækvimilligramdoser af epinephrin.
Prækliniske
forsøg med forsøgsdyr (minipigs, gnavere og hunde) har vist forekomsten af hjertearytmier og pludselig død (med histologisk tegn på myocardienekrose), når beta-agonister og methylksantiner administreres samtidigt. Den kliniske betydning af disse fund er ukendt.
farmakokinetik
subkutan administration af 0, 5 mg Terbutalinsulfat til 17 raske, voksne, mandlige forsøgspersoner resulterede i gennemsnitlig (SD) peak plasma Terbutalinkoncentration på 9, 6 (3, 6) ng / mL, hvilket blev observeret ved en median (interval) tid på 0, 5 (0, 08 til 1, 0) timer efter dosering. Middelværdierne (SD) AUC (0 til 48) og total legemsclearance var henholdsvis 29,4 (14,2) t•ng/mL og 311 (112) mL/min. Den terminale halveringstid blev bestemt hos 9 af de 17 forsøgspersoner og havde en gennemsnitlig (SD) på 5,7 (2,0) timer.
efter subkutan administration af 0,25 mg Terbutalinsulfat til to mandlige forsøgspersoner blev der observeret maksimale serumkoncentrationer af terbutalin på 5,2 og 5,3 ng/mL ca.20 minutter efter dosering.eliminationshalveringstiden for lægemidlet hos 10 ud af 14 patienter var cirka 2,9 timer efter subkutan administration, men længere eliminationshalveringstider (mellem 6 og 14 timer) blev fundet hos de andre 4 patienter. Cirka 90% af lægemidlet blev udskilt i urinen 96 timer efter subkutan administration, hvor omkring 60% af dette var uændret lægemiddel. Det ser ud til, at sulfatkonjugatet er en vigtig metabolit af terbutalin, og urinudskillelse er den primære eliminationsvej.
indikationer og anvendelse til Terbutalin
Terbutalinsulfatinjektion, USP er indiceret til forebyggelse og reversering af bronkospasme hos patienter 12 år og ældre med astma og reversibel bronkospasme forbundet med bronkitis og emfysem.
kontraindikationer
1. Langvarig tocolyse
Terbutalinsulfat er ikke godkendt og bør ikke anvendes til langvarig tocolyse (ud over 48-72 timer). Især bør Terbutalinsulfat ikke anvendes til vedligeholdelsestokolyse i ambulant eller hjemmeindstilling (Se boks advarsel: langvarig tocolyse).
2. Overfølsomhed
Terbutalinsulfatinjektion er kontraindiceret hos patienter, der vides at være overfølsomme over for sympatomimetiske aminer eller en hvilken som helst komponent i dette lægemiddelprodukt.
advarsler
forværring af astma
astma kan forværres akut over en periode på timer eller kronisk over flere dage eller længere. Hvis patienten har brug for flere doser Terbutalinsulfat end normalt, kan dette være en markør for destabilisering af astma og kræver revurdering af patienten og behandlingsregimen under særlig hensyntagen til det mulige behov for antiinflammatorisk behandling, f.eks. kortikosteroider.
brug af antiinflammatoriske midler
brug af beta-adrenerge agonistbronodilatorer alene er muligvis ikke tilstrækkelig til at kontrollere astma hos mange patienter. Det bør tidligt overvejes at tilsætte antiinflammatoriske midler, f.eks. kortikosteroider.
kardiovaskulære effekter
Terbutalinsulfat, som alle andre beta-adrenerge agonister, kan producere en klinisk signifikant kardiovaskulær effekt hos nogle patienter målt ved pulsfrekvens, blodtryk og / eller symptomer. Selvom sådanne virkninger er ualmindelige efter administration af Terbutalinsulfat i anbefalede doser, kan det være nødvendigt at afbryde lægemidlet, hvis de forekommer. Derudover er det rapporteret, at beta‑agonister producerer elektrokardiogram (EKG) ændringer, såsom udfladning af T-bølgen, forlængelse af Kvtc-intervallet og St-segmentdepression. Den kliniske betydning af disse fund er ukendt. Derfor bør Terbutalinsulfat, som alle sympatomimetiske aminer, anvendes med forsigtighed til patienter med hjerte-kar-sygdomme, især koronar insufficiens, hjertearytmier og hypertension.
anfald
der har været sjældne rapporter om anfald hos patienter, der fik Terbutalin; anfald gentog sig ikke hos disse patienter, efter at lægemidlet blev afbrudt.
forholdsregler
generelt
Terbutalin, som med alle sympatomimetiske aminer, bør anvendes med forsigtighed til patienter med hjerte-kar-sygdomme, herunder iskæmisk hjertesygdom, hypertension og hjertearytmier; hos patienter med hyperthyreoidisme eller diabetes mellitus; og hos patienter, der er usædvanligt lydhøre over for sympatomimetiske aminer, eller som har krampeanfald. Signifikante ændringer i systolisk og diastolisk blodtryk er set og kunne forventes at forekomme hos nogle patienter efter brug af en hvilken som helst beta-adrenerg bronchodilator.
umiddelbare overfølsomhedsreaktioner og forværringer af bronkospasme er blevet rapporteret efter administration af terbutalin.Beta-adrenerge agonistmedicin kan producere signifikant hypokalæmi hos nogle patienter, muligvis gennem intracellulær shunting, som har potentialet til at producere uønskede kardiovaskulære virkninger. Faldet er normalt forbigående og kræver ikke tilskud.
store doser intravenøs Terbutalin er rapporteret at forværre allerede eksisterende diabetes mellitus og ketoacidose.
lægemiddelinteraktioner
samtidig brug af terbutalinsulfatinjektion med andre sympatomimetiske midler anbefales ikke, da den kombinerede virkning på det kardiovaskulære system kan være skadelig for patienten.Terbutalin bør administreres med ekstrem forsigtighed til patienter, der behandles med monoaminoksidasehæmmere eller tricykliske antidepressiva, eller inden for 2 uger efter seponering af sådanne midler, da Terbutalins virkning på det vaskulære system kan forstærkes.
betablokkere: Beta-adrenerge receptorblokerende midler blokerer ikke kun lungeffekten af beta-agonister, såsom Terbutalinsulfatinjektion, men kan producere alvorlig bronkospasme hos astmatiske patienter. Derfor bør patienter med astma normalt ikke behandles med betablokkere. Under visse omstændigheder, f.eks. som profylakse efter myokardieinfarkt, kan der dog ikke være acceptable alternativer til brugen af beta-adrenerge blokeringsmidler hos patienter med astma. I denne indstilling kunne kardioselektive betablokkere overvejes, selvom de skal administreres med forsigtighed.diuretika kan forværres akut af beta-agonister, især når den anbefalede dosis af beta-agonisten overskrides. Selvom den kliniske betydning af disse virkninger ikke er kendt, tilrådes forsigtighed ved samtidig administration af beta-agonister og ikke-kaliumbesparende diuretika.
carcinogenese, mutagenese, nedsat fertilitet
I et 2-årigt studie med rotter forårsagede Terbutalinsulfat en signifikant og dosisrelateret stigning i forekomsten af godartede leiomyomer i mesovariet ved diætdoser på 50 mg/kg og derover (ca.810 gange den maksimale anbefalede daglige subkutane (sc) dosis for voksne på mg / m2-basis). I et 21-måneders studie med CD-1-mus viste Terbutalinsulfat ingen tegn på tumorigenicitet ved diætdoser på op til 200 mg/kg (ca.1.600 gange den maksimale anbefalede daglige sc-dosis for voksne på mg/m2-basis). Mutagenicitetspotentialet for Terbutalinsulfat er ikke bestemt.reproduktionsstudier på rotter med Terbutalinsulfat viste ingen forringelse af fertiliteten ved orale doser på op til 50 mg/kg (ca.810 gange den maksimale anbefalede daglige sc-dosis for voksne på mg/m2-basis).
graviditet-teratogene virkninger
graviditetskategori C
der er ingen tilstrækkelige og velkontrollerede undersøgelser af Terbutalinsulfat hos gravide kvinder. Offentliggjorte dyreforsøg viser, at rotteafkom udviser ændringer i adfærd og hjerneudvikling, herunder nedsat cellulær proliferation og differentiering, når dæmninger blev behandlet subkutant med Terbutalin i det sene stadium af graviditet og laktationsperiode. 24 Til 48 gange den almindelige humane dosis hos voksne på 2-4 mg/dag på mg/m2-basis.
Terbutalinsulfat er ikke godkendt og bør ikke anvendes til langvarig tocolyse (ud over 48-72 timer). Især bør Terbutalinsulfat ikke anvendes til vedligeholdelse tocolyse i ambulant eller hjemme indstilling. Alvorlige bivirkninger, inklusive død, er rapporteret efter administration af Terbutalinsulfat til gravide kvinder. I moderen omfatter disse bivirkninger øget hjertefrekvens, forbigående hyperglykæmi, hypokalæmi, hjertearytmier, lungeødem og myokardisk iskæmi. Øget føtal hjertefrekvens og neonatal hypoglykæmi kan forekomme som et resultat af moderadministration (Se boks advarsel: langvarig tocolyse og kontraindikationer: langvarig tocolyse).
i dyreembryofetale udviklingsundersøgelser blev der ikke observeret teratogene virkninger hos afkom, når drægtige rotter og kaniner fik Terbutalinsulfat ved orale doser op til 50 mg/kg/dag, henholdsvis ca.810 og 1.600 gange, den maksimale anbefalede daglige subkutane dosis til voksne på mg/m2-basis.
Terbutalinsulfat bør kun anvendes under graviditet, hvis de potentielle fordele berettiger den potentielle risiko for fosteret.
anvendelse ved fødsel og fødsel
på grund af potentialet for beta-agonistinterferens med uterin kontraktilitet bør anvendelse af terbutalinsulfatinjektion til lindring af bronchospasme under fødslen begrænses til de patienter, hvor fordelene klart opvejer risikoen.
Terbutalin krydser placenta. Efter enkeltdosis IV administration af terbutalin til 22 kvinder i slutningen af graviditeten, som blev leveret ved valgfri kejsersnit på grund af kliniske årsager, viste det sig, at umbilical blodniveauer af terbutalin lå i området fra 11% Til 48% af moderens blodniveauer.
ammende mødre
det vides ikke, om dette lægemiddel udskilles i modermælk. Derfor bør Terbutalinsulfatinjektion kun anvendes under amning, hvis den potentielle fordel berettiger den mulige risiko for den nyfødte.
pædiatrisk brug
terbutalinsulfatinjektion anbefales ikke til patienter under 12 år på grund af utilstrækkelige kliniske data til at fastslå sikkerhed og effektivitet.
geriatrisk anvendelse
kliniske studier af terbutalinsulfatinjektion omfattede ikke tilstrækkeligt antal forsøgspersoner i alderen 65 år og derover til at afgøre, om de reagerer forskelligt fra yngre forsøgspersoner. Anden rapporteret klinisk erfaring har ikke identificeret forskelle i respons mellem ældre og yngre patienter. Generelt bør dosisvalg til en ældre patient være forsigtig, normalt startende i den lave ende af doseringsområdet, hvilket afspejler den større hyppighed af nedsat lever -, nyre-eller hjertefunktion og af samtidig sygdom eller anden lægemiddelbehandling.
bivirkninger
bivirkninger observeret med Terbutalinsulfatinjektion svarer til dem, der almindeligvis ses med andre sympatomimetiske midler. Alle disse reaktioner er forbigående og kræver normalt ikke behandling.
den følgende tabel sammenligner bivirkninger set hos patienter behandlet med Terbutalinsulfatinjektion (0,25 mg og 0,5 mg) med dem, der ses hos patienter behandlet med epinephrininjektion (0,25 mg og 0,5 mg) under otte dobbeltblinde crossover-studier, der involverede i alt 214 patienter.
| Incidence (%) of Adverse Reactions | |||||
| Terbutaline (%) | Epinephrine (%) | ||||
|
0.25 mg |
0.5 mg N = 205 |
0.25 mg N = 153 |
0.5 mg N = 61 |
||
| Reaction Central Nervous System |
|||||
| Tremor | 7.8 | 38.0 | 16.3 | 18.0 | |
| Nervousness | 16.9 | 30.7 | 8.5 | 31.1 | |
| Dizziness | 1.3 | 10.2 | 7.8 | 3.3 | |
| Headache | 7.8 | 8.8 | 3.3 | 9.8 | |
| Drowsiness | 11.7 | 9.8 | 14.4 | 8.2 | |
| Cardiovascular | |||||
| Palpitations | 7.8 | 22.9 | 7.8 | 29.5 | |
| Tachycardia | 1.3 | 1.5 | 2.6 | 0.0 | |
| Respiratory | |||||
| Dyspnea | 0.0 | 2.0 | 2.0 | 0.0 | |
| Chest discomfort | 1.3 | 1.5 | 2.6 | 0.0 | |
| Gastrointestinal | |||||
| Nausea/vomiting | 1.3 | 3.9 | 1.3 | 11.5 | |
| Systemic | |||||
| Weakness | 1.3 | 0.5 | 2.6 | 1.6 | |
| Flushed feeling | 0.0 | 2.4 | 1.3 | 0.0 | |
| Sweating | 0.0 | 2.4 | 0.0 | 0.0 | |
| Pain at injection site | 2.6 | 0.5 | 2.6 | 1.6 | |
bemærk: nogle patienter fik mere end en doseringsstyrke af terbutalinsulfat og epinephrin. Derudover var der rapporter om angst, muskelkramper og tør mund (< 0,5%). Der har været sjældne rapporter om stigninger i lever og overfølsomhedsvaskulitis ved administration af terbutalin.kontakt Hikma Pharmaceuticals USA Inc for at rapportere formodede bivirkninger.. ved 1-877-233-2001 eller FDA ved 1-800-FDA-1088 eller www.fda.gov/medwatch.
overdosering
den mediane dødelige sc-dosis af Terbutalinsulfat hos modne rotter var ca.165 mg/kg (ca. 2.700 gange den maksimale anbefalede daglige sc-dosis for voksne på mg / m2-basis). 2.000 mg/kg (ca.32.000 gange den maksimale anbefalede daglige sc-dosis for voksne på mg / m2-basis).
de forventede symptomer ved overdosering er symptomer på overdreven beta-adrenerg stimulering og / eller forekomst eller overdrivelse af nogen af de symptomer, der er anført under bivirkninger, f.eks. krampeanfald, angina, hypertension eller hypotension, takykardi med hastigheder på op til 200 slag i minuttet, arytmier, nervøsitet, hovedpine, rysten, mundtørhed, hjertebanken, kvalme, svimmelhed, træthed, utilpashed og søvnløshed. Hypokalæmi kan også forekomme. Der er ingen specifik modgift. Behandlingen består i seponering af Terbutalinsulfatinjektion sammen med passende symptomatisk behandling. Den fornuftige anvendelse af en kardioselektiv beta-receptorblokker kan overvejes under hensyntagen til, at sådan medicin kan producere bronchospasme. Der er ikke tilstrækkelig dokumentation til at afgøre, om dialyse er gavnlig for overdosering af Terbutalinsulfatinjektion.
Terbutalin Dosering og Administration
hætteglas bør kun anvendes til subkutan administration og ikke intravenøs infusion.
sterilitet og nøjagtig dosering kan ikke garanteres, hvis hætteglassene ikke anvendes i overensstemmelse med dosering og ADMINISTRATION.
Bortskaf ubrugt portion efter brug af en enkelt patient.
den sædvanlige subkutane dosis af terbutalinsulfatinjektion er 0,25 mg injiceret i det laterale deltoidområde. Hvis der ikke forekommer signifikant klinisk forbedring inden for 15 til 30 minutter, kan en anden dosis på 0, 25 mg administreres. Hvis patienten derefter ikke reagerer inden for yderligere 15 til 30 minutter, bør andre terapeutiske foranstaltninger overvejes. Den samlede dosis inden for 4 timer må ikke overstige 0,5 mg.
Bemærk: parenterale lægemidler skal inspiceres visuelt for partikler og misfarvning inden administration, Når opløsning og beholder tillader det.
hvordan leveres Terbutalin
Terbutalinsulfatinjektion, USP, 1 mg / mL, leveres i et volumen på 1 mL indeholdt i et 2 mL gult hætteglas. Hvert hætteglas indeholder 1 mg Terbutalinsulfat pr 1 mL opløsning; 0,25 mL opløsning vil give den sædvanlige kliniske dosis på 0,25 mg.
NDC 0143-9375-10 karton med 10 hætteglas.
opbevares ved 20 liter til 25 liter C (68 liter til 77 liter F) .
Beskyt mod lys ved at opbevare hætteglas i original karton, indtil de udleveres.
må ikke anvendes, hvis opløsningen er misfarvet.
Bortskaf ubrugt portion efter brug af en enkelt patient.
fremstillet af:
Hikma FARMACEUC LURUTICA (PORTUGAL), S. A..
Estrada do Rio Da M. L., N. L. 8, 8A E. 8B-Ferven L. L.,
2705 – 906 Terrugem SNT,
PORTUGAL
distribueret af:
Hikma Pharmaceuticals USA Inc. 07724 USA
Novaplus er et registreret varemærke tilhørende Visient, Inc.
revideret: Oktober 2020
PIN552-NOV/2
PRINCIPAL displaypanel
NDC 0143-9375-01 kun
Terbutalin
sulfat
injektion, USP
1 mg/mL
til subkutan
Brug kun

hoveddisplaypanel
NDC 0143-9375-10 kun
terbutalin
sulfat
injektion, USP
1 mg/ml
til subkutan
Brug kun
10 gange 1 ml enkeltdosishætteglas
steril, ikke-pyrogen, vandig
opløsning til subkutan injektion.
Må ikke anvendes, hvis opløsningen er misfarvet.
Bemærk: sædvanlig enkeltdosis er en fjerdedel
af hætteglassets indhold. SEE PRESCRIBING
INFORMATION.
SERIALIZATION IMAGE
| Terbutaline SULFATE Terbutaline sulfate injection |
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
|
|||||||||||||
Labeler – Hikma Pharmaceuticals USA Inc. (001230762)
Registrant – Hikma FARMACEUTICA (PORTUGAL), S. A. (452742943)
mere om terbutalin
- bivirkninger
- under graviditet eller amning
- doseringsinformation
- Lægemiddelbilleder
- lægemiddelinteraktioner
- Sammenlign alternativer
- prissætning & kuponer
- på Engelsk
- 11 anmeldelser
- drug class: adrenerge bronkodilatatorer
- FDA advarsler (1)
Forbrugerressourcer
- patientinformation
- Terbutalin (avanceret læsning)
- Terbutalin subkutan (avanceret læsning)
professionelle ressourcer
- ordineringsinformation
- Terbutalin (professionel patientrådgivning)
- terbutalin tabletter (FDA)
relaterede behandlingsvejledninger
- for tidlig fødsel
- allergisk astma
- astma, vedligeholdelse
- astma, akut
medicinsk ansvarsfraskrivelse