Svalové Plasticity
Kosterní svalstvo je největší tkáně v těle. Je vysoce plastický a může podstoupit dramatické nepatologické výkyvy hmoty i síly v reakci na nesčetné množství vlivů prostředí. Po cvičení odporu nebo vystavení anabolickým steroidům svaly podstupují hypertrofii a zvyšují její hmotnost, průřezovou plochu a sílu (Aagaard, 2004; Schiaffino a kol., 2013). Tyto stejné parametry mohou klesat strmě, když svaly zahájit atrofie v reakci na řadu urážky, které zahrnují: hladovění, denervation, imobilizace, sepse, rakovina, kachexie, srdeční selhání, diabetes, selhání ledvin, chronické obstrukční plicní onemocnění, syndrom získané imunodeficience (Schiaffino et al., 2013).
důsledky atrofie mají zjevné důsledky pro zdraví. Svalová slabost významně přispívá k úmrtnosti i morbiditě a je spojena se zvýšeným rizikem všech příčin úmrtí (Metter et al., 2002). Ve skutečnosti může snížení svalové atrofie u kachexie rakoviny významně prodloužit život (Zhou et al ., 2010). Stejně, mnoho starších lidí trpí z sarkopenie, vleklé svalové plýtvání onemocnění, které obvykle začíná po dosažení věku 50 let a zahrnuje ztrátu asi 1% svalové hmoty za rok (Woo, 2017). To znamená, že ve věku 80 let ztratili sarkopeničtí jedinci asi 40% své svalové hmoty, což je klíčový faktor při přijímání pádů, křehkosti a pečovatelského domu. V důsledku toho je pochopení mechanismů a potenciálních terapeutických odpovědí na atrofii široce základním a klinickým zájmem (Ali a Garcia, 2014; Cohen et al ., 2015; Ziaaldini a kol., 2017).
hypotéza Myonukleární domény
kosterní sval je poměrně unikátní v tom, že zralé buňky jsou syncytiální a mohou obsahovat stovky jader. Toto je nezbytná adaptace vzhledem k tomu, že jednotlivá svalová vlákna mohou být obrovská a dosahují délky až ~600 mm (23 palců) (např., 1998) a objemy, které mohou být více než 100 000krát větší než typická mononukleovaná buňka (Bruusgaard et al ., 2003). Příspěvky z více jader jsou nutné k produkci velkého množství mRNA potřeba přímé podivuhodnou syntézu bílkovin potřebné k vytvoření a zachování kontraktilní aparát (Nevalainen et al., 2013).
Oba plastové přírody svalu a jeho syncytiální organizace vyvolaly spor, který teprve v poslední době se zdá, že byl vyřešen—“myonuclear domény hypotéza“ (Qaisar a Larsson, 2014; Gundersen, 2016; Schwartz et al., 2016). Tato teorie má své kořeny v pojmu „Wirkungssphäre“ nebo „sféry vlivu“ navržené Strassburger (1893), v němž tvrdil, že jádro podporuje pouze diskrétní objem cytoplazmy, čímž se definuje horní hranice pro velikost buňky. Tento princip dále rozpracoval Gregory (2001), který tvrdil, že obsah a objem buněčné deoxyribonukleové kyseliny jsou pevně spojeny. Syncytiální povaha kosterního svalu pomáhá těmto buňkám překonat toto omezení. Hypotéza myonukleární domény diktuje, že za účelem udržení správného poměru jaderně-cytoplazmatického se během hypertrofie přidávají nová jádra a ztrácejí se atrofií.
existují značné údaje prokazující, že počet jaderných buněk se zvyšuje se svalovou hypertrofií (Moss, 1968; Cabric a James, 1983; Egner a kol., 2016), i když přetrvává určitá kontroverze (Murach et al., 2018). Tento proces byl oblastí intenzivního vyšetřování a nedávno byly definovány některé základní molekulární mechanismy, které regulují získávání nových jader během hypertrofie (Guerci et al ., 2012; Bentzinger a kol., 2014; Ross a kol., 2018). Tyto nadpočetné jádra jsou získány, když lineage-omezené kmenové buňky, typicky satelitní buňky, pojistka se svalová vlákna a přispívat jejich jádra (Brack a Rando, 2012; Bachman et al., 2018). Satelitní buňky jsou umístěny pod bazální membránou a přiléhají k sarkolemma (Katz, 1961; Mauro, 1961). Zůstávají v klidu, dokud stimulován buď anabolické steroidy, jako je testosteron nebo fokální poranění po cvičení odpor, na kterém místě oni vstoupit do buněčného cyklu a proliferace (Joubert a Tobin, 1995; Abreu et al., 2017). Některé z dceřiných buněk pojistku s svalových vláken a usnadnit opravy a růst, zatímco jiní zatčení a rozpuštění satelitní bazén (Dumont et al., 2015; Goh and Millay, 2017). Zbývající přebytečné buňky podstoupí apoptózu(Schwartz, 2008).
kontroverzním aspektem hypotézy myonukleární domény je tvrzení, že myonuklei jsou ztraceny během atrofie. Existuje mnoho intervencí, které vyvolávají atrofii na zvířecích modelech, včetně: imobilizace, denervace a sepse (Fitts et al., 1986; Minnaard a kol., 2005; O ‚ Leary et al., 2012). V každém případě dochází k čisté ztrátě plochy průřezu svalů (primární test)a vzhledu apoptotických buněk v tkáni (McCall et al., 1998; Smith a kol., 2000; Strasser a kol., 2000; Alway et al., 2003; McClung et al., 2007; Andrianjafiniony a kol., 2010; Guo et al., 2012; Palumbo et al., 2012; Barnes et al., 2015; Cheema a kol., 2015; Li a kol., 2016; Kletzien et al., 2018). V těchto studiích se apoptóza měří různými metodami, včetně aktivace kaspázy ,uvolňování mitochondriálních Endogů nebo fragmentace DNA. Tyto studie poskytují přesvědčivé údaje, že apoptóza se dramaticky zvyšuje během rané fáze atrofie. Například v nedávné komplexní studii (Guo et al., 2012), Guo a kol. předmětem myši na 14 dní odpružení zadní končetiny, léčba, která vyústila v ~69% snížení svalové mokré hmotnosti a ~43.8% snížení průřezové plochy vůči unmanipulated kontralaterální svaly. Autoři také kvantifikovat množství markerů apoptózy, včetně TUNEL barvení, kaspázy-3 štěpení/aktivace a štěpení poly(adenosin difosfát ribóza) polymerázy (PARP), což je protein zapojený do opravy DNA. Každé z těchto opatření apoptózy se významně zvýšilo po zavěšení zadních končetin. Zatímco hlavním cílem této práce bylo vyhodnotit pozitivní vliv elektrické stimulace na omezení atrofie následující urážka, oni a mnozí další výzkumníci interpretovat tyto druhy dat jako poskytuje silnou podporu pro myonuclear domény hypotéza.
z buněčného biologického hlediska představuje předpokládaná ztráta jader v syncytiální tkáni, jako je kosterní sval, hlavní praktický problém. Jak může jednotlivec jádro stal tak ohrožena, že její genom rychle kondenzuje a fragmenty, zatímco jeho sousedé přetrvávají a pomoci udržet životaschopnosti svalových vláken? Vzhledem k tomu, že apoptóza je obvykle zprostředkován aktivací třída cystein proteáz známý jako caspases, není jasné, jaký mechanismus by mohl sloužit k omezení činnosti difúzní proteázy ve společné cytoplazmě.
Tato otázka byla řešena nepřímo v jiném syncytiální typ buňky, lidské syncytiotrofoblast, tkáně, která obklopuje placenty a obsahuje asi 5 × 1010 jader (Mayhew a kol., 1999). Když je apoptóza indukována v syncytiotrofoblastu, šíří se jako vlna rychlostí asi 5 mikronů za minutu, dokud není zapojena celá tkáň (Longtine et al ., 2012). V důsledku toho neexistují žádné“ privilegované “ oblasti v syncytiální cytoplazmě a všechna jádra jsou nakonec zničena.
Jedním z klíčových problémů, s analýze apoptózy v kosterním svalu je, že je velmi heterogenní tkáň, kde se přibližně polovina jeho jader bydliště mimo svalových vláken (Schmalbruch a Hellhammer, 1977). Tyto mononukleované buňky zahrnují satelitní buňky, endotelové buňky, fibroblasty, pericyty a makrofágy (Tedesco et al ., 2010). V důsledku toho je velmi obtížné určit, na které straně sarkolemmy sídlí jádro, a tedy pokud je to skutečný myonukleus.
in vivo časosběrné zobrazování značených myších svalových vláken
navzdory velkému počtu článků prokazujících apoptózu během svalové atrofie několik autorů zpochybnilo tyto výsledky (Wada et al ., 2002; Zhong et al., 2005; Aravamudan et al., 2006; Gundersen a Bruusgaard, 2008; Duddy a kol., 2011; Qaisar a Larsson, 2014). Například pomocí izolovaných svalových vláken in vitro, Duddy et al. poznamenal, že zatímco objem svalových vláken se v průběhu času snižoval, což odráželo atrofický proces, Počet myonukleí se jevil jako stabilní (Duddy et al ., 2011).
V sérii elegantní experimenty, Gundersen laboratoře injekčně jednotlivých extensor digitorum longus (EDL) nebo soleus svalová vlákna, s barvivy, že nezávisle označené jádra a cytoplazmy v anestezovaných myší (Bruusgaard a Gundersen, 2008; Bruusgaard et al., 2010). To jim umožnilo identifikovat každé jádro v jednotlivých svalových vláknech in vivo v průběhu času a poté vyhodnotit jeho osud. Například EDL svaly byly indukovány k hypertrofii ablací jejich hlavních synergentů (Bruusgaard et al., 2010). Mezi dny 6 a 11, počet myonuclei zvýšil o 54% a mezi dny 9. a 14 bylo 35% nárůst v průřezu (Obrázek 1). Tyto údaje jsou v souladu s hypotézou, že svaly získávají nadpočetná jádra před hlavním růstem vlákna během hypertrofie.

Obrázek 1. Myonuklei se získávají během hypertrofie, ale neztrácejí se během atrofie u myší. Mikrografy stejného EDL svalového vlákna v průběhu času po indukci hypertrofie (Horní řada) a následné indukci atrofie(spodní řada). Fluorescenčně značené oligonukleotidy byly použity k vizualizaci jader in vivo. Tečkované čáry představují sarkolemmu. Měřítko = 50 µm . (Převzato z Bruusgaard et al., 2010. Používá se se svolením sborníku Národní akademie věd.)
poté zkoumali osud těchto jedinečně identifikovatelných myonukleí ve stejných svalových vláknech, když byli indukováni podstoupit atrofii. Denervace vedla k přibližně 50% snížení objemu svalových vláken, ale žádná ztráta myonukleí (Obrázek 1; Bruusgaard et al. , 2010). Nedodržení jaderné ztráta nebyla vzhledem k atrofické stimul zaměstnán od té doby byly získány stejné výsledky, když svaly byly vyvolané atrofie v reakci na tetrodotoxin-indukované nervové blokády, zadní končetiny pozastavení, rakovinné kachexie, nebo zadržen (Bruusgaard a Gundersen, 2008; Bruusgaard et al., 2010; Winje a kol., 2018a). Ve skutečnosti, v průběhu jejich studia, zkoumali více než 200 000 individuálních myonuclei v atrofické svaly a pozorovány pouze 4 TUNEL-pozitivní (apoptotických) jádra, které představuje ztrátu pouze ~0.002% z jádra (Bruusgaard et al., 2012). Tato data silně podporují hypotézu, že atrofie kosterního svalstva není doprovázena myonukleární smrtí.
hmyzí sval jako Model
jak silné jsou tyto studie, existují určitá omezení spojená s použitím savčích modelů. Za prvé, vždy se spoléhají na experimentální intervence, jako je denervace, k vyvolání svalové atrofie. Za druhé, kontralaterální sval se obvykle používá jako vnitřní kontrola, i když je také vystaven některým stejným environmentálním signálům,jako jsou stresové hormony (Bonaldo a Sandri, 2013). A konečně, kosterní svaly mohou během vývoje také podstoupit programovanou buněčnou smrt (PCD) a tyto modely zřídka řeší roli apoptózy v těchto buňkách.
alternativní model, který netrpí žádnou z těchto omezení, a umožňuje studium svalů jádra během obou atrofie a přirozeně se vyskytující PCD, je intersegmental svalu (ISM) z tabáku hawkmoth Manduca sexta. Ismy se skládají z listů obřích svalových vláken, kde každá buňka má délku asi 5 mm a průměr až 1 mm (obrázek 2A). ISMs připojit k segmentové hranice do břicha a vytvářet i procházení chování larvy a eclosion (vznik) chování dospělých můra, když unikne z pupal kůžičky na konci metamorfózy.
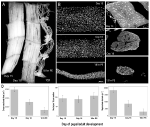
Obrázek 2. Retence myonukleí během atrofie i smrti intersegmentálních svalů (ISMs) z můry Manduca sexta. (A) ISMs ze tří fází vývoje: homeostatický (15. den vývoje pupal-dospělý; vlevo); atrofická (18. den; střední); a umírání (18 h po eklozi; vpravo). Měřítko se rovná ~1 mm (převzato z Schwartz et al., 2016). (B) ISMs z těchto stejných vývojových fází byly vyčištěny a obarveny jaderným barvivem DAPI a vizualizovány konfokální mikroskopií (převzato z Schwartz et al., 2016). C) sekce ISM vláken (10 µm) byly obarveny jaderným barvivem DAPI. Všimněte si dramatické ztráty svalových bílkovin (světle šedá oblast) během atrofie a smrti, ale retence jader ve všech fázích (převzato z Schwartz et al., 2016). (D) kvantifikace objemu ISM vláken (vlevo), jaderného čísla (uprostřed) a velikosti myonukleární domény (vpravo) během homeostázy, atrofie a smrti. (Střední ± standardní chyba.) (Převzato z Schwartz et al., 2016).
Na 15. den normální 18 dnů pupal-dospělý vývoj, ISMs zahájit hormonálně spustil program atrofie že výsledky v 40% ztráta hmotnosti v době eclosion 3 dny později (Obrázek 2A; Schwartz a Truman, 1983). Tato dramatická ztráta svalové hmoty je ekvivalentní ztrátě u 80letých jedinců se sarkopenií, ale probíhá spíše po dobu 3 dnů než 30 let. Zatímco ismy ztrácejí hmotnost, zachovávají si normální fyziologické vlastnosti,jako je klidový potenciál a síla / plocha průřezu (Schwartz a Ruff, 2002). ISMs jsou použity pro generování eclosion chování na konci dne 18 a pak zahájit soudržnosti POLITIK ve prospěch rozvoje, které jsou oba vyvolány peptidový hormon (Schwartz a Truman, 1982, 1983). .
na rozdíl od savčích svalů, ISMs neobsahují kapilár, satelitní buňky, endoteliální buňky či pericyty, což znamená, že prakticky ve všech jader ve tkáni pobývat sami svalová vlákna (Beaulaton a Lockshin, 1977). Použili jsme dvě nezávislé metody pro sledování jaderného osudu během atrofie i smrti v tomto modelu (Schwartz et al ., 2016). První byl standardní anatomický přístup. Když ismy podstoupí atrofii a smrt, dochází k dramatickému snížení objemu i plochy průřezu vláken ,ale hrubě se jaderné číslo nezměnilo (obrázek 2B). Pomocí řezu tkání pro kvantitativní studie jsme zjistili, že tam byl ~49% snížení vlákno průřezu během atrofie a dalších 30% pokles v raných fázích smrti (Obr. 2C,D; Schwartz et al., 2016). Počet jader se však během stejného období nezměnil, což znamená, že došlo k funkčnímu snížení myonukleární domény o 84%.
druhý způsob jsme použili, byl k měření obsahu DNA z jednotlivých svalových vláken ze zvířat na den 13, kdy jsou svaly homeostatický, až 18 h po-eclosion, když svaly jsou vysoce degenerované (Schwartz et al., 2016). Kvantifikovali jsme obsah DNA 420 jednotlivých buněk a zjistili jsme, že během vývoje nedošlo k žádné významné ztrátě. Tyto biochemické analýzy dobře souhlasí s anatomických dat a naznačují, že relativní koncentrace obou jader a funkčně genomické DNA se zvýšil, jak svaly atrofovaly a zemřel. V důsledku toho údaje z myší i můr naznačují, že svalová jádra nepodléhají apoptóze během atrofie (nebo PCD) a vedou k závěru, že hypotéza myonukleární domény by měla být odmítnuta.
Závěry
Tato pozorování mají řadu důsledků jak pro pochopení základní biologie svalů a pro rozvoj potenciálu terapeutických zásahů. Zatímco tam je značné vykazování údajů přítomnost apoptotických jader ve tkáni následující atrofické urážky, nedávné údaje naznačují, že tyto nejsou pravdivé myonuclei, ale spíše odsoudil mononukleární buňky, které jsou umístěny mimo svalových vláken. Hlavním důvodem pro tento rozdíl je, že tradiční nástroje používané pro detekci apoptózy nedostatek usnesení požadováno, aby odpovídajícím způsobem určit, na které straně sarcolemma umírající buňka nachází. Metody, které štítek myonuclei konkrétně, a to buď prostřednictvím in vivo injekce fluorescenčního barviva (Bruusgaard a Gundersen, 2008) nebo pomocí genetické manipulace vyjádřit značku proteinů (Duddy et al., 2011), odhalují jen málo, pokud vůbec nějaká apoptotická jádra uvnitř značených vláken. Nedávné demonstrace, že protilátky proti Proteinu Pericentriolar Materiál 1 (PCM1) štítek, pouze autentické myonuclei nabízí perspektivní nástroj, který může být aplikován na tradiční histologické materiály, které jsou běžně analyzovány v této oblasti (Winje et al., 2018b).
selhání kosterních svalů zaměstnat apoptózu jako mechanismus pro eliminaci myonukleí není překvapující. Zdá se, že zralý kosterního svalu je do značné míry vyloučeno zahájení apoptózy v tom, že upreguluje expresi silný přežití proteiny, jako je X-linked inhibitor apoptózy bílkovin (XIAP) (Smith et al., 2009) a represor apoptózy s doménou náboru kaspázy (ARC) (Xiao et al., 2011), zatímco současně vyjadřuje nízké hladiny mediátorů apoptózy jako apoptotických proteázy aktivující faktor 1 (Apaf-1) (Burgess et al., 1999). To dává smysl, teleologically, protože svaly jsou předmětem extrémní odchylky, včetně narušení sarcolemma po intenzivním cvičení, tak to by bylo katastrofální, kdyby se spouští buněčnou smrt, spíše než zahájeny opravy tkání a případně hypertrofie. Stejně jako jiné terminálně diferencované buňky mají svaly tendenci využívat neapoptotické mechanismy, zejména autofagické PCD (také známé jako degenerace typu II) (Clarke, 1990; Schwartz et al. , 1993; Kole a kol., 2013; Ginet a kol., 2014), když zemřou během vývoje.
i kdyby existoval mechanismus, kterým by svaly mohly selektivně cílit na jednotlivá jádra, není jasné, že by to bylo prospěšné. Ve skutečnosti, zachování „přebytek“ jádra během atrofie poskytuje výraznou výhodu pro jedince od kosterních svalů často procházejí cykly atrofie a hypertrofie v reakci na podmínky prostředí, jako je dostupnost potravin. Schopnost rychle se zotavit využitím již existujících myonukleí může sloužit důležitou roli v adaptaci (Jackson et al ., 2012) a pomáhají vysvětlit fenomén “ svalové paměti „(Staron et al., 1991; Gundersen, 2016). Je dobře zdokumentováno, v oblasti fyziologii cvičení, které je mnohem snazší získat určité úrovně svalového fitness prostřednictvím cvičení, než to bylo dosáhnout na první místo, i když tam byla dlouhá uplynulých období zadržen. Jinými slovy, fráze „použít nebo ztratit“ může být přesněji artikulována jako “ použít nebo ztratit, dokud na tom znovu nepracujete.“Tohle bylo demonstrováno přímo tím, že další experiment z Gundersen laboratoře, které prokázaly, že jakmile sval získala nového jádra, to udrží je dlouho po hypertrofické stimulace je odstraněn. Jsou vyvolané svalové hypertrofie u samic myší, tím, že zachází s nimi po dobu 2 týdnů s testosteronem a pak zkoumal svaly 3 týdny po vysazení steroidu (Egner et al., 2013). Svalový objem se vrátil na výchozí hodnotu, ale nově získaná jádra přetrvávala i o 3 měsíce později. Když svaly byly vystaveny přetížení na obnovení hypertrofie, steroidní léčených ty, rychle prošel 36% zvýšení vlákniny objem při řízení svaly rostly pouze o 6%. Tyto údaje naznačují, že „nadbytečná“ jádra by mohla být rychle mobilizována, aby se usnadnila rekvalifikace.
tato pozorování mají potenciální důsledky pro politiku veřejného zdraví. Bylo prokázáno, že růst svalů, fyziologické funkce a regenerační kapacita klesají s věkem, z velké části kvůli snížené proliferaci satelitních buněk (Blau et al ., 2015). V důsledku toho, cvičení během dospívání, kdy růst svalů, je obohacen o hormony, výživa a robustní satelitní bazénu, by mohlo funkčně sloužit umožnit jednotlivci, aby „banka“ myonuclei, která by mohla být vyčerpána, později v životě, zpomalit účinky stárnutí a případně zabránit sarkopenie.
kromě toho mají tyto údaje důsledky v oblasti soutěžních sportů. Použití anabolických steroidů je silným podnětem pro svalovou hypertrofii a přidání nových myonukleí (Egner et al ., 2013). Od těchto jader přetrvávat dlouho po užívání steroidů končí, sportovci pravděpodobností odvodit výhody nelegálních drog bez rizika detekce.
stručně řečeno, zatímco přidávání nových jader s svalový růst je do značné míry přijat, apoptotických ztráta jádra s atrofií nemohou být podporovány, což naznačuje, že striktní výklad myonuclear domény hypotéza nemůže být podporovány. Místo toho se zdá, že jakmile jsou získány, myonuklei přetrvávají, i když se sval stává atrofickým nebo iniciuje buněčnou smrt.
Autor Příspěvky
autor potvrzuje, že jediným přispěvatelem této práce a schválí ke zveřejnění.
financování
práce pro tuto publikaci byla podpořena finančními prostředky z Nadace profesorů Eugena m. a Ronnieho Isenberga. Autorovi nebyla poskytnuta žádná firemní podpora a nebyly zmíněny ani schváleny žádné komerční produkty.
Prohlášení o střetu zájmů
autor prohlašuje, že výzkum byl proveden bez jakýchkoli obchodních nebo finančních vztahů, které by mohly být vykládány jako potenciální střet zájmů.
Poděkování
autor by rád poděkoval Paní Christine Brown za pomoc při přípravě tohoto rukopisu a Eugene M. a Ronnie Isenberg Profesorem Nadace pro podporu.
Aagaard, P. (2004). Vytváření svalů „silnější“: cvičení, výživa, drogy. J.Muskuloskelet. Neuron. Komunikovat. 4, 165–174.
PubMed Abstraktní | Google Scholar
Abreu, P., Mendes, S. V., Ceccatto, V. M., a Hirabara, S. M. (2017). Aktivace satelitních buněk vyvolaná aerobní adaptací svalů v reakci na vytrvalostní cvičení u lidí a hlodavců. Life Sci. 170, 33–40. doi: 10.1016 / j. lfs.2016.11.016
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Ali, S., Garcia, J. M. (2014). Sarkopenie, kachexie a stárnutí: diagnóza, mechanismy a terapeutické možnosti-mini-recenze. Gerontologie 60, 294-305. doi: 10.1159/000356760
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Vždycky, S. E., Martyn, J. K., Ouyang, J., Chaudhrai, A., a Murlasits, Z. S. (2003). Id2 expression during apoptosis and satellite cell activation in unloaded and loaded quail skeletal muscles. Am. J. Physiol. Regul. Integr. Comp. Physiol. 284, R540–R549. doi: 10.1152/ajpregu.00550.2002
PubMed Abstract | CrossRef Full Text | Google Scholar
Andrianjafiniony, T., Dupre-Aucouturier, S., Letexier, D., Couchoux, H., and Desplanches, D. (2010). Oxidative stress, apoptosis, and proteolysis in skeletal muscle repair after unloading. Am. J. Phys. Cell Physiol. 299, C307–C315. doi: 10.1152/ajpcell.00069.2010
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Aravamudan, B., Mantilla, C. B., Zhan, W. Z., a Sieck, G. C. (2006). Denervační účinky na velikost myonukleární domény membránových vláken potkanů. J.Appl. Fyziol. 100, 1617–1622. doi: 10.1152 / japplphysiol.01277.2005
CrossRef Plný Text | Google Scholar
Bachman, J. F., Klose, A., Liu, W., Paříž, N. D., Blanc, R. S., Schmalz, M., et al. (2018). Prepubertální růst kosterního svalstva vyžaduje myonukleární příspěvek odvozený od satelitních buněk PAX 7. Vývoj 145: 167197.
Google Scholar
Barnes, B. T., se Svěřuje, A. L., Bohatá, M. M., a Dupont-Versteegden, E. E. (2015). Odlišné svalové apoptotické dráhy jsou aktivovány ve svalech s různými typy vláken v krysím modelu kritického onemocnění myopatie. J. Muscle Res. Cell Motil. 36, 243–253. doi: 10.1007/s10974-015-9410-8
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Beaulaton, J., a Lockshin, R. a. (1977). Ultrastrukturální studie normální degenerace intersegmental svaly Anthereae polyphemus a Manduca sexta (insecta, lepidoptera) se zvláštním zřetelem buněčné autofagie. J. Morphol. 154, 39–57. doi: 10.1002 / jmor.1051540104
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Bentzinger, C. F. von Maltzahn, J., Dumont, N. a., Stark, D. A., Wang, Y. X, Nhan, K., et al. (2014). Wnt 7a stimuluje pohyblivost a štěpení myogenních kmenových buněk, což vede ke zlepšení svalové síly. J. Cell Biol. 205, 97–111. doi: 10.1083 / jcb.201310035
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Blau, H. M., Cosgrove, B. D., a Ho, A. T. (2015). Ústřední úloha svalových kmenových buněk při regeneračním selhání se stárnutím. Adresa. Med. 21, 854–862. doi: 10.1038 / nm.3918
PubMed Abstract / CrossRef Full Text / Google Scholar
Bonaldo, P., and Sandri, m. (2013). Buněčné a molekulární mechanismy svalové atrofie. Dis. Model. Mech. 6, 25–39. doi: 10.1242 / dmm.010389
CrossRef Plný Text | Google Scholar
Brack, A. S., a Rando, T. a. (2012). Kmenové buňky specifické pro tkáň: poučení ze satelitní buňky kosterního svalstva. Buněčná Kmenová Buňka 10, 504-514. doi: 10.1016 / j. stem.2012.04.001
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Bruusgaard, J. C., Egner, I. M., Larsen, T. K., Dupre-Aucouturier, S., Desplanches, D., a Gundersen, K. (2012). Žádná změna myonukleárního počtu během vykládky a překládky svalů. J.Appl. Fyziol. 113, 290–296. doi: 10.1152 / japplphysiol.00436.2012
PubMed Abstract / CrossRef Full Text / Google Scholar
Bruusgaard, J. C., and Gundersen, k. (2008). In vivo časosběrná mikroskopie neodhalila žádnou ztrátu myších myonukleí během týdnů svalové atrofie. J. Clin. Investovat. 118, 1450–1457. doi: 10.1172/JCI34022
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Bruusgaard, J. C., Johansen, I. B., Egner, I. M., Rana, Z. A., a Gundersen, K. (2010). Myonuklei získané přetížením předcházejí hypertrofii a při zadržování se neztratí. Proc. Natle. Acad. Věda. USA 107, 15111-15116. doi: 10.1073 / pnas.0913935107
CrossRef Full Text / Google Scholar
Bruusgaard, J. C., Liestol, k., Ekmark, m., Kollstad, K., and Gundersen, k. (2003). Počet a prostorové rozložení jader ve svalových vláknech normálních myší studovaných in vivo. J. Physiol. 551, 467–478. doi: 10.1113 / jphysiol.2003.045328
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Burgess, D. H., Svensson, M., Dandrea, T., Gronlund, K., Hammarquist, F., Orrenius, S., et al. (1999). Cytosoly lidského kosterního svalstva jsou refrakterní na aktivaci kaspáz typu II závislou na cytochromu c a postrádají APAF-1. Buněčná Smrt Se Liší. 6, 256–261. doi: 10.1038 / sj.cdd.4400489
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Cabric, M., a James, N. T. (1983). Morfometrické analýzy svalů cvičených a netrénovaných psů. Rána. J. Anat. 166, 359–368. DOI: 10.1002 / aja.1001660309
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Cheema, N., Herbst, A., McKenzie, D., a Aiken, J. M. (2015). Apoptóza a nekróza zprostředkovávají ztrátu vláken kosterního svalstva u mitochondriálních enzymatických abnormalit vyvolaných věkem. Stárnoucí Buňka 14, 1085-1093. doi: 10.1111/acel.12399
PubMed Abstract | CrossRef Full Text | Google Scholar
Clarke, P.G. (1990). Vývojová buněčná smrt: morfologická rozmanitost a více mechanismů. Anat. Embryol. 181, 195–213.
Google Scholar
Cohen, s., Nathan, J. A., and Goldberg, a. L. (2015). Ztráta svalů při onemocnění: molekulární mechanismy a slibné terapie. Adresa. Rev. Drug Discov. 14, 58–74. doi: 10.1038/nrd4467
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Duddy, W. J., Cohen, T., Duguez, a. S., a Koroptev, T. a. (2011). Izolované svalové vlákno jako model nepoužívané atrofie: charakterizace pomocí PhAct, metoda kvantifikace f-aktinu. Expo. Cell Res.317, 1979-1993. doi: 10.1016 / j. yexcr.2011.05.013
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Dumont, N. a., Wang, Y. X, a Rudnicki, M. a. (2015). Vnitřní a vnější mechanismy regulující funkci satelitních buněk. Vývoj 142, 1572-1581. doi: 10.1242 / dev.114223
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Egner, I. M., Bruusgaard, J. C., Eftestol, E., a Gundersen, K. (2013). Mechanismus buněčné paměti pomáhá hypertrofii přetížení ve svalech dlouho po epizodické expozici anabolickým steroidům. J. Physiol. 591, 6221–6230. doi: 10.1113 / jphysiol.2013.264457
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Egner, I. M., Bruusgaard, J. C., a Gundersen, K. (2016). Vyčerpání satelitních buněk zabraňuje hypertrofii vláken v kosterním svalu. Vývoj 143, 2898-2906. doi: 10.1242 / dev.134411
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Fitts, R. H., Metzger, J. M., Riley, D. A., a Unsworth, B. R. (1986). Modely nepoužívání: srovnání zavěšení zadních končetin a imobilizace. J.Appl. Fyziol. 60, 1946–1953.
Google Scholar
Ginet, V., Pittet, M. P., Rummel, C., Osterheld, M. C., Meuli, R., Clarke, P. G., et al. (2014). Umírající neurony v thalamu udušených novorozenců a potkanů jsou autofagické. Anna. Neurol. 76, 695–711. DOI: 10.1002 / ana.24257
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Goh, Q, a Millay, D. P. (2017). Požadavek fúze kmenových buněk zprostředkované myomakerem pro hypertrofii kosterního svalstva. elife 6. diváci: 10.7554 / eLife.20007
PubMed Abstract / CrossRef Full Text / Google Scholar
Gregory, T. R. (2001). Náhoda, koevoluce, nebo příčinná souvislost? Obsah DNA, velikost buněk a C-hodnota enigma. Biol. Reverend Camb. Philos. SOC. 76, 65–101. doi: 10.1017/s1464793100005595
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Guerci, A., Lahoute, C., Hebrard, S., Collard, L., Graindorge, D., Favier, M., et al. (2012). Parakrinní signály závislé na Srf produkované myofibery řídí hypertrofii kosterního svalstva zprostředkovanou satelitními buňkami. Metab Buňky. 15, 25–37. doi: 10.1016 / j. cmet.2011.12.001
PubMed Abstract / CrossRef Full Text / Google Scholar
Gundersen, K. (2016). Svalová paměť a nový buněčný model svalové atrofie a hypertrofie. J.Exp. Biol. 219, 235–242. doi: 10.1242 / jeb.124495
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Gundersen, K., a Bruusgaard, J. C. (2008). Jaderné domény během svalové atrofie: jádra ztracena nebo paradigma ztracena? J. Physiol. 586, 2675–2681. doi: 10.1113 / jphysiol.2008.154369
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Guo, B. S., Cheung, K. K., Yeung, S. S., Zhang, B. T., a Yeung, E. W. (2012). Elektrická stimulace ovlivňuje proliferaci satelitních buněk a apoptózu při atrofii svalů indukované vykládkou u myší. PLoS One 7: e30348. doi: 10.1371 / deník.pone.0053523
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Jackson, J. R., Mula, J., Kirby, T. J., Fry, C. S. Lee, J. D., Ubele, M. F., et al. (2012). Deplece satelitních buněk neinhibuje opětovný růst kosterního svalstva dospělých po atrofii vyvolané vykládkou. Rána. J.Phys. Buněčný Fyziol. 303, C854-C861. doi: 10.1152 / ajpcell.00207.2012
PubMed Abstract / CrossRef Full Text / Google Scholar
Joubert, Y., and Tobin, C. (1995). Léčba testosteronem vede k aktivaci klidových satelitních buněk a jejich rekrutování do buněčného cyklu ve svalu levator ani u potkanů. Rozvoj. Biol. 169, 286–294. doi: 10.1006 / dbio.1995.1144
PubMed Abstract / CrossRef Full Text / Google Scholar
Katz, B. (1961). Ukončení aferentního nervového vlákna ve svalovém vřetenu žáby. Philos. Trans. R.Soc. Londe. B Biol. Věda. 243, 221–240.
PubMed Abstract / Google Scholar
Kletzien, h., Hare, a. J., Leverson, G., and Connor, N. P. (2018). Vliv buněčné smrti související s věkem na morfologii a počet vláken ve svalu jazyka. Svalový Nerv 57, E29-E37. doi: 10.1002 / mus.25671
PubMed Abstract / CrossRef Full Text / Google Scholar
Kole, a. J., Annis, R. P., and Deshmukh, m. (2013). Zralé neurony: vybavené pro přežití. Cell Death Dis. 4: e689. doi: 10.1038 / cddis.2013.220
PubMed Abstract / CrossRef Full Text / Google Scholar
Li, T. S., Shi, h., Wang, L., and Yan, C. (2016). Vliv mezenchymálních kmenových buněk kostní dřeně na proliferaci satelitních buněk a apoptózu u svalové atrofie vyvolané imobilizací u potkanů. Med. Věda. Monite. 22, 4651–4660. doi: 10.12659 / MSM.898137
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Lockshin, R. a., Williams, C. M. (1965). Programovaná buněčná smrt – i. cytologie degenerace v intersegmentálních svalech pernyi silkmoth. J. Fyziol Hmyzu. 11, 123–133. doi: 10.1016/0022-1910(65)90099-5
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Longtine, M. S., Barton, A., Chen, B., Nelson, D. M. (2012). Zobrazování živých buněk ukazuje, že apoptóza se iniciuje lokálně a šíří se jako vlna skrz syncytiotrofoblasty v primárních kulturách lidských placentárních klkových trofoblastů. Placenta 33, 971-976. doi: 10.1016 / j. placenta.2012.09.013
PubMed Abstract / CrossRef Full Text / Google Scholar
Mauro, a. (1961). Satelitní buňka vláken kosterního svalstva. J. Biophys. Biochem. Cytol. 9, 493–495.
Google Scholar
Mayhew, T. M., Leach, L., McGee, R., Ismail, W. W., Myklebust, R., a Lammiman, M. J. (1999). Proliferace, diferenciace a apoptóza ve vilózním trofoblastu ve 13-41 týdnech těhotenství(včetně pozorování prstencových lamel a komplexů jaderných pórů). Placenta 20, 407-422. doi: 10.1053 / místo.1999.0399.
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
McCall, G. E. Allen, D. L., Linderman, J. K., Grindeland, R. E., Roy, R. R., Mukku, V. R., et al. (1998). Udržování velikosti myonukleární domény u potkaních soleus po přetížení a léčbě růstovým hormonem / IGF-I. J.Appl. Fyziol. 84, 1407–1412.
Google Scholar
McClung, J. M., Kavazis, a. N., DeRuisseau, K. C., Falk, D. J., Deering, m. a., Lee, y., et al. (2007). Kaspáza – 3 regulace membránové myonukleární domény během atrofie vyvolané mechanickou ventilací. Rána. J. Respir. Zásah. Péče Med. 175, 150–159. doi: 10.1164 / rccm.200601-142OC
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Metter, E. J. Talbot, L. a., Schrager, M., a Conwit, R. (2002). Síla kosterního svalstva jako prediktor mortality ze všech příčin u zdravých mužů. J. Gerontol. Biol. Věda. Med. Věda. 57, B359-B365. doi: 10.1093 / gerona / 57.10.B359
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Minnaard, R., Drost, M. R., Wagenmakers, a. J., van Kranenburg, G. P., Kuipers, H., a Hesselink, M. K. (2005). Ztráta kosterního svalstva a kontraktilní výkon u septických potkanů. Svalový Nerv 31, 339-348. doi: 10.1002 / mus.20268
PubMed Abstract / CrossRef Full Text / Google Scholar
Moss, F. P. (1968). Vztah mezi rozměry vláken a počtem jader během normálního růstu kosterního svalstva u drůbeže domácí. Rána. J. Anat. 122, 555–563. DOI: 10.1002 / aja.1001220308
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Murach, a. K. A., Englund, D. A., Dupont-Versteegden, e. E. McCarthy, j. J., Peterson, C. a. (2018). Flexibilita myonukleární domény zpochybňuje rigidní předpoklady o příspěvku satelitních buněk k hypertrofii vláken kosterního svalstva. Před. Fyziol. 9:635. doi: 10.3389 / fphys.2018.00635
CrossRef Full Text / Google Scholar
Nevalainen, m., Kaakinen, M., and Metsikko, k. (2013). Distribuce transkriptů mRNA a translační aktivity v kosterních myofiberech. Cell Tissue Res.353, 539-548. doi: 10.1007/s00441-013-1659-x
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
O ‚ leary, M. F., Vainshtein, A., Carter, H. N., Zhang, Y., a Kapuce, D. A. (2012). Mitochondriální dysfunkce vyvolaná denervací a autofagie v kosterním svalu zvířat s deficitem apoptózy. Rána. J.Phys. Buněčný Fyziol. 303, C447-C454. doi: 10.1152/ajpcell.00451.2011
PubMed Abstract | CrossRef Full Text | Google Scholar
Palumbo, C., Rovesta, C., and Ferretti, M. (2012). Striated muscle fiber apoptosis after experimental tendon lesion in a rat model. J. Anat. 221, 358–363. doi: 10.1111/j.1469-7580.2012.01554.x
PubMed Abstract | CrossRef Full Text | Google Scholar
Qaisar, R., and Larsson, L. (2014). What determines myonuclear domain size? Indian J. Physiol. Pharmacol. 58, 1–12.
PubMed Abstract | Google Scholar
Ross, J. A., Levy, Y., Svensson, K., Philp, a., Schenk, s., and Ochala, J. (2018). SIRT1 reguluje jaderné číslo a velikost domény ve vláknech kosterního svalstva. J.Cell. Fyziol. 233, 7157–7163. doi: 10.1002 / jcp.26542
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Schiaffino, S., Dyar, K. a., Ciciliot, S., Blaauw, B., a Sandri, M. (2013). Mechanismy regulující růst a atrofii kosterního svalstva. FEBS j. 280, 4294-4314. doi: 10.1111 / febs.12253
PubMed Abstract / CrossRef Full Text / Google Scholar
Schmalbruch, H., and Hellhammer, u. (1977). Počet jader ve svalech dospělých potkanů se zvláštním odkazem na satelitní buňky. Anat. Záznam. 189, 169–175. doi: 10.1002 / ar.1091890204
PubMed Abstract | CrossRef Full Text | Google Scholar
Schwartz, L.M. (2008). Atrofie a programovaná buněčná smrt kosterního svalstva. Buněčná Smrt Se Liší. 15, 1163–1169. doi: 10.1038 / cdd.2008.68
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Schwartz, L. M., Brown, C., McLaughlin, K., Smith, W., a Bigelow, C. (2016). Myonukleární doména není udržována v kosterním svalu během atrofie ani programované buněčné smrti. Rána. J.Phys. Buněčný Fyziol. 311, C607–C615. doi: 10.1152 / ajpcell.00176.2016
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Schwartz, L. M., a Ruff, R. L. (2002). Změny kontraktilních vlastností kosterního svalstva během vývojově programované atrofie a smrti. Rána. J.Phys. Buněčný Fyziol. 282, C1270–C1277. doi: 10.1152 / ajpcell.01275.2000
CrossRef Plný Text | Google Scholar
Schwartz, L. M., Smith, S. W., Jones, M. E., a Osborne, B.a. (1993). Dochází ke všem programovaným buněčným úmrtím prostřednictvím apoptózy? Proc. Natle. Acad. Věda. U. S. A. 90, 980-984.
Google Scholar
Schwartz, L. M., and Truman, J. W. (1983). Hormonální kontrola rychlosti metamorfního vývoje u tabákových hornworm Manduca sexta. Rozvoj. Biol. 99, 103–114. doi: 10.1016/0012-1606(83)90257-9
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Schwartz, L. M., a Truman, J. W. (1982). Peptidová a steroidní regulace svalové degenerace u hmyzu. Věda 215, 1420-1421. doi: 10.1126 / věda.6278594
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Smith, H. K., Maxwell, L., Martyn, J. a., a Bass, j. J. (2000). Fragmentace jaderné DNA a morfologické změny v kosterním svalu dospělých králíků po krátkodobé imobilizaci. Buněčná Tkáň Res.302, 235-241. doi: 10.1007/s004410000280
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Smith, M. l., Huang, Y. Y., a Deshmukh, M. (2009). Diferenciace kosterního svalstva evokuje endogenní XIAP k omezení apoptotické dráhy. PLoS One 4: e5097. doi: 10.1371 / deník.pone.0005097
CrossRef Plný Text / Google Scholar
Staron, R. S., Leonardi, M. J., Karapondo, D. L., Malicky, E. S., Falkel, J. E., Hagerman, F. C., et al. (1991). Adaptace síly a kosterního svalstva u žen vyškolených v těžké odolnosti po zadržení a rekvalifikaci. J.Appl. Fyziol. 70, 631-640.
Google Scholar
Strassburger, e. (1893). Oblast působení jader a velikost buněk. Histol Beitr. 5, 97-124.
Google Scholar
Strasser, h., Tiefenthaler, m., Steinlechner, m., Eder, i., Bartsch, G., and Konwalinka, G. (2000). Apoptóza závislá na věku a ztráta rabdosfinkterových buněk. J. Urola. 164, 1781–1785. doi: 10.1016/S0022-5347(05)67106-6
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Tedesco, F. S. Dellavalle, A., Diaz-Manera, J., Messina, G., a Cossu, G. (2010). Oprava kosterního svalu: regenerační potenciál kmenových buněk kosterního svalu. J. Clin. Investovat. 120, 11–19. doi: 10.1172/JCI40373
PubMed Abstract | CrossRef Full Text/Google Scholar
Wada, K. I., Takahashi, h., Katsuta, s., and Soya, h. (2002). Žádné snížení myonukleárního počtu po dlouhodobé denervaci u dospělých myší. Rána. J.Phys. Buněčný Fyziol. 283, C484-C488. doi: 10.1152 / ajpcell.00025.2002
CrossRef Plný Text | Google Scholar
Winje, I. M., Sheng, X, Hansson, K. a., Solbrå, A., Tennøe, S., Saatcioglu, F., et al. (2018a). Kachexie nevyvolává ztrátu myonukleárních nebo svalových vláken během xenografovaného karcinomu prostaty u myší. Acta Physiol. e13204. doi: 10.1111 / apha.13204
CrossRef Full Text | Google Scholar
Winje, I. m., Bengtsen, m., Eftestol, e., Juvkam, i., Bruusgaard, J. C., and Gundersen, k. (2018b). Specifické značení myonukleí protilátkou proti pericentriolárnímu materiálu 1 na úsecích tkáně kosterního svalstva. Acta Physiol. 223: e13034. doi: 10.1111 / apha.13034
CrossRef Full Text / Google Scholar
Woo, J. (2017). Sarkopenie. Cline. Geriatr. Med. 33, 305–314. doi: 10.1016 / j. cger.2010.02.012
CrossRef Full Text | Google Scholar
Xiao, R., Ferry, a. L., and Dupont-Versteegden, E.E. (2011). Buněčná rezistence diferencovaných myotubů je spojena se zvýšenými antiapoptotickými mechanismy ve srovnání s myoblasty. Apoptóza 16, 221-234. doi: 10.1007/s10495-010-0566-9
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Yang, D., Morris, S. F., a Sigurdson, L. (1998). Sartorius sval: anatomické úvahy pro rekonstrukční chirurgy. Chirurg Radiol. Anat. 20, 307–310. doi: 10.1007
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Zhong, H., Roy, R. R., Siengthai, B., a Edgerton, V. R. (2005). Účinky nečinnosti na velikost vlákna a myonukleární číslo ve svalu potkana soleuse. J.Appl. Fyziol. 99, 1494–1499. doi: 10.1152 / japplphysiol.00394.2005
CrossRef Plný Text | Google Scholar
Zhou, X. Wang, J. L., Lu, J., Song, Y., Kwak, K. S., Jiao, Q., et al. (2010). Zvrácení kachexie rakoviny a svalové ztráty antagonismem act RIIB vede k prodlouženému přežití. Cela 142, 531-543. doi: 10.1016 / j. buňka.2010.07.011
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Ziaaldini, M. M., Marzetti, E., Picca, A., a Murlasits, Z. (2017). Biochemické dráhy sarkopenie a jejich modulace fyzickým cvičením: narativní přehled. Před. Med. 4:167. doi: 10.3389 / fmed.2017.00167
CrossRef Full Text / Google Scholar