Na začátku XIX. století, von Reckingausen zjištěno, že krevní cévy byly pokryty listu buňky. Tato jednobuněčná tlustá vrstva je tvořena endoteliálními buňkami, které lemují vnitřní povrch krve a lymfatických cév. U lidí se odhaduje, že celkový povrch endotelové vrstvy je asi 35 m2 a že existuje asi 1 až 1,6 103 endotelových buněk. Celková délka tepen, žil a kapilár je asi 90000 km (více než dvakrát cestovat po celém světě). Endotelové buňky jsou ploché a vzájemně propojené buněčnými spoji. Jejich hlavní funkcí je jako prostředník mezi krví a ostatními tkáněmi a přispívá k vlastnostem krve, a to jak v normálních, tak v patologických tkáních. Jsou také důležité pro výměnu imunitních buněk mezi krví a tkáněmi.
1. Morfologie
endotelové buňky jsou velmi zploštělé buňky, natolik, že jejich jádro je vyšší strukturou buňky, i když je jádro také zploštělé. Buněčný tvar je přizpůsoben kanálu endoteliální buňka je podšívka (Obrázek 1, 2 a 3). V užších kapilárách mohou endotelové buňky rozšířit svou cytoplazmu po celém obvodu krevní cévy, takže kanál je řada endotelových buněk. Ve větších kanálech, jako jsou tepny a žíly, je pro pokrytí celkového obvodu kanálu zapotřebí mnoho endotelových buněk.
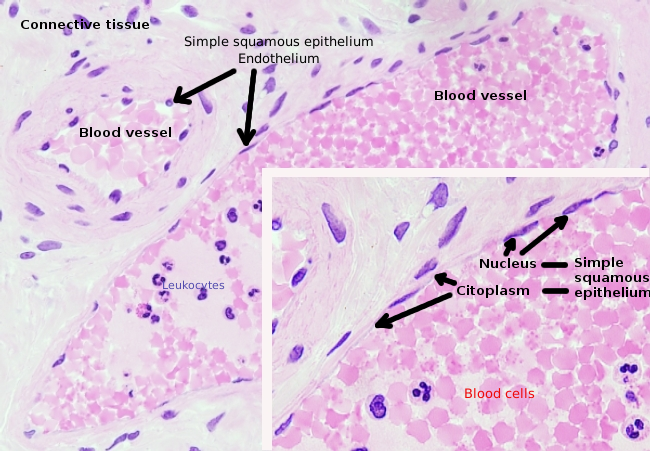
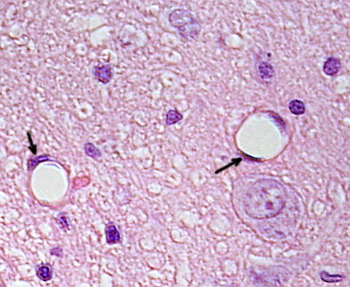
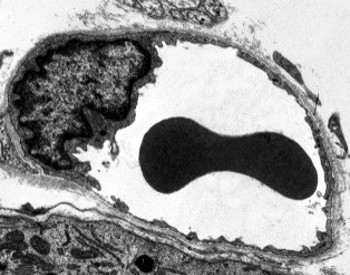
Perinukleární cytoplazmě obsahuje většinu mitochondrie a další organely jako Golgiho aparát, vzhledem k tomu, že periferie cytoplazmě jsou tenčí a má málo organel, i když endoplazmatické retikulum lze nalézt v blízkosti plazmatické membrány. Endotelové buňky mají mnoho vezikul, většina z nich jsou endocytární vezikuly.
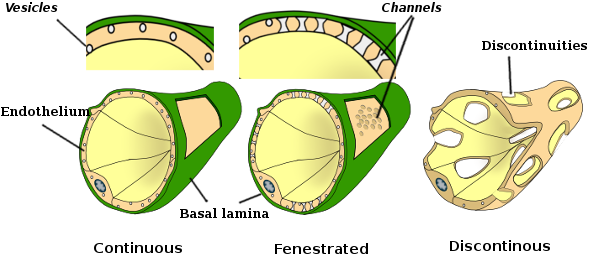
V některých oblastech, jako jsou játra, ledviny, kůry, a endokrinní žlázy, endotelové buňky kapilár show póry nebo malé dírky, známý jako fenestratrions. Jsou to dráhy o průměru asi 60 až 70 nm, s úzkým průchodem asi 5 nm, které přímo komunikují krev a lymfy s ostatními tkáněmi. Kapiláry mající tyto typy endotelových buněk jsou známé jako fenestrované kapiláry. Póry jsou distribuovány ve skupinách a jejich hustota závisí na typu endotelu.
endotelové buňky jsou odděleny od okolní tkáně vrstvou extracelulární matrice zvané bazální lamina. Endoteliální buňky přispívají k této vrstvy s proteiny, lamininu, fibronektinu a kolagenu typu II, IV a V.
Zdroj a šíření
Vasculogenesis je tvorba nových endotelových buněk v tkáních s žádnou již existující krevní cévy. Stává se to v embryu. U dospělých a také u embryí se z již přítomných krevních cév vytvářejí nové krevní cévy, a tedy nové endotelové buňky. Tento proces je známý jako angiogeneze. Nové endotelové buňky se produkují větvením nebo dělením krve a lymfatických cév. Angiogeneze je běžné v rostoucí tkáně, nebo ty, pod těžkou přestavby, jako dělohy v savčích samic, nebo v patologických stavů, jako jsou nádory, záněty a rány.
Vaskulogeneze
první endotelové buňky savců jsou generovány po gastrulaci během vývoje embrya. Odlišují se od buněk zvaných angioblasty, tvoří skupiny a organizují se v krátkých krevních cévách. Tento proces se nejprve děje ve vitelinovém vaku embrya. Tyto počáteční krevní cévy rostou a spojují se mezi sebou a vytvářejí síť. Později rekrutují fibroblasty a svalové buňky. Tato počáteční síť prochází průběžným procesem remodelace během dalších vývojových fází. U embryí jsou všechny endotelové buňky zpočátku podobné, ale později se diferencují v endotelu žíly, tepny, kapiláry a lymfatických cév. Několik molekul jako FGF2, BMP4, IHH a VEGF indukuje oddělené diferenciační dráhy. Induktor Notch se jeví jako velmi důležitý, protože vede k endotelu tepny, zatímco jeho inhibice vede k endotelu žíly. Lymfatický endotel je tvořen z endotelu kardinální žíly a potřebuje expresi COUPF-II a SOX18. Kromě toho je endotel diferencován podle orgánu, ve kterém je umístěn. Například, endotel tvoří pevně uzavřené vrstvy v mozku tvoří bariéru krev-mozek, vzhledem k tomu, že je fenestrované volně organizované v játrech upřednostňovat výměnu molekul s krví.
Jako endoteliální buňky jsou stále organizovány v tepny a žíly cest, některých endoteliálních buňkách vyvolávají krvetvorných buněk do diferenciační proces známý jako endoteliální-krvetvorných přechod (EHT). Tento proces se také děje v některých dospělých tkáních, jako je při tvorbě placenty a dalších tkání během těhotenství.
angiogeneze
angiogeneze je tvorba nových krevních cév a endotelu větvením nebo dělením již existujících krevních cév. U dospělých je rychlost proliferace endotelových buněk velmi nízká. Například u savců se endoteliální buňka může rozdělit jednou za měsíc nebo může čekat několik let. To znamená, že angiogeneze je vzácná v tkáních za normální fyziologie, s výjimkou ženských reprodukčních orgánů. Může se však aktivovat v patologických procesech, jako jsou poškození tkání a nádory. Některé látky indukují angiogenezi, jako je endoteliální růstový faktor (EGF), kyselý EGF, fibroblastový růstový faktor (FGF), transformující růstový faktor (TGF) a prostaglandiny. Angiogeneze začíná, když se angiogenní látky uvolňují z okolních tkání. Endoteliální buňka blízké krevní cévy, obvykle z venule, začne migrovat do angiogenního zdroje signálu a táhne další endotelové buňky, které se začnou proliferovat a tvořit novou cévu. Tyto endotelové buňky přechodně ztrácejí své těsné spojení, což vede k odhalení bazální membrány, která je rychle trávena enzymy uvolňovanými z endotelových buněk. Některé endotelové buňky procházejí trávenou bazální membránou, zatímco proliferace pokračuje. Celý tento proces umožňuje prodloužení a větvení nové krevní cévy, dokud signál vaskulogeneze nezmizí. Špičky krevních cév se spojí s jinými krevními cévami, aby vytvořily uzavřené obvody a umožnily tok krve bez mrtvých zakončení.
oblasti s progenitory endoteliálních buněk byly nalezeny v dorzální aortě a endokardu. Mezenchymální buňky mohou být odlišeny od endotelových buněk endokardu a tvoří trikuspidální chlopeň a některé fibroblasty srdce, ale ne kardiomiocyty. Endotelové buňky jsou tak citlivé na vnější signály, že udržování integrity endotelu je aktivní proces, který je zprostředkován jinými signály, jako je FGF. Aktivní proces není jen pro integritu, ale také pro udržení buněčného fenotypu. Když endotelové buňky nepřijímají správné signály, zemřou apoptózou nebo se stanou mezenchymálními buňkami, které mohou syntetizovat hojnou extracelulární matrici. Přechod z endotelu na mezenchymální buňku je za některými chorobami, jako je arterioskleróza a vláknitá miokarditida.
funkce
myšlenka, že endotel je jen pasivní výstelka lymfatických a krevních cév, musí být změněna. Funkce endotelu jsou pro organismus rozmanité a nezbytné. Ve skutečnosti, to je fyzické struktury kardiovaskulárního a lymfatického potrubí, ale také reguluje výměny molekul mezi průsvitu cév a okolních tkání, a to ovlivňuje fyziologické vlastnosti krve. Kromě fyzické bariéry se endotelové buňky vyvíjejí sekreční, metabolické a imunitní funkce. Mění své fyziologické chování ovlivněné molekulami, jako jsou růstové faktory, koagulanty a antikoagulancia, lipoproteiny s nízkou hustotou, oxid dusnatý, serotonin, enkefalin a mnoho dalších. Endotelové buňky mají receptory pro všechny tyto látky.
bariéra
endotelové buňky tvoří vrstvu, která obvykle působí jako bariéra mezi krví a okolními tkáněmi. Soudržnost mezi endoteliálními buňkami je splněna buněčnými křižovatkami, jako jsou těsné křižovatky a přilnavé křižovatky. Byly také pozorovány mezery, i když jejich hlavní funkcí je komunikace mezi sousedními buňkami. Endotelové buňky mohou modulovat tyto adheze a měnit propustnost bariéry, která může ovlivnit nejen molekuly, ale také buňky překračující endotel. V některých orgánech, jako jsou játra, jsou však endotelové buňky mnohem volněji zabaleny a ponechávají mnoho volného prostoru, takže endotel lze jen stěží považovat za bariéru.
transmisní elektronové mikroskopické snímky ukazují mnoho vezikul v cytoplazmě endotelových buněk. Oni jsou myšlenka být zapojen v intracelulární transport mezi apikální (směrem do krve) a bazolaterální membrány (směrem k bazální lamina). Tento typ dopravy je známý jako transkytóza. Je zajímavé, že transcytózní vezikuly jsou hojnější v endotelových buňkách kapilár než v buňkách větších krevních cév. Znamená to, že endotelové buňky v kapilárách mají intenzivnější výměnu molekul mezi krví a tkáněmi, zatímco v nádobách s velkým průměrem se podílejí hlavně na vedení krve. Některé endoteliální buňky, známé jako fenestrované, póry nebo velmi malé kanálky, které se přímo připojit krve s okolní tkání, což umožňuje některé malé velikosti molekul přes endotel bez vstupu do cytoplazmy nějaké endoteliálních buněk (Obrázek 4). Konečně existují orgány s velmi propustným endotelem. V játrech jsou sinusoidy krevní cévy, kde endotelové buňky opouštějí volný prostor mezi sebou a funkce jako bariéra sotva existuje.
mnoho typů buněk cestuje v krvi směrem k cílovým orgánům v těle. Tam procházejí endotelem krevních cév, obvykle na úrovni postkapilárních žil. To znamená, že endotelové buňky musí modifikovat buněčné spoje tak, aby buňky procházely endotelovou vrstvou. Leukocyty vystupují z krevní cévy rozpoznáním a ukotvením ke specifickým molekulám apikální membrány endotelových buněk. Selektiny, integriny a imunoglobuliny jsou zodpovědné za rozpoznávání a adhezi leukocytů k endotelové vrstvě. Selektiny začínají ukotvovat leukocyty, které se valí přes endoteliální povrch. Tato počáteční adheze je slabá a reverzibilní.
mnoho leukocytů opouští krev během zánětlivých procesů a pohybuje se do postižených tkání. Chemokiny jsou molekuly atraktivní pro leukocyty, které jsou uvolňovány poškozenými tkáněmi a spojeny s glykokalixem endotelových buněk. Aktivují se leukocyty valící se po endoteliálním povrchu s chemokiny, adheze buněk a buněk se zesílí a leukocyty zůstávají na místě. Aktivace leukocytů vede k aktivaci jeho integrinů, které rozpoznávají imunoglobuliny endotelové buňky. Tyto imunoglobuliny jsou exprimovány v membránách endotelových buněk po aktivaci buňky chemokiny. Buňky buněčné adheze zvyšuje koncentrace vápníku v endotelových buňkách a vede k buněčné spoje dezorganizace a zatažení cytoplasmy. Tímto způsobem se leukocyty mohou pohybovat na hranici endotelových buněk a procházet endotelem. Adhezní molekuly se také podílejí na tomto pohybu leukocytů.
krevní vlastnosti
endotelové funkce jsou složitější než jen řízení molekul a buněk procházejících endotelem. Endotelové buňky se také podílejí na krevním tlaku, koagulaci a některých dalších vlastnostech krve.
předpokládá se, že primitivní oběhový systém se objevil před 600 miliony let u bezobratlých, ale postrádal endotel. Endotelové buňky se objevily před 100 miliony let a poskytovaly krvi laminárnější tok (nikoli turbulentní), a proto účinnější výměnu plynů.
endotelové buňky modulují krevní tlak uvolňováním látek, které působí na hladké svalstvo cév. Uvolňují oxid dusnatý (NO) a prostacyklin, které uvolňují hladkou svalovinu cév. Uvolňují také endotelin a faktor aktivátoru krevních destiček, oba snižují průměr krevních cév. Oxid dusnatý se konstitutivně uvolňuje a poskytuje správný svalový tonus, inhibuje agregaci krevních destiček a adhezi leukocytů. Endotelin je silný vazokonstriktor. Jak endoteliálních buněk rozhodnout, co molekula má být propuštěn, zatím není jasné, ale mechanorreceptors v jejich apikální membrány, které jsou schopny cítit tok vlastnosti krve může být věrohodné.
za normálních podmínek uvolňují endotelové buňky molekuly do krve, které pomáhají udržovat správnou tekutost. Pracují na dvou úrovních: tekutost (antikoagulancia) a prevence agregace krevních destiček (antitrombotika). Proteiny C A S jsou důležité molekuly ovlivňující tekutost krve. C protein, tvořící komplex s proteinem S, inaktivuje koagulační faktory VIIIa a Va. S protein je syntetizován endoteliálními buňkami. Kromě toho endoteliální glykokalix obsahuje glykosaminoglykan podobný heparinu, který je schopen inaktivovat trombin.
v souvislosti s jejich antikoagulační funkci, endoteliální buňky, uvolnění oxidu dusnatého a prostacyklinu, jak roste cyklického AMP v krevních destiček a tvorby obtížnější agregaci krevních destiček. Tyto dvě molekuly se kontinuálně uvolňují do krve. Endotelové buňky mají ve svých apikálních membránách ektonukleázy, které odstraňují ATP a ADP, oba silné promotory agregace krevních destiček. Kromě toho endotelové buňky uvolňují molekulu aktivátoru, která transformuje plaminogen na plazmin, což podporuje odstranění trombů.
všechny tyto molekulární dráhy se mohou změnit, když endotelové buňky obdrží některé signály nebo jsou poškozeny tkáně, což vede ke koagulaci krve a agregaci krevních destiček. Za těchto okolností se endotelové buňky stávají aktivními účastníky koagulace a trombózy.
imunitní obrana
endotelové buňky hrají hlavní roli v imunitní obraně a jsou zapojeny do dvou mechanismů: prezentace antigenů na T lymfocyty a nábor imunitních buněk. Spolu s makrofágy, endoteliální buňky mohou prezentovat antigeny T lymfocytů, protože se constitutively express MHC-I (hlavní histokompatibilní komplex) a může být vyvolán express MHC-II, oba nezbytné pro antigen prezentace. Endotelové buňky jsou schopny aktivovat imunitní paměť, ale ne nové T lymfocyty. Mezi endoteliálními buňkami a T lymfocyty existuje obousměrná aktivace, takže molekuly uvolňování endotelových buněk pro přilákání zánětlivých buněk a expresní adhezní molekuly pro ukotvení krevních leukocytů.
Bibliografie
Cines BD, Pollak ES, Buck CA, Loscalzo J, Zimmerman GA, McEver RP, Pober JS, Knot TM, Konkle BA, Schwartz BS, Barnathan ES, McCrae KR, Obejmout, BA, Schmidt M, Stern DM 1998. Endotelové buňky ve fyziologii a patofyziologiivaskulárních poruch. Časopis Americké hematologické společnosti. 91:3527-3561
Fajardo LF. 1988. Složitost endotelových buněk. American journal of clinical pathology. 92:241-250.
Michiels c.2003. Funkce endotelových buněk. Žurnál buněčné fyziologie. 196: 430-443